Контрольная работа: Химические процессы в биологическом организме
Первичная структура белков определяет все остальные уровни организации белковой молекулы. Поэтому при изучении биологической функции различных белков важно знание этой структуры. Первым белком, для которого была установлена аминокислотная последовательность, был гормон поджелудочной железы — инсулин. Эта работа, потребовавшая 11 лет, была выполнена английским биохимиком Ф. Сенгером (1954). Он определил расположение 51 аминокислоты в молекуле гормона и показал, что она состоит из 2-х цепей, соединенных дисульфидными связями. Позже большая часть работ по установлению первичной структуры белков была автоматизирована. С развитием методов генетической инженерии появилась возможность еще более ускорить этот процесс, определяя первичную структуру белков в соответствии с результатами анализа нуклеотидной последовательности в генах, кодирующих эти белки. Вторичную и третичную структуру белков исследуют с помощью достаточно сложных физических методов, например, кругового дихроизма или рентгеноструктурного анализа белковых кристаллов. Третичная структура была впервые установлена английским биохимиком Дж. К. Кендрю (1957) для белка мышц — миоглобина.
4. Дайте сравнительную характеристику всех видов РНК. Оформите ответ в виде таблицы, указав молярную массу, минорные основания, углеводы, структуру, место локализации, функции
синтез белок аминокислота
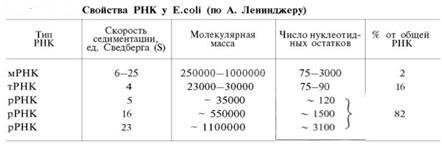
О количестве РНК нет точных данных, поскольку содержание ее в разных клетках в значительной степени определяется интенсивностью синтеза белка. На долю РНК приходится около 5–10% от общей массы клетки. Современная классификация различных типов клеточной РНК основывается на данных топографии, функции и молекулярной массы. Выделяют три главных вида РНК: матричную (информационную) – мРНК, которая составляет 2–3% от всей клеточной РНК; рибосомную – рРНК, составляющую 80–85% и транспортную – тРНК, которой около 16%. Эти 3 вида различаются нуклеотидным составом и функциями (табл. 1).
Таблица 1.
5. Фермент лактатдегидрогенеза окисляет молочную кислоту в пировиноградную. Покажите с помощью уравнения данной реакции механизм действия кофермента НАД
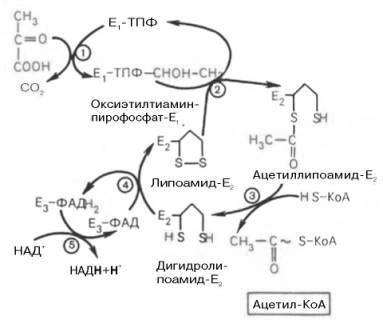
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
На I стадии этого процесса пируват теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидроли-поилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением.
На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид–Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидро-липоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н+.
Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, ди-гидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 кофер-ментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, ли-поамид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД).
6. Объясните комплементарный механизм репликации ДНК и его роль в обеспечении специфичности воспроизведения структуры. Дайте соответствующие схемы
Нуклеиновые кислоты (ДНК и РНК) относятся к сложным высокомолекулярным соединениям, состоят из небольшого числа индивидуальных химических компонентов более простого строения. Так, при полном гидролизе нуклеиновых кислот (нагревание в присутствии хлорной кислоты) в гидролизате обнаруживают пуриновые и пиримидиновые основания, углеводы (рибоза и дезоксирибоза) и фосфорную кислоту :
В молекуле ДНК углевод представлен дезоксирибозой, а в молекуле РНК – рибозой, отсюда их названия: дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК) кислоты. Кроме того, они содержат фосфорную кислоту, по два пуриновых и по два пиримидиновых основания; различия только в пиримидиновых основаниях: в ДНК содержится тимин, а в РНК – урацил. В составе ДНК и РНК открыты так называемые минорные (экзотические) азотистые основания (строение некоторых из них приводится далее).
Углеводы (рибоза и дезоксирибоза) в молекулах ДНК и РНК находятся в β-D-рибофуранозной форме:
В составе некоторых фаговых ДНК обнаружена молекула глюкозы, которая соединяется гликозидной связью с 5-оксиметилцитозином.
Основу структуры пуриновых и пиримидиновых оснований составляют два ароматических гетероциклических соединения – пиримидин и пурин :
Молекула пурина состоит из двух конденсированных колец: пиримидина и имидазола.
В составе нуклеиновых кислот встречаются три главных пиримидиновых основания: цитозин, урацил и тимин.
7. Какие метаболиты образуются в результате окислительного дезаминирования глутаминовой кислоты, аспарагиновой кислоты и аланина? Напишите уравнения реакций дальнейшего превращения метаболитов в организме. Назовите ферменты, катализирующие эти процессы
Активация фосфорилазы, как видно из рассмотренного выше цикла, должна сопровождаться снижением активности гликогенсинтетазы. Этот фермент также существует в двух формах, однако, в этом случае активная форма не фосфорилирована. При фосфорилировании соответствующей протеинкиназой она превращается в неактивную гликоген синтетазу.
Следовательно, изображенный выше цикл синтеза и фосфоролиза гликогена следует дополнить довольно сложной схемой взаимопревращений активных и неактивных форм ферментов, катализирующих эти процессы:
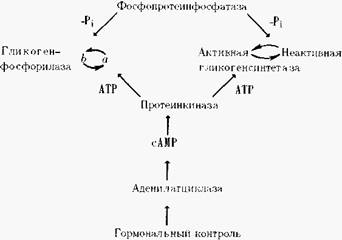
Необходимо иметь в виду, что и эта схема сильно упрощена. Выяснилось, что активность протеинкиназы может регулироваться калъмодулином - белком, связывающим ионы кальция, — и, следовательно, зависит от концентрации в клетке и этого вторичного мессенджера.
Аналогично, фосфорилированием и дефосфорилированием контролируется активность целого ряда других метаболических ферментов, в частности синтетазы жирных кислот, пируватдегидрогеназы. Важно подчеркнуть, что реакции фосфорилирования и дефосфорилирования коренным образом отличаются от аллостерической регуляции ферментов, поскольку они не находятся в прямой зависимости от биохимического статуса клетки и, следовательно, могут использоваться для изменения активности под воздействием внеклеточных сигналов, они удобны для регуляции на уровне организма. Известны и другие протеинкиназы, фосфорили-рующие остатки серина или треонина в белках, в том числе независимые от сАМР или контролируемые cGMP, диацилглицерином.
Выбор остатка серина, подвергаемого фосфорилированию, может зависеть от последовательности аминокислот, которые его окружают, Так, сАМР-зависимая протеинкиназа быка фосфорилирует гидроксильную группу серина в последовательности Arg-Arg-Ala-Ser-Val (Leu), причем соседствующие остатки аргинина, видимо, направляют фермент.
Фосфорилирование по остаткам тирозина, которое катализируется специфическими протеинкиназами (тирозинкиназами), встречается значительно реже, чем фосфорилирование остатков серина и треонина, — на долю фосфотирозина приходится около 0,1% всего связанного с белком фосфата. Однако биологическая роль этой реакции очень велика, так как она активно используется для передачи сигналов в биологических системах.
8. Напишите уравнение реакции фосфолирирования галактозы при участии соответствующей киназы и дальнейшего перехода фасфарного эфира галактозы во фруктозу 6-фосфат. Дайте полное название метаболитов и ферментов, ускоряющих эти реакции