Контрольная работа: Роль кальция в возбуждении клетки
В мембране нервов и мышечных волокон содержится большое количество потенциалзависимых кальциевых каналов. Кальций, входящий в клетку через эти каналы во время потенциала действия, оказывает влияние на самые разные процессы. К примеру, кратковременное увеличение уровня кальция в ходе потенциала действия вызывает секрецию как секрецию химических медиаторов в нервном окончании, так и сокращение мышечного волокна.
В некоторых мышечных волокнах и нейронах кальциевые токи достигают такой величины, что либо вносят значительный вклад, либо полностью формируют фазу роста потенциала действия. Процесс этот носит регенеративный характер благодаря возрастанию gСа при деполяризации, точно такому, как у натриевых каналов (см. выше). Участие кальциевых каналов в потенциале действия было впервые изучено Фаттом и Гинзборгом, а впоследствии Хагиварой. Кальциевые потенциалы действия описаны в сердечной мышце, в целом ряде нейронов беспозвоночных, а также в нейронах вегетативной и центральной нервной системы позвоночных 60) . Наличие кальциевых потенциалов действия также показано в ненейрональных типах клеток, таких как ряд эндокринных клеток и некоторых яйцеклетках беспозвоночных. Потенциалзависимые кальциевые токи блокируются в миллимолярных концентрациях кобальтом, магнием или кадмием, добавленным во внеклеточный раствор.
Барий может заменить кальций в прохождении через пору канала; магний на это не способен. Поразительным примером сосуществования натриевых и кальциевых потенциалов действия в одном типе клеток является клетка Пуркинье в мозжечке млекопитающих. Натриевые потенциалы действия генерируются в теле клетки Пуркинье, в то время как кальциевые — в дендритах.
Ионы кальция и возбудимость
Ионы кальция влияют также на возбудимость мембраны: снижение внеклеточной концентрации кальция приводит к увеличению возбудимости; повышение внеклеточного уровня кальция, напротив, влечет за собой снижение возбудимости. Франкенхаузер и Ходжкиниспользовали метод фиксации потенциала для исследования этих эффектов в аксоне кальмара. Они обнаружили, что при снижении внеклеточной концентрации кальция происходит сдвиг потенциала зависимости активации натриевых каналов таким образом, что для достижения порога и генерации натриевого тока нормальной величины требовались меньшие уровни деполяризации. Снижение уровня необходимой деполяризации было постоянным во всем диапазоне возбудимости и зависело от концентрации кальция. Пятикратное повышение внеклеточного уровня кальция приводило к снижению порогового уровня деполяризации на 10-15 м В.
Франкенхаузер и Ходжкин предположили, что этот эффект может быть обусловлен тем, что ионы кальция частично заслоняют (или экранируют) отрицательные заряды, расположенные на внешней поверхности мембраны. Подобное воздействие на мембрану может оказать, к примеру, гликолизация мембранных белков последовательностями углеводов, содержащими отрицательно заряженную сиаловую кислоту. Натриевый канал ската сам по себе обладает более чем 100 остатками сиаловой кислоты. При условии заслонения зарядов градиент потенциала на мембране будет равен измеряемому потенциалу покоя. После устранения кальция, заряды, лишенные экранирования, увеличат отрицательный заряд на внешней стороне мембраны, тем самым снижая общий электрический градиент. Эта гипотеза вносит новый ракурс в понимание мембранного потенциала: разность потенциалов между внутри- и внеклеточным растворами определяется вне- и внутриклеточной концентрациями ионов, а также проводимостями. Однако, форма градиента потенциала может зависеть от заряженных молекул, связанных с поверхностью мембраны. Для потенциалчувствительных элементов мембраны этот эффект будет иметь огромное значение, поскольку они распознают лишь те градиенты потенциала, которые находятся в непосредственной близости от них.
Одна из проблем с гипотезой поверхностного заряда состоит в том, что удаление внеклеточного кальция должно повлиять не только на активацию, но и на инактивацию натриевых каналов, а также на активацию калиевых. Снижение порога натриевой инактивации и калиевой активации приведет тогда к снижению возбудимости. В силу неизвестных причин, влияние устранения кальция на эти параметры гораздо менее выражено, чем влияние на активацию натриевых каналов. Возможно, это и не удивительно, что локальные изменения электрического градиента оказывают столь разное влияние на различные молекулы канала, или даже на разные участки одной и той же молекулы, в зависимости от расположения потенциалчувствительного элемента относительно поверхностных зарядов. Какими бы ни были причины этих различий, общий эффект кальция заключается в стабилизации мембраны и внесении дополнительной степени надежности при варьировании уровня потенциала мембраны между покоем и порогом для потенциала действия.
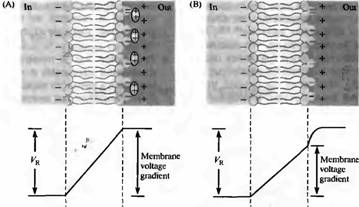 |
Рис. 1. Влияние поверхностного заряда на мембранный потенциал. (А) Нейтрализация двухвалентными катионами отрицательных зарядов в структуре мембраны. (В) Устранение экранирующих элементов (например, кальция) изменяет распределение заряда и градиент потенциалов на мембране, но не потенциал покоя. |
Вклад открытых калиевых каналов в реполяризацию
Кроме выпрямителя с задержкой, в нейронах имеется целый ряд других типов калиевых каналов некоторые из которых принимают участие в реполяризации мембраны. Один из таких каналов — это Α-канал, быстро активируемый в результате деполяризации. Вклад Α-каналов в реполяризацию в ходе потенциала действия минимален по двум причинам: они быстро инактивируются, и в большинстве клеток активация этого типа каналов возможна лишь при условии предварительной гиперполяризации (т. е. они инактивированы в состоянии покоя). Два других типа потенциалзависимых калиевых каналов, М-канал и S-канал, похожи на выпрямитель с задержкой тем, что открываются в ответ на деполяризацию. Дополнительное свойство М-каналов состоит в том, что они инактивируются ацетилхолином через мускариновые АХ рецепторы (отсюда название). S-каналы открыты в покое и инактивируются серотонином.
Кальций-активируемые калиевые каналы также могут вносить вклад в реполяризацию. В ходе потенциала действия кальций входит в клетку через потенциалзависимые кальциевые каналы. Во многих типах клеток такое повышение уровня кальция способствует увеличению калиевой проводимости, которая способствует реполяризации и приводит к последующей гиперполяризации. Существует как минимум три подтипа кальций-активируемых калиевых каналов, с очень большим (200 пСм), средним (30 пСм) и малым (10 пСм) уровнями проводимости. Наличие этих каналов можно продемонстрировать экспериментально посредством повышения уровня кальция внутри клетки, например, путем инъекции через внутриклеточную микропипетку. Вслед за такой инъекцией проводимость мембраны резко возрастает и мембранный потенциал покоя приближается к калиевому равновесному потенциалу. По мере устранения излишков кальция из цитоплазмы за счет внутриклеточных буферов и выброса кальция из клетки, сопротивление и потенциал возвращаются к своему нормальному уровню. Существует также тип калиевых каналов, активируемый внутриклеточным натрием. В некоторых клетках активация таких каналов может вносить вклад в реполяризацию в ходе потенциала действия
Свойства канала, связанные с потенциалом действия
В ходе экспериментов методом пэтч-кламп на крысиных мышечных волокнах в культуре, проводимость потенциалзависимых натриевых каналов была измерена непосредственно и составила 20 пСм (рис. 1); подобные измерения в мотонейронах крысы выявили проводимость величиной 14 пСм. Плотность натриевых каналов была измерена в ряде тканей методом исследования плотности мест связывания ТТХ. Используя меченый тритием тетродотоксин, Левинсон и Мевес определили, что на один квадратный микрометр мембраны аксона кальмара приходится приблизительно 553 места связывания молекулы токсина. Цифры, полученные в других тканях, варьируют от 2 молекул на мкм2 в оптическом нерве новорожденных крысятдо 2 000 в перехвате Ранвье седалищного нерва кролика. Плотность натриевых каналов в скелетной мышце была измерена методом локальной деполяризации небольшого участка мембраны с помощью внеклеточной пипетки при одновременном измерении натриевого тока, протекающего через этот участок мембраны. Результаты варьировали от одного участка к другому, что указывает на неравномерность распределения каналов в мембране. Плотность была наибольшей в районе концевой пластинки, снижалась по мере удаления от нее и достигала 10 % от максимального уровня по мере приближения к сухожилию. Кроме того, было показано, что натриевые каналы в мышце группируются в кластеры.
Проводимость калиевых каналов, ответственных за позднюю составляющую тока, была измерена в препарате вскрытого аксона кальмара. Каналы типа «выпрямитель с задержкой» обладают проводимостью 10, 20 и 40 пСм, причем наиболее часто встречается канал с проводимостью 20 пСм. Подобно натриевым, калиевые каналы мышцы лягушки распределены не равномерно, а кластерами. Тем не менее, паттерны расположения кластеров натриевых и калиевых каналов не совпадают между собой. Выпрямители с задержкой полностью отсутствуют в перехватах Ранвье миелинизированного нерва кролика, так как в ответ на деполяризацию поздний выходящий ток не возникает. В ходе потенциала действия реполяризация после быстрой инактивации натриевых каналов достигается за счет большого тока утечки.
Выводы
Потенциал действия в большинстве клеток возникает за счет кратковременного возрастания натриевой проводимости, которое стремится привести мембранный потенциал к уровню натриевого равновесного потенциала и за которым следует увеличение калиевой проводимости, возвращающее мембрану в состояние покоя.
Возрастание проводимостей возникает благодаря потенциалзависимости натриевых и калиевых каналов: вероятность их открытия возрастает при деполяризации.
Эксперименты на аксоне кальмара с фиксацией потенциала предоставили детальную информацию о потенциалзависимости и временном ходе изменений проводимостей. При деполяризации мембраны натриевая проводимость сначала быстро активируется, а затем инактивируется. Калиевая проводимость активируется с задержкой и остается на высоком уровне до тех пор, пока не кончится деполяризация.
Временной ход и потенциалзависимость изменений натриевых и калиевых проводимостей в точности определяют амплитуду и временной ход потенциала действия, а также такие характеристики мембраны, как порог активации и рефрактерный период.
Теоретически активация натриевой и калиевой проводимостей при деполяризации должна быть связана со смещением заряда внутри клетки. Эти смещения, называемые воротными токами, удалось измерить экспериментально.
Эксперименты с использованием метода пэтч-кламп дополнили сведения, полученные в более ранних опытах с фиксацией потенциала, новыми деталями о процессе возбуждения. Так, например, натриевые каналы открываются на довольно короткое время, и вероятность их открытия в ходе деполяризации сначала возрастает, а затем снижается, в соответствии с активацией и инактивацией натриевой проводимости в целой клетке. Различные кинетические модели были предложены с целью описания процессов активации и инактивации каналов.
Кальций играет важную роль в возбуждении. В некоторых клетках именно вход кальция, а не натрия, отвечает за фазу роста потенциала действия. Кроме того, внеклеточный уровень кальция определяет возбудимость мембраны. Снижение внеклеточной концентрации кальция приводит к увеличению возбудимости
Литература
1. Фролов М.В., Милованова Г.Б. Электрофизиологические помехи и контроль состояния оператора.
2. Системные аспекты психической деятельности. Под ред. Судакова К.В. и др.
3. Терлецкий Н.А. О пользе и вреде излучения для жизни. (Relata Refero.)