Курсовая работа: Электрохимические методы анализа и их современное аппаратурное оформление: обзор WEB–сайтов фирм–продавцов химико-аналитического оборудования
Вольтамперограммы, полученные с помощью вращающегося или капающего электрода при монотонном изменении (линейной развертке) напряжения, имеют вид, схематически представленный на рисунке. Участок увеличения тока наз. волной. Волны м. б. анодными, если электроактивное вещество окисляется, или катодными, если оно восстанавливается. Когда в растворе присутствуют окисленная (Ох) и восстановленная (Red) формы вещества, достаточно быстро (обратимо) реагирующие на микроэлектроде, на вольтамперограмме наблюдается непрерывная катодно-анодная волна, пересекающая ось абсцисс при потенциале, соответствующем окислительно-восстановитановительному потенциалу системы Ox/Red в данной среде. Если электрохимическая реакция на микроэлектроде медленная (необратимая), на вольтамперограмме наблюдаются анодная волна окисления восстановленной формы вещества и катодная волна восстановления окисленной формы (при более отрицат. потенциале). Образование площадки предельного тока на вольтамперограмме связано либо с ограниченной скоростью массопереноса электроактивного вещества к поверхности электрода путем конвективной диффузии (предельный диффузионный ток, Id ), либо с ограниченной скоростью образования электроактивного вещества из определяемого компонента в растворе. Такой ток называется предельным кинетическим, а его сила пропорциональна концентрации этого компонента.
Форма волны для обратимой электрохимические реакции описывается уравнением:
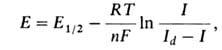
где R-газовая постоянная, Т-абсолютная температура, E1/2 -потенциал полуволны, т.е. потенциал, соответствующий половине высоты волны (Id /2;). Значение E1/2 характерно для данного электроактивного вещества и используется для его идентификации. Когда электрохимические реакции предшествует адсорбция определяемого вещества на поверхности электрода, на вольтамперограммах наблюдаются не волны, а пики, что связано с экстремальной зависимостью адсорбции от потенциала электрода. На вольтамперограммах, зарегистрированных при линейном изменении (развертке) потенциала со стационарным электродом или на одной капле капающего электрода (устар. - осциллографич. полярограмме), также наблюдаются пики, нисходящая ветвь которых определяется обеднением приэлектродного слоя раствора электроактивным веществом. Высота пика при этом пропорциональна концентрации электроактивного вещества. В полярографии предельный диффузионный ток (в мкА), усредненный по времени жизни капли, описывается уравнением Ильковича:
![]()
где n-число электронов, участвующих в электрохимической реакции, С-концентрация электроактивного вещества (мМ), D-eгo коэффициент диффузии (см2 /с),![]() время жизни ртутной капли (с), m-скорость вытекания ртути (мг/с).
время жизни ртутной капли (с), m-скорость вытекания ртути (мг/с).

С вращающимся дисковым электродом предельный диффузионный ток рассчитывают по уравнению:
![]()
где S-площадь поверхности электрода (см2 ),![]() -круговая частота вращения электрода (рад/с), v-кинематическая вязкость раствора (см2 /с), F-число Фарадея (Кл/моль).
-круговая частота вращения электрода (рад/с), v-кинематическая вязкость раствора (см2 /с), F-число Фарадея (Кл/моль).
Циклическая вольтамперометрия (вольтамперометрия с относительно быстрой треугольной разверткой потенциала) позволяет изучать кинетику и механизм электродных процессов путем наблюдения на экране осциллографической трубки с послесвечением одновременно вольтамперограмм с анодной и катодной разверткой потенциала, отражающих, в частности, и электрохимические реакции продуктов электролиза.
Нижняя граница определяемых концентраций Сн в методах В. с линейной разверткой потенциала составляет 10-5 -10-6 М. Для ее снижения до 10-7 -10-8 М используют усовершенствованные инструментальные варианты - переменно-токовую и дифференциальную импульсную вольтамперометрию.
В первом из этих вариантов на постоянную составляющую напряжения поляризации налагают переменную составляющую небольшой амплитуды синусоидальной, прямоугольной (квадратноволновая вольтамперометрия), трапециевидной или треугольной формы с частотой обычно в интервале 20-225 Гц. Во втором варианте на постоянную составляющую напряжения поляризации налагают импульсы напряжения одинаковой величины (2-100 мВ) длительностью 4-80 мс с частотой, равной частоте капания ртутного капающего электрода, или с частотой 0,3-1,0 Гц при использовании стационарных электродов. В обоих вариантах регистрируют зависимость от U или Е переменной составляющей тока с фазовой или временной селекцией. Вольтамперограммы при этом имеют вид первой производной обычной вольтамперометрической волны. Высота пика на них пропорциональна концентрации электроактивного вещества, а потенциал пика служит для идентификации этого вещества по справочным данным.
Пики различных электроактивных веществ, как правило, лучше разрешаются, чем соответствующие вольтамперометрические волны, причем высота пика в случае необратимой электрохимической реакции в 5-20 раз меньше высоты пика в случае обратимой реакции, что также обусловливает повышенную разрешающую способность этих вариантов вольтамперометрии. Например, необратимо восстанавливающийся кислород практически не мешает определению электроактивных веществ методом переменно-токовой вольтамперометрии. Пики на переменно-токовых вольтамперограммах отражают не только электрохимические реакции электроактивных веществ, но и процессы адсорбции - десорбции неэлектроактивных веществ на поверхности электрода (пики нефарадеевского адмиттанса, устар. - тенсамметрич. пики).
Для всех вариантов вольтамперометрии используют способ снижения Сн , основанный на предварительном электрохимическом, адсорбционном или химическом накоплении определяемого компонента раствора на поверхности или в объеме стационарного микроэлектрода, с последующей регистрацией вольтамперограммы, отражающей электрохимическую реакцию продукта накопления. Эту разновидность вольтамперометрии называют инверсионной (устар. название инверсионной В. с накоплением на стационарном ртутном микроэлектроде - амальгамная полярография с накоплением). В инверсионной вольтамперометрии с предварительным накоплением Сн достигает 10-9 -10-11 М . Минимальные значения Сн получают, используя тонкопленочные ртутные индикаторные электроды, в т.ч. ртутно-графитовые, состоящие из мельчайших капелек ртути, электролитически выделенных на подложку из специально обработанного графита.
Для фазового и элементного анализа твердых тел используют инверсионную вольтамперометрию с электроактивными угольными электродами (т. наз. минерально-угольными пастовыми электродами). Их готовят из смеси угольного порошка, исследуемого порошкообразного вещества и инертного связующего, напр. вазелинового масла. Разработан вариант этого метода, который дает возможность проводить анализ и определять толщину металлических покрытий. В этом случае используют специальное устройство (прижимная ячейка), позволяющее регистрировать вольтамперограмму, пользуясь каплей фонового электролита, нанесенного на исследуемую поверхность.
Применение
Вольтамперометрию применяют: для количественного анализа неорганических и органических веществ в очень широком интервале содержаний - от 10-10 % до десятков %; для исследования кинетики и механизма электродных процессов, включая стадию переноса электрона, предшествующие и последующие химические реакции, адсорбцию исходных продуктов и продуктов электрохимических реакций и т. п.; для изучения строения двойного электрического слоя с, равновесия комплексообразования в растворе, образования и диссоциации интерметаллических соединений в ртути и на поверхности твердых электродов; для выбора условий амперометрического титрования и др.
1.2 Кондуктометрия
Кондуктометрия - основана на измерении электропроводности раствора и применяется для определения концентрации солей, кислот, оснований и т.д. При кондуктометрических определениях обычно используют электроды из одинаковых материалов, а условия их проведения подбирают таким образом, чтобы свести к минимуму вклад скачков потенциала на обеих границах раздела электрод/электролит (например, используют переменный ток высокой частоты). В этом случае основной вклад в измеряемый потенциал ячейки вносит омическое падение напряжения IR, где R – сопротивление раствора. Электропроводность однокомпонентного раствора можно связать с его концентрацией, а измерение электропроводности электролитов сложного состава позволяет оценить общее содержание ионов в растворе и применяется, например, при контроле качества дистиллированной или деионизованной воды. В другой разновидности кондуктометрии – кондуктометрическом титровании – к анализируемому раствору порциями добавляют известный реагент и следят за изменением электропроводности. Точка эквивалентности, в которой отмечается резкое изменение электропроводности, определяется из графика зависимости этой величины от объема добавленного реагента.
1.3 Потенциометрия
Потенциометрия - применяется для определения различных физико-химических параметров исходя из данных о потенциале гальванического элемента. Электродный потенциал в отсутствие тока в электрохимической цепи, измеренный относительно электрода сравнения, связан с концентрацией раствора уравнением Нернста. В потенциометрических измерениях широко применяются ионоселективные электроды, чувствительные преимущественно к какому-то одному иону в растворе: стеклянный электрод для измерения рН и электроды для селективного определения ионов натрия, аммония, фтора, кальция, магния и др. В поверхностный слой ионоселективного электрода могут быть включены ферменты, и в результате получается система, чувствительная к соответствующему субстрату. Отметим, что потенциал ионоселективного электрода определяется не переносом электронов, как в случае веществ с электронной проводимостью, а в основном переносом или обменом ионов. Однако уравнение Нернста, связывающее электродный потенциал с логарифмом концентрации (или активности) вещества в растворе, применимо и к такому электроду. При потенциометрическом титровании реагент добавляют в анализируемый раствор порциями и следят за изменением потенциала. S-образные кривые, характерные для такого типа титрования, позволяют определить точку эквивалентности и найти такие термодинамические параметры, как константа равновесия и стандартный потенциал.
1.4 Амперометрия
Метод основан на измерении предельного диффузионного тока, проходящего через раствор при фиксированном напряжении между индикаторным электродом и электродом сравнения. При амперометрическом титровании точку эквивалентности определяют по излому кривой ток – объем добавляемого рабочего раствора. Хроноамперометрические методы основаны на измерении зависимости тока от времени и применяются в основном для определения коэффициентов диффузии и констант скорости. По принципу амперометрии (как и вольтамперометрии) работают миниатюрные электрохимические ячейки, служащие датчиками на выходе колонок жидкостных хроматографов. Гальваностатические методы аналогичны амперометрическим, но в них измеряется потенциал при прохождении через ячейку тока определенной величины. Так, в хронопотенциометрии контролируется изменение потенциала во времени. Эти методы применяются главным образом для изучения кинетики электродных реакций.
1.5 Кулонометрия.
В кулонометрии при контролируемом потенциале проводят полный электролиз раствора, интенсивно перемешивая его в электролизере с относительно большим рабочим электродом (донная ртуть или платиновая сетка). Полное количество электричества (Q, Кл), необходимое для электролиза, связано с количеством образующего вещества (А, г) законом Фарадея:
![]()
где M – мол. масса (г/моль), F число Фарадея. Кулонометрическое титрование заключается в том, что при постоянном токе электролитически генерируют реактив, вступающий во взаимодействие с определяемым веществом. Ход титрования контролируют потенциометрически или амперометрически. Кулонометрические методы удобны тем, что являются по своей природе абсолютными (т.е. позволяют рассчитать количество определяемого вещества, не прибегая к калибровочным кривым) и нечувствительны к изменению условий электролиза и параметров электролизера (площади поверхности электрода или интенсивности перемешивания). При кулоногравиметрии количество вещества, подвергшегося электролизу, определяют взвешиванием электрода до и после электролиза.
Существуют и другие электроаналитические методы. В переменно-токовой полярографии на линейно меняющийся потенциал налагают синусоидальное напряжение малой амплитуды в широкой области частот и определяют либо амплитуду и фазовый сдвиг результирующего переменного тока, либо импеданс. Из этих данных получают информацию о природе веществ в растворе и о механизме и кинетике электродных реакций. В тонкослойных методах используются электрохимические ячейки со слоемэлектролита толщиной 10–100 мкм. В таких ячейках электролиз идет быстрее, чем в обычных электролизерах. Для изучения электродных процессов применяют спектрохимические методы со спектрофотометрической регистрацией. Для анализа веществ, образующихся на поверхности электрода, измеряют поглощение ими света в видимой, УФ- и ИК-областях. За изменением свойств поверхности электрода и среды следят с помощью методов электроотражения и эллипсометрии, которые основаны на измерении отражения излучения от поверхности электрода. К ним относятся методы зеркального отражения и комбинационного рассеяния света (рамановская спектроскопия), спектроскопия второй гармоники (фурье-спектроскопия).