Курсовая работа: Химия каренов
В данном случае перегруппировка Вагнера-Меервейна, протекающая как алкильный сдвиг, не приводит к изменению карановой структуры. Однако алкильный сдвиг возможен лишь потому, что в образующемся вторичном ионе 16 делокализация заряда с участием циклопропанового кольца приводит к его раскрытию и образованию гомоаллильного иона 17 , обладающего меньшей энергией. Ион 17 стабилизируется путем выброса протона от одной из геминальных метильных групп, давая эфир 14 . В кислой среде этот эфир изомеризуется в эфир 15 через классический катион 18 .
2. Перегруппировки, протекающие через ионы с высокой степенью делокализации заряда
Очевидно, что в систему ЦПК - заряженный атом углерода может включаться одна или несколько двойных связей. Образующийся при этом гомопентадиенильный ион характеризуется большей степенью делокализации заряда, чем гомоаллильный, и имеет, соответственно, более низкую энергию. Поэтому реакции с участием гомопентадиенильных ионов протекают легче, чем с участием гомоаллильных. Изомеризация 4-карен-3-ола (19 ) в гидроксидиен 20 происходит при кипячении в воде даже в отсутствие кислотных катализаторов:26
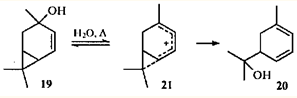
Как и при изомеризации соединений 6 и 7 , необратимость атаки по циклопропановому фрагменту иона 21 обусловливает региоспецифичность реакции.
Следует отметить, что соседство (и, возможно, сопряжение) двойной связи и ЦПК в нейтральной молекуле не является обязательным условием образования гомопентадиенильного иона и, следовательно, протекание скелетной перегруппировки. С точки зрения механизма интересна селективная изомеризация кар-3-ен-5-ола (22 ) в м -мента-1,3-диен-8-ол (20 ): двойную связь и ЦПК объединяет в систему сопряжения возникающий между ними карбокатаонный центр.27
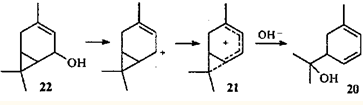
В систему сопряжения катионоидный центр - ЦПК может включаться не только соседняя двойная связь, но также и второй трехчленный карбоцикл. Участие такого интермедиата в реакции приводит к перегруппировке трициклооктанового скелета в замещенный циклогептадиен.28 Эта перегруппировка интересна тем, что в данном случае гем -дихлорциклопропановое кольцо раскрывается по внутренней связи, а гем -диметилциклопропановое — по внешней.
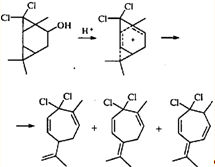
Из приведенных выше примеров ионных перегруппировок видно, что для гем -диметилциклопропанового кольца раскрытие по внешней связи является закономерностью, практически не знающей исключений. Трехчленный цикл, связанный с двумя атомами галогена, напротив, может вести себя по-разному. При метанолизе аддукта 3-карена с дибромкарбеном ЦПК раскрывается по двум направлениям, приводя к продуктам как с сохранением карановой структуры, так и к продуктам перегруппировки.29

То, что трехчленные циклы в ионных реакциях раскрываются по разным связям, может быть обусловлено природой геминальных заместителей. гем -Диметильная группировка укорачивает (и усиливает) противолежащую связь циклопропана,30 а два геминальных атома хлора удлиняют и ослабляют ее. Геминальные атомы брома действуют таким же образом, но слабее.31
Чрезвычайно легко протекает ацетолиз тозилата 23; 32 в данном случае интермедиатом является гомогептатриенильный ион 24 , в котором степень делокализации заряда еще выше, чем в гомопентадиенильном.

Выше было сказано, что гомоаллильные и гомопентадиенильные перегруппировки являются необратимыми, однако это утверждение не совсем корректно. Действительно, подобные превращения карановых производных можно провести со 100%-ной степенью конверсии. Это обусловлено геометрией иона и образующейся молекулы. Атом углерода ЦПК при С(2), не включенный в цепь сопряжения, в гомоаллильном ионе, в процессе его стабилизации меняет гибридизацию с sp2 на sp3 При этом угол С(1)—С(2)—С(3), равный в молекуле циклопропана 60°, в конечной молекуле увеличивается до 109°, что вызывает, в свою очередь, увеличение расстояния между атомами С(1) и С(3). Однако если эти атомы удастся каким-то образом сблизить, вновь становится возможным образование гомоаллильного иона.

На практике соединения с ментановым скелетом никогда не превращаются в карановые. Однако именно в карановых структурах, благодаря особенностям их строения, можно наблюдать ретро-гомоаллильную перегруппировку, при которой гомоаллильный ион образуется из линейного фрагмента молекулы и приводит к замыканию трехчленного цикла. Эффект подобного рода наблюдался при взаимодействии тозилата 25 с лчтийалюминийгидридом,33 триэтилалюминием,34 а также при его сольволизе.35
Очевидно, что в идеальном случае эта реакция должна протекать по механизму SN 1. Однако скорее всего в реакции участвуют контактные ионные пары: происходит очень сильная поляризация субстрата с почти полным разделением зарядов, но образовавшийся катион стабилизирован противоионом. Отщепление тозилатной группы в соединении 25 приводит к катиону с зарядом на первичном атоме углерода, который гораздо менее стабилен, чем третичные ионы, образующиеся при протонировании ЦПК. Стабилизация иона может осуществляться путем сопряжения заряженного атома с двойной связью, причем перекрывание p -орбиталей происходит не вдоль σ -связи, а через пространство ("throughspace").

Сближению этих фрагментов способствует тесное сольватное окружение, поскольку процесс должен происходить быстро. Этот путь приводит к образованию гомоаллильного иона 26 и/или дигомопентадиенильного иона 27 . В том случае, когда интермедиатом является ион 27 , происходит совершенно необычная перегруппировка: фактически одна молекула претерпевает одновременно две перегруппировки различной направленности — гомоаллильную, приводящую к раскрытию циклопропанового кольца, и ретро-гомоаллильную, приводящую к замыканию нового трехчленного карбоцикла.
Тут уместно привести чрезвычайно интересный факт: 2-тозилоксиметил-3-карен (28 ) при ацетолизе дает тот же эфир 29 , что и 4-тозилоксиметил-2-карен (25 ).36

Механизм образования ацетата 29 пока не выяснен. Обращает внимание также отсутствие продуктов, образования которых можно было бы ожидать, опираясь на данные по превращениям эфира 25 . Известно еще одно достаточно необычное превращение тозилата 28 : при пиролизе он дает тот же углеводород, что и тозилат 25 , а именно 1-метил-4-изопропенилбицикло[4.1.0]гепт-2-ен (30 ).36

Механизм пиролиза эфира 25 37 будет рассмотрен ниже, как и возможный механизм пиролиза тозилата 28 .
Механизмы ионных перегруппировок, включающих ионы с делокализованным по цепи сопряжения зарядом, являются, конечно, гипотетическими, основанными на строении конечных продуктов. До сих пор неясно, действительно ли возможно сопряжение в таких системах. Ниже, при рассмотрении гидрирования 2-карена (31 ) будет показано, что соседство двойной связи и ЦПК отнюдь не гарантирует их сопряжения, по крайне мере в основном состоянии нейтральной молекулы. 17,38 Было бы чрезвычайно полезно проверить с помощью современных квантово-химических расчетов, возможна ли при перегруппировках соединений ряда карана делокализация заряда в системе сопряжения, в которой одним из элементов является ЦПК.
III. Перегруппировки, протекающие по радикальному механизму
Радикальные перегруппировки монотерпеноидов каранового ряда происходят, как правило, при фотохимических реакциях. Фотохимические превращения таких соединений достаточно подробно описаны в обзоре 12 . Для 3-карена перегруппировки в условиях облучения не наблюдались. Известно лишь его фотохимическое окисление с образованием трех гидропероксидов.39 Изомерный 2-карен при облучении в присутствии сенсибилизатора перегруппировывается в 1,4,4-триметилбицикло[3.2.0]гепт-2-ен (32 ), который был использован для синтеза грандизола.4
