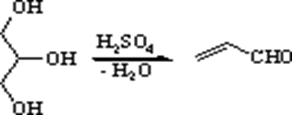Курсовая работа: Методи синтезу хінолінів
Хінолінове ядро є структурним фрагментом молекул деяких алкалоїдів та лікарських засобів.
8‑Гідроксихінолін. Це безбарвна кристалічна речовина (т. пл. 75–76 °С) з характерним запахом, малорозчинна у воді, розчинна у хлороформі, діетиловому ефірі та бензолі. 8‑Гідроксихінолін добувають нагріванням орто- амінофенолу з гліцерином і сірчаною кислотою в присутності орто-нітрофенолу (синтез Скраупа) або сплавленням 8‑хінолінсульфокислоти з лугами.
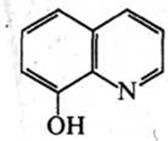
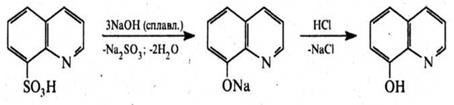
З іонами багатьох металів (Mg2+ , Al3+ , Zn2+ , Mn2+ , Со2+ , Ni2+ , Cu2+ , Fe»+ , Fe'+ та ін.) 8‑гідроксихінолін утворює малорозчинні у воді комплекси (хелати).
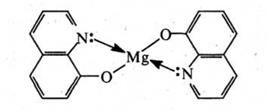
На цій властивості ґрунтується застосування 8‑гідроксихіноліну як аналітичного реагенту.
Ряд похідних 8‑гідроксихіноліну використовуються в медичній практиці як протимікробні засоби. До них відносяться такі лікарські препарати, як хінозол, нітроксолін (5‑НОК) і ентеросептол:
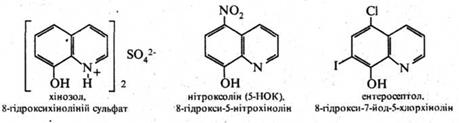
Вважають, що їх бактерицидна дія викликана зв'язуванням іонів Со2+ , необхідних для життєдіяльності мікроорганізмів.
Ізохінолін (бензо[с ] піридин) є ізомером хіноліну. Молекула ізохіноліну, як і хіноліну, складається з конденсованих піридинового та бензольного циклів, але, на відміну від хіноліну, цикли з'єднані вздовж зв'язку С3 -С4 піридинового кільця.
Нумерацію атомів ізохінолінового ядра проводять згідно з правилами ІЮПАК наведеним способом.
Ізохінолін безбарвна кристалічна речовина (т. пл. 24,6 °С), розчинна у воді, етанолі, діетиловому ефірі, хлороформі та бензолі.
За хімічними властивостями ізохінолін мало чим відрізняється від хіноліну. За рахунок гетероатома він виявляє оснбвні властивості та легко утворює солі з кислотами, алкіл- і ацилгалогенідами. Як основа ізохінолін трохи сильніше хіноліну (рКВН + ізохіноліну 5,14; рКВН + хіноліну 4,94).
Реакції електрофільного заміщення, як і в ядрі хіноліну, проходять здебільшого в положеннях 5 і 8. Нуклеофільне заміщення в ізохіноліновому циклі відбувається переважно у положенні 1.
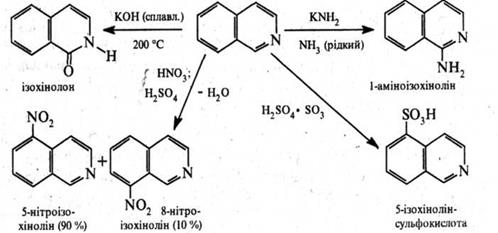
При відновленні ізохіноліну, як і у молекулі хіноліну, в першу чергу гідрується піридинове ядро. Так, при дії натрієм в етанолі або воднем над нікелевим каталізатором ізохінолін відновлюється до 1,2,3,4‑тетрагідроізохіноліну.
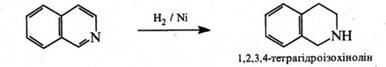
За жорсткіших умов гідруванню піддається і бензольне кільце. При окисненні ізохіноліну лужним розчином КМпО4 утворюється суміш фталевої та 3,4‑піридиндикарбонової кислот:
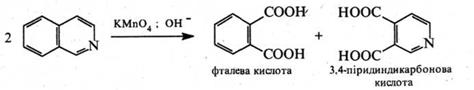
Під дією органічних пероксикислот ізохінолін окиснюється по гетероатому, утворюючи N‑оксид.
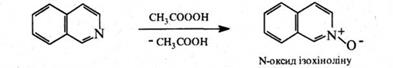
Ядро ізохіноліну є структурним фрагментом молекул алкалоїдів ізохінолінового ряду – папаверину, морфіну, кодеїну та ін.
1.4 Застосування хінолінів
Хінолінова циклічна система значно поширена в природі. Хіноліновий кістяк протягом тривалого часу був основою для пошуку синтетичних противомалярійних препаратів. Один з таких препаратів – хлорохін. Ціанінові барвники також складають значну частку в комерційній продукції на основі хінолінової сировини. Вони застосовуються для сенсибілізації фотографічних емульсій до червоних і інфрачервоних променів, що не діють на бромисте срібло без сенсибілізації. Найпростішим барвником цього типу є етиловий червоний. Тетрагідропохідна оксамніхін використовується для боротьби із шистосомой, що служить основною причиною захворювання в тропічних регіонах. На основі синтезу похідних хіноліну з ізатину, можна одержати багато інших хіміко-фармацевтичних препаратів. 8‑оксихінолін (оксин) широко використовується в аналітичній хімії для виявлення багатьох металів, що дають з ними внутрікомплексні солі оксинати (хелати) за рахунок участі вільної пари електронів азоту, а також як дезинфікуючі засоби (хіназол), 5‑хлор‑7‑йод‑8‑Оксихінолін (ентеросептол) застосовується для боротьби з кишковими захворюваннями. Він настільки повно зв'язує іонний кобальт (кобаламіну – вітаміну B12 ), що вижитти бактерій неможуть. Хінолін часто використовується в лабораторії в якості висококиплячого основного розчинника.
2. Характеристика методів синтезу хінолінів
2.1. Синтез хіноліну Скраупа
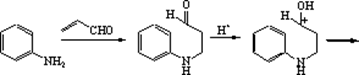
Основним методом одержання хіноліну є синтез Скраупа, що полягає у взаємодії аніліну або заміщених анілінів із гліцерином, у присутності сірчаної кислоти й окислювача, у якості якого часто використовують нітробензол, мета-нітробензолсульфокислоту, а іноді і просто кисень повітря.
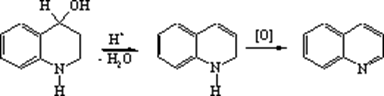
На першій стадії гліцерин під дією сірчаної кислоти дегідратується з утворенням акролеїну. Далі відбувається приєднання аніліну до акролеїну по типу реакції Михаеля. Унаслідок протонування альдегідної групи, що утвориться в інтермедіаті відбувається її активація як електрофіла, що приводить до замикання гетероциклу в результаті електрофільного заміщення в орто-положення бензольного кільця. Наступна дегідратація приводить до дигідропохіного хіноліну, а потім окисляється окислювачем за наявності в реакційному середовищі у хінолін. Використовуваний як окислювач нітроарен відновлюється у відповідний анілін.