Курсовая работа: Основания
Названия гидроксидов составляются из слова « гидроксид » и русского названия элемента в родительном падеже с указанием, если это необходимо, степени окисления элемента (римскими цифрами в скобках). Например, LiOH– гидроксид лития, ![]() - гидроксид железа ( ІІ ),
- гидроксид железа ( ІІ ), ![]() - гидроксид железа ( ІІІ ).
- гидроксид железа ( ІІІ ).
Но основные свойства имеют не только гидроксиды металлов, а также и некоторые другие вещества, которые к гидроксидам отнести нельзя, например, NH3 , BF3 . Кроме того многие химические процессы могут протекать не в водной среде, а в среде неводных растворителей ( бензол, пиридин ), к которым теория электролитической диссоциации не применима вообще. Кислоты и основания могут реагировать между собой, не будучи диссоциированными на ионы. Так, безводный хлороводород, состоящий только из молекул, легко реагирует с безводными основаниями. Эти факты показали необходимость создания теории кислот и оснований, которая бы могла объяснить наведенные выше факты.
Доказательство того, что протон не существует в свободном состоянии, сделал необходимым пересмотр понятия « кислота », а также нужно было установить роль растворителя в растворе.
В 1923 году появились две новые теории кислот и оснований: датского физикохимика Дж. Бренстеда, дополненная английским химиком Лаури и Г. Льюиса.
Теория Бренстеда получила название протонной. Теория называется протонной потому, что главная роль в определении понятий кислота и основание отведена в ней простейшей химической частице Н+ - катиону водорода в виде свободного протона.
В соответствии с протонной теорией:
Кислота – это вещество, водородсодержащие частицы которого (молекулы или ионы) способны отдавать свои протоны.
Основание – это вещество, частицы которого (молекулы, ионы) способны принимать протоны от кислот.
Таким образом, кислота – это донор протонов: ![]() , а основание – это акцептор протонов:
, а основание – это акцептор протонов: ![]() , где НА – общая формула кислоты, В – общая формула основания.
, где НА – общая формула кислоты, В – общая формула основания.
Кислота и основание, связанные из – за обмена протоном, называются сопряженной кислотно – основной парой. Кислотные свойства некоторого вещества проявляются лишь в присутствии акцептора протонов, а основные свойства – в присутствии донора протона. Вещества, которые могут отдавать или принимать протоны, объединяют одним понятием – протолиты. Во время взаимодействия любой кислоты с основанием, согласно Дж. Бренстеда [ 8, ст. 51 - 55 ], будет наблюдаться протолитическая реакция, для которой характерно состояние протолитического равновесия. Это равновесие, согласно с законами термодинамики, всегда будет смещаться в сторону получения более слабых протолитов.
Протолиты, которые в одних условиях могут отдавать свои протоны, а в других – принимать протоны, называют амфолитами. Таким образом амфолиты могут одновременно быть донорами и акцепторами протонов.
В соответствии с протонной теорией вода является по отношению к самой себе амфолитом:
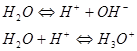
что объясняет протекание автопротолиза воды: ![]() . Автопротолиз воды количественно характеризуется ионным произведением воды:
. Автопротолиз воды количественно характеризуется ионным произведением воды: ![]() при 25°С. Значение К невелико и указывает на малую степень протекания автопротолиза воды.
при 25°С. Значение К невелико и указывает на малую степень протекания автопротолиза воды.
Протолиты в водном растворе подвержены протолизу в различной степени. В связи с этим различают сильные и слабые протолиты (аналогично сильные и слабым окислителям и восстановителям в водном растворе).
Сильные протолиты (кислоты, основания) подвергаются протолизу в большей степени.
Слабые протолиты (кислоты, основания) подвергаются протолизу в малой степени.
Установление абсолютной силы протолитов по их сродству к протону в принципе возможно, однако практически трудно осуществимо и требует сложной измерительной техники. Практически достаточно знать относительную силу протолитов ( по отношению к некоторому эталону ). Для водных растворов протолитов таким эталоном кислотности и основности является растворитель – вода.
Мерой относительной силы протолитов в водном растворе служит величина рКк . В соответствии с определением рКк :
· слабая кислота является тем более сильным протолитом, чем ниже значение рКк соответствующей сопряженной пары;
· слабое основание является тем более сильным протолитом, чем выше значение рКк соответствующей сопряженной пары.
А13+ • Н2 О + Н2 О = А1ОН2+ + Н3 О-
Слабыми основаниями по Бренстеду будут все анионы, сопряженные со слабыми кислотами и не содержащие собственных протонов:
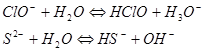
Многие гидроанионы, такие как ![]() ,
, ![]() ,
, ![]() ,
, ![]() в водном растворе являются амфолитами. Их протолиз протекает в малой степени и состоит из двух реакций, в одной из которых реагент играет роль слабой кислоты, а в другой - роль основания.
в водном растворе являются амфолитами. Их протолиз протекает в малой степени и состоит из двух реакций, в одной из которых реагент играет роль слабой кислоты, а в другой - роль основания.
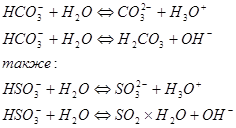
Амфолитами по отношению к воде являются также амфотерные гидроксиды, такие как Ве(ОН)2 , Zп(ОН)2 , А1(0Н)3 и Сг(ОН)3 . Они мало растворимы в воде; та их часть, которая переходит в раствор, быстро гидратируется ( условно одной молекулой воды, например А1(ОН)3×Н2О ) и вступает в две одновременно протекающие реакции протолиза ( как кислота и как основание ):
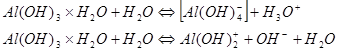
Определение кислот и оснований по Бренстеду позволяет систематизировать множество химических реакций. В первую очередь это относится к тем реакциям, которые по Аррениусу рассматриваются как нейтрализация и гидролиз солей ( 1, ст. 146 - 161 ). Реакция нейтрализация по Бренстеду обратная автопротолизу воды, а поскольку последний протекает в малой степени, то реакция нейтрализации оказывается практически необратимо проходящей до конца.