Научная работа: Радикальная сополимеризация акрилат- и метакрилатгуанидинов с виниловыми мономерами
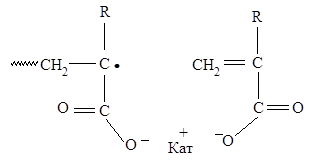
Схема 1
С ростом рН должна увеличиваться вероятность образования ионных пар на концах растущих цепей, что в рамках гипотезы должно приводить к увеличению эффективной константы скорости роста kр . Действительно, в соответствии с данными работ [15, 16], повышение концентрации ионов Na+ при данной концентрации мономера и фиксированном значении рН раствора (рН > 7) сопровождается увеличением общей скорости полимеризации [16]. (Понятие «ионная пара» используется в терминах Фуосса, т.е. предполагается непосредственный контакт сольватных оболочек противоположно заряженных ионов [20]).
Хорошо известно, что полианионы поликислот способны связывать низкомолекулярные противоионы в водных растворах [24]. Обычно сродство между противоположно заряженными низкомолекулярными ионами, например между Na+ и CH3 COO– , в не слишком концентрированных водных растворах недостаточно для стабилизации ионных пар. Образование стабильных ионных пар наблюдается лишь в менее полярных органических растворителях. Однако в случае полиэлектролитов связыванию способствует электростатическое поле всего полииона. Поэтому при высоких степенях ионизации значительная часть противоионов оказывается иммобилизованной в полимерных клубках.
Характерно, что в условиях, когда растущие цепи не ионизованы, добавление низкомолекулярных солей, как показали кинетические исследования, не влияет на скорость полимеризации акрилат- и метакрилатанионов (табл. 2) [15, 16].
Таблица 2
Кинетические эффекты, наблюдаемые при добавлении низко-молекулярных солей при радикальной полимеризации акрилат- и метакрилатанионов (60 °С)
| Акрилатанион [М]=1,2 моль/л, [ДАК] = 5´10–3 моль/л | Метакрилатанион [М] = 0,92 моль/л, [ДАК] = 4,85´10–4 моль/л | |||||
| рН* | Низкомолеку-лярная соль | V×105 , моль/л×сек | рН* | Низкомоле-кулярная соль | V×105 , моль/л×сек |
[h]** |
| 8,0 | – | 1,9 | 9,5 | – | 0,20 | 0,62 |
| 8,0 | [NaCl]=2 моль/л | 7,5 | 9.5 | [КCl] = 0,9 моль/л | 1,61 | 1,4 |
* рН установлен добавлением NaOH; ** в 0,02 N водном растворе NaOH.
Для получения прямой информации о влиянии рН и ионной силы раствора на константы скоростей элементарных стадий процесса, в работе [15] было проведено детальное кинетическое исследование фотополимеризации метакрилат- и акрилатанионов в водных растворах, рН которых устанавливали добавлением NaOH. Результаты проведеных исследований и измерений представлены в табл. 3 и 4.
Таблица 3
Константы скоростей элементарных реакций при полимеризации крилатаниона
| рН |
V´106 моль/л с |
Vин´109 моль/л с | kp/k01/2, л1/2/моль1/2сек1/2 |
k0´10–8, моль/л с |
kр, моль/л с |
| 7,9 | 5,1 | 9,1 | 0,04 | 2,6 | 650 |
| 7,9* | 25,0 | 9,1 | 0,20 | 2,6 | 3100 |
| 11,0 | 51,0 | 9,1 | 0,40 | 2,7 | 6600 |
| 13,6 | 21,0 | 9,1 | 0,17 | 2,8 | 2500 |
[М] = 1,2 моль/л; [ДАК] = 8,3´10-4 моль/л; 23 °С.
*) 1,5 н р-р NaCl в воде
Таблица 4
Константы скоростей элементарных реакций при
полимеризации метакрилатаниона
| рН |
V´106, моль/л с |
Vин´109, моль/л с | kp/k01/2, л1/2/моль1/2сек1/2 |
k0´10–8 л/моль с |
К-во Просмотров: 268
Бесплатно скачать Научная работа: Радикальная сополимеризация акрилат- и метакрилатгуанидинов с виниловыми мономерами
|