Реферат: Бериллий и сплавы, содержащие бериллий. Свойства, применение в химической технологии
Удельная прочность и жесткость материалов
| Материал | σв, МПа | γ, (кг/м3) ∙10–3 | σв /(γg), км | E /(γg), км |
| Магниевый сплав МА10 | 430 | 1,8 | 24 | 2,3 |
| Алюминиевый сплав В95 | 700 | 2,9 | 21 | 2,4 |
| Титановый сплав ВТ6 | 1500 | 4,5 | 22 | 2,6 |
| Сталь 03Н18К9М5Т | 1750 | 7,8 | 23 | 2,6 |
| Бериллий | 680 | 1,8 | 38 | 16,1 |
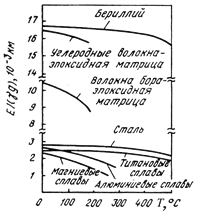
Влияние температуры на удельный модуль упругости различных материалов
Свойства Ве зависят от качества и структуры металла и заметно меняются с температурой, механические – от чистоты металла, величины зерна и текстуры, определяемой характером обработки. Обработка давлением приводит к определённой ориентации кристаллов Ве, возникает анизотропия, становится возможным значительное улучшение свойств. Механические свойства в направлении, перпендикулярном вытяжке, почти не меняются. Ве – хрупкий металл (особенно литой) при комнатной температуре, что является главным препятствием к его широкому использованию в качестве конструкционного материала; к еще большей хрупкости материала приводит содержание даже незначительных примесей (например, введение в очищенный Ве всего 0,001% Si). Имеет низкую пластичность и хорошую коррозионную стойкость. Упругость паров Ве при температуре плавления очень мала.
Механические свойства Ве в литом и деформированном состояниях различаются в зависимости от направления проведения испытаний. Наилучшими механическими свойствами обладает Ве после тёплой обработки давлением, которая проводится при температурах ниже температуры рекристаллизации. Температура рекристаллизации Ве изменяется в пределах от 700 °С до 900 °С в зависимости от степени деформации и времени выдержки. Рекристаллизационный отжиг значительно повышает пластичность и уменьшает прочность Ве.
Отношение прочности к плотности у Be значительно выше, чем у авиационных сталей и сплавов на основе Ti и Al.
Важным специфическим свойством Ве является его высокая проницаемость для рентгеновских лучей, которая в 17 раз выше, чем у алюминия.
Высокие ядерные характеристики – самое низкое среди металлов эффективное поперечное сечение захвата тепловых нейтронов и самое высокое поперечное сечение их рассеяния.
Дает эвтектические сплавы с Al и Si. Растворимость примесных элементов в Ве чрезвычайно мала.
Химические свойства
Степени окисления +2 и +1 (последняя крайне неустойчива), конфигурация внешних электронов 2s2 .
По химическим свойствам Be подобен Al. Сходство между этими элементами привело к существенному заблуждению относительно валентности и атомной массы Ве – долгое время Ве считали трехвалентным с относительной атомной массой 14 (что примерно равно утроенной массе одного эквивалента Ве 3 × 4,7); лишь через 70 лет после открытия Ве русский ученый Д.И. Менделеев пришел к выводу, что в его периодической таблице места для такого элемента нет, а вот двухвалентный элемент с относительной атомной массой 9 (приблизительно равной удвоенной массе одного эквивалента Ве 2 × 4,7) легко размещается между Li и B.
Металлический Ве относительно мало реакционноспособен при комнатной температуре (например, устойчив к кислороду воздуха благодаря плёнке окиси, образующейся на его поверхности), в данных условиях взаимодействует с F2 . В компактном виде не реагирует с водой и водяным паром даже при температуре красного каления и не окисляется воздухом до 600° С. При 1200 °С металлический Ве горит, превращаясь в белый порошок ВеО. Галогены реагируют с Ве при температуре выше 600° С, а халькогены требуют еще более высокой температуры. Компактный Ве интенсивно реагирует с N2 при температурах более 1000 градусов, а в порошкообразном состоянии – при температурах более 500о С. Аммиак взаимодействует с Ве при температуре выше 1200° С с образованием нитрида Be3 N2 , а углерод дает карбид Ве2 С при 1700° С. С Н2 Ве непосредственно не реагирует, и гидрид ВеН2 получают косвенным путем (получен при разложении бериллийорганических соединений, устойчив до 240 °С).
Ве легко растворяется в разбавленных водных растворах кислот (соляной, серной, азотной, плавиковой), слабо реагирует с концентрированной серной и разбавленной азотной кислотами, однако холодная концентрированная азотная кислота пассивирует металл. Реакция Ве с водными растворами щелочей сопровождается выделением Н2 и образованием гидроксобериллатов:
Be + 2NaOH( р ) + 2H2 O = Na2 [Be(OH)4 ] + H2
При проведении реакции с расплавом щелочи при 400–500° С образуются диоксобериллаты:
Be + 2NaOH(ж) = Na2 BeO2 + H2
Металлический Ве быстро растворяется в водном растворе NH4 HF2 . Эта реакция имеет технологическое значение для получения безводного BeF2 и очистки Ве: Be + 2NH4 HF2 = (NH4 )2 [BeF4 ] + H2
Мелкодисперсный порошок Ве сгорает в парах S, Se, Te. Расплавленный Be взаимодействует с большинством окислов, нитридов, сульфидов и карбидов.
Соединения бериллия
У Ве, в отличие от других элементов 2 группы, нет соединений с преимущественно ионными связями, в то же время для него известны многочисленные координационные соединения, а также металлоорганические соединения, в которых часто образуются многоцентровые связи.
Вследствие малого размера атома Ве почти всегда проявляет координационное число 4, что важно для аналитической химии.
Соли Ве сильно гигроскопичны и за небольшим исключением (фосфат, карбонат) хорошо растворимы в воде, быстро гидролизуются с образованием ряда гидроксокомплексов неопределенной структуры, среда раствора кислая. Осаждение начинается при отношении OH– :Be2+ > 1. Дальнейшее добавление щелочи приводит к растворению осадка.
Гидрид Ве ВеН2 был впервые получен в 1951 восстановлением ВеCl2 с помощью LiAlH4 . Аморфное белое вещество, при нагревании до 250° С гидрид ВеН2 выделять Н2 . Это соединение умеренно устойчиво в воздухе и воде, но быстро разлагается кислотами. ВеН2 полимеризован за счет трехцентровых связей ВеНВе.
BeHal : Безводные BeHalнельзя получить реакциями в водных растворах вследствие образования гидратов, таких как [Be(H2 O)4 ] F2 , и гидролиза. Лучшим способом для получения BeF2 является термическое разложение (NH4 )2 [BeF4 ], а BeCl2 удобно получать из оксида – для этого действуют Cl2 на смесь BeO и СО2 при 650–1000° С. BeCl2 можно также синтезировать прямым высокотемпературным хлорированием металлического Ве или его карбида. Эти же реакции используются для получения безводных бромида и иодида.
BeF 2 – стекловидный материал, его структура состоит из неупорядоченной сетки из атомов Ве (КЧ 4), связанных мостиками из атомов F, и похожа на структуру кварцевого стекла. Выше 270° С BeF2 самопроизвольно кристаллизуется. Подобно кварцу, он существует в низкотемпературной α-форме, которая при 227° С переходит в β-форму, кроме того, можно получить формы кристобалита и тридимита. Структурное сходство между BeF2 и SiO2 распространяется также на фторобериллаты (которые образуются при взаимодействии BeF2 с фторидами щелочных элементов и аммония) и силикаты.
BeF2 – компонент фторобериллатных стекол и солевой смеси, используемой в ядерных реакторах на расплавленных солях.
Хлорид и другие галогениды Ве можно рассматривать как полиядерные комплексные соединения, в которых координационное число Ве равно 4. В кристаллах BeCl2 есть бесконечные цепочки с мостиковыми атомами Cl: