Реферат: Энтропия органических веществ при нормальных и повышенных давлениях
258,65
62,55
258,72
0,03
500
274,01
75,44
274,12
0,04
600
288,78
86,27
288,86
0,03
Прогнозирование энтропий органических соединений при повышенных давлениях
При прогнозировании энтропий веществ при повышенных давлениях широко используется подход, аналогичный рассмотренному выше для энтальпий образования (разд. 1) и основанный на принципе соответственных состояний и разложении Питцера для энтропии:
 (2.11)
(2.11)
и таблицах Ли-Кеслера (табл. 2.7, 2.8) для энтропии.
В уравнении (2.11) - ацентрический фактор;  - поправка к энтропии на давление, характеризующая поведение простого вещества;
- поправка к энтропии на давление, характеризующая поведение простого вещества;  - функция отклонения в поведении рассматриваемого вещества от поведения простого вещества;
- функция отклонения в поведении рассматриваемого вещества от поведения простого вещества; ![]() - идеально-газовая энтропия вещества при рассматриваемой температуре,
- идеально-газовая энтропия вещества при рассматриваемой температуре, ![]() - искомая энтропия, R - газовая постоянная, равная 8,31441 Дж/(моль×К) или 1,98725 кал/(моль×К);
- искомая энтропия, R - газовая постоянная, равная 8,31441 Дж/(моль×К) или 1,98725 кал/(моль×К); ![]() - стандартное давление (1 атм, 101325 Па и пр.),
- стандартное давление (1 атм, 101325 Па и пр.), ![]() - интересующее давление, для которого производится расчет энтропии, выраженное в тех же единицах, что и стандартное давление.
- интересующее давление, для которого производится расчет энтропии, выраженное в тех же единицах, что и стандартное давление.
Таблицы Ли-Кеслера, как и для энтальпий (разд. 1), составлены на основе достаточно универсального уравнения состояния вещества (уравнение Бенедикта-Уэбба-Рубина) с соблюдением общепринятых принципов, т.е. между любыми соседними значениями в столбцах или строках таблицы корректной является линейная интерполяция. В таблицах область, лежащая выше ломаной линии, принадлежит жидкому состоянию вещества.
Расчет ![]() иллюстрируется примером 2.5.
иллюстрируется примером 2.5.
Пример 2.5
Рассчитать ![]() окиси этилена при давлении, изменяющемся от 0,71 до 142 атм., и при температурах 304,85, 422,10, 492,45 и 562,80 К.
окиси этилена при давлении, изменяющемся от 0,71 до 142 атм., и при температурах 304,85, 422,10, 492,45 и 562,80 К.
Изотермические изменения энтропии, рассчитанные по уравнению
Значения для простого вещества 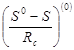
|
Tr |
Pr | ||||||
|
0,010 |
0,050 |
К-во Просмотров: 1210
Бесплатно скачать Реферат: Энтропия органических веществ при нормальных и повышенных давлениях
| |||||