Статья: Белки
Начнем с белков. Белки состоят из мономеров – аминокислот. Каждая аминокислота имеет аминогруппу, связанную с атомом углерода, с этим же атомом связана карбоксильная группа, водород и аминокислотный остаток. Такая конфигурация присутствует во всех аминокислотах. Аминогруппа может быть присоединена к первому за карбоксильной группой атому углерода, или ко второму атому и т.д. Атомы нумеруются греческими буквами, и в зависимости от того, к какому по порядку атому присоединена аминокислота, ее называют альфа-аминокислота, или бета-аминокислота и т.д. В состав белков входят только альфа-аминокислоты.
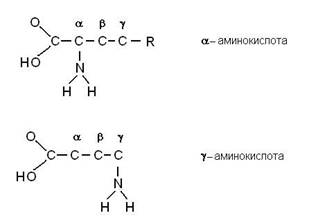
Напомним, что карбоксильная группа имеет кислотный характер, она диссоциирует на ионы в водном растворе с образованием протона и отрицательно заряженной группы СОО¯, а NH2–группа имеет основной характер, она способна присоединять протон водорода, становясь положительно заряженной. В молекуле аминокислоты протон от карбоксильной группы может переносится на аминогруппу – такие образования называются цвиттер-ионы. В растворе аминокислоты находятся в виде цвиттер-ионов.
Существенно, что молекулы аминокислот могут отличаться в своей пространственной конфигурации. Это явление называется стереизомерией. Эти молекулы называются D- изомерами и L- изомерами. Молекулы являются зеркальным отображением друг друга, и иначе, чем через четвертое измерение они одна в другую перейти не могут. На плоскости тот атом, который находится ближе, перед плоскостью, изображается треугольной стрелкой, тот, что дальше, за плоскостью – пунктирной линией.
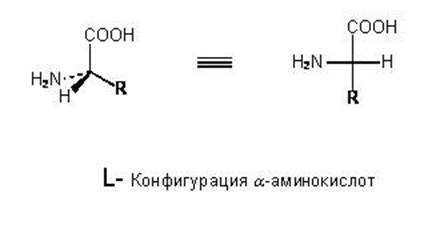
В живом организме все аминокислоты – L–изомеры. D-изомеры встречаются довольно редко и имеют определенные функции, например, могут входить в состав антибиотиков.
Всего живая клетка использует 20 аминокислот. Они отличаются строением боковой цепи, как видно из рисунка, могут быть разветвленные цепи, они могут содержать ароматические кольца. Например, у пролина второй углеродный атом израсходовал все свободные связи на ароматическую группу, и поэтому он не обладает такой подвижностью относительно группы С-С, и поэтому в белках, где есть пролин, вращение полипептидной цепи в этих участках ограниченно.
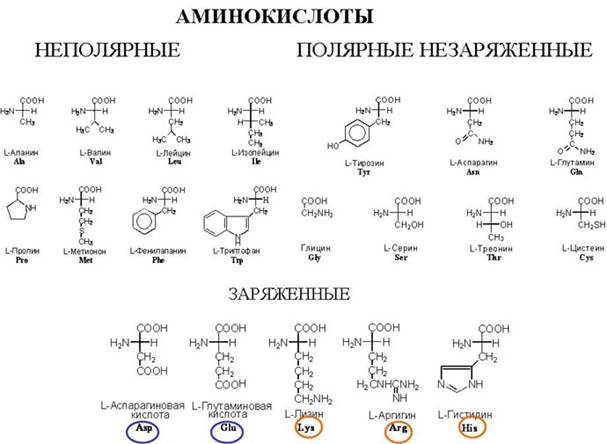
Аминокислоты делят на неполярные, то есть не имеющие заряда и не имеющие групп, которые можно было бы ионизировать, полярные не заряженные и пять кислот относятся к заряженным: это 2 кислоты, которые содержат вторую карбоксильную группу, которая может ионизироваться и нести на себе отрицательный заряд, и три аминокислоты имеющие дополнительные аминогруппы, которые несут в растворах с собой положительный заряд и используются в белках для того, чтобы зарядить необходимые части молекулы. Изменение заряда белковой молекулы может оказать большое влияние на структуру и функцию.
Последовательность аминокислот в белке составляет его первичную структуру.
Как же они соединяются? Аминокислоты способны взаимодействовать друг с другом, образуя пептидную связь. При этом молекула воды уходит, а углерод соединяется с азотом – собственно пептидная связь. Понятно, что следующая карбоксильная группа может прореагировать с аминогруппой другой кислоты и таким образом образуется полипептидная цепочка, что и называется первичной структурой белка. При записи первичной структуры аминокислоты обозначают либо трехбуквенным кодом, по первым трем буквам названия, либо используют однобуквенный код. В базах данных первичная структура белка записывается обычно однобуквенным кодом.
В зависимости от того, какие аминокислоты образовали цепочку, он может свернуться в пространстве и принять ту или иную пространственную структуру, которая называется вторичной структурой белка. Полипептидная цепочка сворачивается в пространстве в различные структуры, например спираль с определенными характеристиками, с определенным шагом (α-спираль), или вытянутую структуру (β-структура). β– спирали могут взаимодействовать между собой, образуя целые белковые листы. α- спирали образуют достаточно жесткие цилиндрические структуры. На рисунках альфа-спирали изображаются или как спиральные ленты или как цилиндры, а бета-структуру изображаются как плоские полосы.
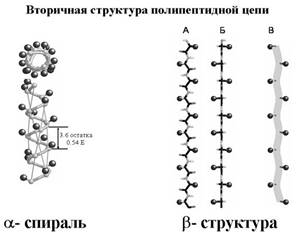
Что же заставляет белки сворачиваться? В формировании вторичной структуры принимают участие гидрофобные взаимодействия, ионные взаимодействия, водородные связи и ковалентные связи.
Гидрофобные взаимодействия. Как уже было сказано выше, существуют полярные и неполярные аминокислоты. Если в полипептидной цепи рядом находятся гидрофобные аминокислоты (неполярные), то в водном растворе нерастворимые в воде гидрофобные участки постараются уйти от взаимодействия с водой, свернуться так, чтобы оказаться рядом и укрыться от воды, образовать структуру с минимальной потенциальной энергией. Если рядом находятся заряженные аминокислотные остатки, то они будут притягиваться в случае разноименных зарядов или отталкиваться в случае одноименных зарядов. Поэтому первичная структура белка, то есть, наличие гидрофобных или заряженных участков на полипептидной цепи, определяет то, как этот белок свернется. Или, если, к примеру, имеется пролин, то он будет держать соседние атомы под определенным углом, определяя тем самым их положение в пространстве.
Расположение элементов вторичной структуры (альфа-спиралей и других элементов) в пространстве относительно друг друга называется третичной структурой белка.
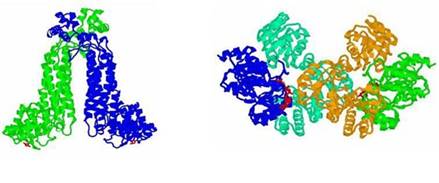
Но, кроме того, что сам белок при попадании в водный раствор примет ту конформацию, в которой он должен работать, в клетке еще есть белки, которые называются шапероны (от слова shape - форма), которые помогают другим белкам правильно сворачиваться. Если белки сворачиваются неправильно, то это может иметь катастрофические последствия. Несколько лет назад в Европе была эпидемия коровьего бешенства, и большое количество коров пришлось уничтожить. Коровье бешенство (губчатая энцефалопатия – мозг животного становится похож на губку) вызывается не вирусом и не бактерией, а особым клеточным агентом – неправильно свернутым белком. Этот белок приводит к образованию в клетке конгломератов, то есть, белки буквально выпадают в осадок, и жизнь клетки нарушается, прежде всего влияя на нервную систему. Это происходит потому, что белки, которые в норме в клетке взаимодействовали бы с этим белком, не могут этого сделать, так как он свернут неправильно, и поэтому клетка начинает неправильно функционировать. Таким образом, это болезнь неправильно свернутых белков. Эта эпидемия разразилась после того, как стали применять новую технологию переработки костной муки. При более низких температурах белки из костей больных животных, которые после переработки шли в качестве добавки к корму, перестали уничтожаться, а стали попадать в корм, вызвав тем самым эпидемию. Каким же образом неправильно свернутые белки попадают из пищеварительного тракта в мозг? Оказывается, что клеточные механизмы (ферменты протеазы), которые уничтожают отработанные белки, этот белок «угрызть» не могут. И прионные белки, не меняясь, могут очень долго сохраняться в организме. К тому же, некоторые белки устойчивы к воздействию температур.
У людей есть аналог этой болезни. Это инфекционное заболевание называется куру. Оно описано у народов, имеющих привычку съедать мозги умерших предков (из уважения к последним). В них как раз и находились инфекционные белки. Это так называемая медленная инфекция (белок ведь, в отличие от вируса, не размножается, а постепенно высаживает на себя другие клеточные белки, распространяя вокруг себя плохую «привычку» неправильно сворачиваться). Есть схожая болезнь у овец скрейпи (характер такой же, просто дело в другом белке). И еще есть наследственное заболевание, которое называется синдром Крейтцфельда-Якоба. В одном из белков, который функционирует в мозгах, происходит мутация. В других клетках этот белок также есть, но просто, в первую очередь, нарушения сказываются на нервные ткани, так как они эволюционно самые молодые, и поэтому наиболее чувствительны к любым нарушениям в функционировании клетки. Эта мутация не позволяет белку правильно свернуться, и поэтому у человека развиваются все те же симптомы, что и при коровьем бешенстве у животных.
Сейчас по первичной структуре белка можно предсказать многие элементы его вторичной структуры, то есть как белок свернется. Когда были разработаны алгоритмы такого предсказания, устраивались соревнования, кто лучше предскажет структуру белка. Например структура была известна по данным кристаллографии, но ее никому не показывали, и группы ученых , используя свои алгоритмы, смотрели, чей алгоритм будет лучше.
На рисунке представлена первичная структура белка аполипопротеина Е, он занимается транспортом холестерина, это человеческий белок. На рисунке однобуквенным кодом записана последовательность аминокислот (первичная структура).
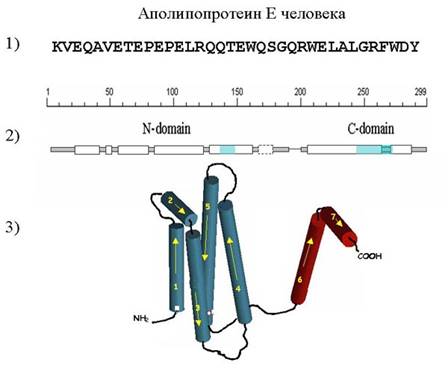
Под первичной структурой представлена вторичная структура белка, альфа-спиральные участки обозначены прямоугольниками. Над ними указаны номера аминокислот (белок состоит из 299 аминокислот). Пунктиром обозначен участок, которые во время функционирования белка то расплетается, то опять сворачивается.
Ниже показана третичная структура белка, то есть то, как спирали расположены в пространстве и взаимодействуют друг с другом. У белка есть N – конец, это та часть на которой находится аминогруппа. Та сторона, на которой находится карбоксильная группа, называется соответственно С-конец.
Есть мутация в этом белке, которая меняет заряд одной аминокислоты. В результате меняются ионные взаимодействия внутри молекулы белка. Это меняет сродство белка к липидам разных классов. В результате повышается вероятность развития старческого слабоумия, называемого болезнью Альцгеймера. На этом примере, хорошо видно, как изменение одной единственной аминокислоты может повлиять на функции белка.
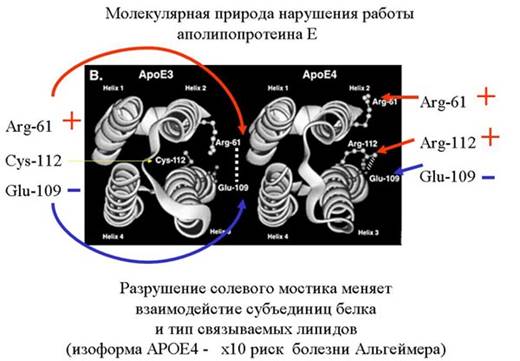
На рисунке показано, как свернут белок. Arg-61, положительно заряженный, взаимодействует с отрицательно заряженной глутаминовой кислотой. Тут образуется своеобразный мостик. Слева на рисунке представлен белок, который отличается одной мутацией от белка, изображенного справа. В нем происходит одна аминокислотная замена. Вместо нейтрального, незаряженного цистеина появляется положительно заряженный аргинин (Arg-112), с которым начинает взаимодействовать с отрицательно заряженной глутаминовой кислотой (Glu-109), так как он расположен к глутаминовой кислоте ближе, чем аргинин-61. Исчезает солевой мостик. Меняются взаимодействия внутри белка. Это приводит к тому, что меняет сродство к липидам. Его функция заключается в переносе липидов. И он, вместо липопротеинов более высокой плотности, начинает иметь большее сродство полипротеинами меньшей плотности. У людей с такой мутацией более высокий уровень холестерина и выше уровень риска развития старческого слабоумия. Кстати, помимо физической нагрузки, профилактикой развития старческого слабоумия является умственная работа. Примерно 15% европейцев имеют такую мутацию, у бушменов же это число достигает 40% . Но им этот белок ничуть не мешает, а старческого слабоумия у них не бывает вообще, так как у них низко холестериновая диета и много физических нагрузок. Им этот белок даже полезен, так как холестерин им нужно запасать. У людей же с западной «диетой» большое содержание жиров, и «жадный» вариант белка, дающий высокий уровень холестерина, становиться вредным. Холестерин нужен, но его не должно быть ни слишком много, ни слишком мало. Таким образом, проявление изменений в первичной структуре белка зависит от образа жизни.