Дипломная работа: Разработка энергосберегающих технологий процесса ректификации продуктов синтеза хлорбензола
-
- в дифенилоксид и фенилфенолы
15
-
--
-другие продукты
11
-
-
Гидролизом хлорбензола при 400—420 ºС без давления в присутствии фосфатов кальция и меди получают фенол (по Рашигу):
С6 Н5 С1 + Н2 О —> С6 Н5 ОН + НС1 (3.1.2.)
Формально образующийся НС1 может быть использован повторно для получения хлорбензола окислительным хлорированием бензола.
Недостатки метода — большая энергоемкость процесса, а также необходимость применять специальное коррозионно-устойчивое оборудование. В прошлом метод Рашига преобладал среди промышленных методов получения фенола, например в США. В дальнейшем метод потерял конкурентоспособность в связи с появлением эффективного способа получения фенола из кумола через стадию образования гидропероксида кумола. Переработка хлорбензола в фенол в целом утратила свое значение, и тем более потерял практическую ценность некаталитический щелочной гидролиз хлорбензола (400 °С, давление более 30 МПа) или гидролиз его в присутствии меди, как катализатора:
C6 H5 Cl + 2NaOH —> C6 H5 ONa + NaCl +H2 O (3.1.3.)
При нитровании хлорбензола нагреванием с азотной кислотой образуется смесь о- и n -изомеров:
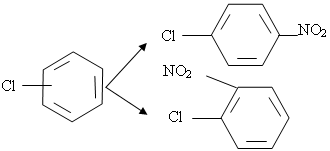
При обработке хлорбензола эквивалентным количеством HNO3 выход о-изомера снижается. Процесс ведут при 60—80 °С и отношении реактантов HNO3 : С6 Н5 С1= (0,2—0,8) : 1 (мол.), концентрация HNO3![]() 95%.
95%.
Хлорнитробензолы восстанавливают в хлоранилины — важнейшие промежуточные соединения для синтеза эффективных пестицидов.
Селективность процесса 96%. Хлоранилины превращают вначале в арилизоцианаты действием фосгена,а образующиеся, арилизоцианаты конденсируют со спиртами и аминами.
В присутствии олеума хлорбензол конденсируется с хлоралем, образуя известный инсектицид дихлордифенилтрихлорме-тилметан (ДДТ). Длительное его использование привело к появлению резистентных штаммов насекомых. Обладая высокой персистентностью в растениях и организмах животных, он способен накапливаться в тканях, в связи с чем частично или полностью запрещен к применению. Его аналоги, не содержащие хлор в бензольном ядре, а также аналоги несимметричного строения не имеют указанных отрицательных свойств и используются в быту и в сельском хозяйстве.
При относительно невысокой температуре (200—250 °С) в присутствии меди (или ее солей) хлорбензол взаимодействует с фенолом, образуя дифенилоксид:
С6 Н5 С1 + С6 Н5 ОН —> (С6 Н5 )2 О + НСl (3.1.4.)
Дифениловый эфир является термостойким теплоносителем.
3.2. Дихлорбензолы
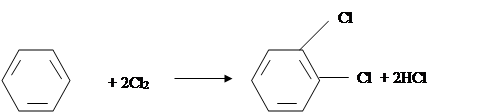 Единственным практически значимым методом получения о-дихлорбензола можно считать прямое хлорирование бензола или хлорбензола
Единственным практически значимым методом получения о-дихлорбензола можно считать прямое хлорирование бензола или хлорбензола
(3.2.1.)
Принципиальная схема производства 1,2- и 1,4- дихлорбензолов.
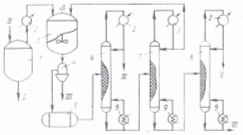
Рис. 3.2.1. Принципиальная схема производства 1,2- и 1,4-дихлорбензолов:
1 — перегонный куб; 2 — холодильник; 3 — кристаллизатор;