Доклад: Сероводород
 Информация общего характера.
Информация общего характера.
Молекула Н2 S имеет структуру равнобедренного треугольника с атомом серы в центре [d(HS) = 133 пм, угол HSH = 92°]. Сероводород представляет собой бесцветный и весьма ядовитый газ, уже 1 часть которого на 100 000 частей воздуха обнаруживается по его характерному запаху (тухлых яиц).
В жидком состоянии Н2 S проводит электрический ток несравненно хуже, чем вода, так как собственная его электролитическая диссоциация ничтожно мала: [SH3 + ] [HS- ] = 3·10-33 . Жидкий, сероводород имеет низкую диэлектрическую проницаемость (e = 6 при 0 °С) и как растворитель похож скорее на органические жидкости, чем на воду. Так, он практически не растворяет лед. Твердый Н2 S имеет строение плотной упаковки с 12 ближайшими соседями у каждой молекулы (т. е. совершенно иное, чем лед). Теплота плавления сероводорода равна 2,5 кДж/моль, а теплота испарения 18,8 кДж/моль.
tпл -85,54 °С, tкип -60,35 °С; при 0 °С сжижается под давлением 1 МПа. Восстановитель.
Химические свойства.
Сероводород взаимодействует с основаниями:
H2 S + 2NaOH = Na2 S + 2H2 O
H2 S проявляет очень сильные восстановительные свойства:
H2 S-2 + Br2 = S0 + 2HBr
H2 S-2 + 2FeCl3 = 2FeCl2 + S0 + 2HCl
H2 S-2 + 4Cl2 + 4H2 O = H2 S+6O4 + 8HCl
3H2 S-2 + 8HNO3 (конц) = 3H2 S+6O4 + 8NO + 4H2 O
H2 S-2 + H2 S+6O4 (конц) = S0 + S+4O2 + 2H2 O
(при нагревании реакция идет по - иному:
H2 S-2 + 3H2 S+6O4 (конц) =-t° = 4S+4O2 + 4H2 O)
Серебро при контакте с сероводородом чернеет:
4Ag + 2H2 S + O2 = 2Ag2 S + 2H2 O
Качественная реакция на сероводород и растворимые сульфиды - образование темно-коричневого (почти черного) осадка PbS:
H2 S + Pb(NO3 )2 = PbS(осадок) + 2HNO3
Na2 S + Pb(NO3 )2 = PbS(осадок) + 2NaNO3
Pb2+ + S2- = PbS(осадок)
Один объём воды растворяет в обычных условиях около 3 объемов сероводорода (с образованием приблизительно 0,1 М раствора (сероводородной воды)). При нагревании растворимость понижается. Подожженный на воздухе сероводород сгорает по одному из следующих уравнений:
2 Н2 S + 3 O2 = 2 H2 O + 2 SO2 + 1125 кДж (при избытке кислорода)2 Н2 S + O2 = 2 H2 O + 2 S + 531 кДж (при недостатке кислорода).
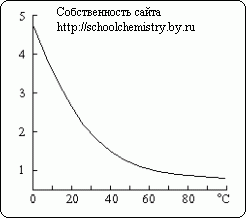
Растворимость сероводорода (объемы на 1 объём воды).
Легко окисляется сероводород и в растворе: при стоянии на воздухе сероводородная вода постепенно мутнеет вследствие выделения серы (по второй из приведенных выше реакций). Бром и йод восстанавливаются до НВr и HI. Аналогично действует он и на многие другие вещества. Сероводород является, таким образом, сильным восстановителем.
В водном растворе Н2 S ведёт себя как весьма слабая кислота. Средние соли (с анионом S2- ) называются сульфидами, кислые (с анионом HS- ) - гидросульфидами. Несмотря на бесцветность самих ионов S2- и HS- , многие соли сероводорода окрашены в характерные цвета. Подавляющее большинство сульфидов практически нерастворимо в воде. А большая часть гидросульфидов хорошо растворима (но известна лишь в растворе).
Охлаждение насыщенного водного раствора сероводорода может быть получен кристаллогидрат Н2 S·6Н2 О. Растворимость Н2 S в органических растворителях значительно выше, чем в воде. Например, один объем спирта поглощает при обычной температуре 7 объемов сероводорода. Растворимость его в расплавленной сере резко возрастает выше 130 °С и достигает максимума около 350 °С. По-видимому, это связано с образованием полисульфидов. В водном растворе сероводород легко окисляется иодом до свободной серы:I2 + Н2 S = 2 НI + S.Напротив, в газовой фазе сера окисляет иодистый водород до свободного иода:S +2 НI = Н2 S + I2 + 6 кДж.Ниже -50 °С может существовать молекулярное соединение состава Н2 S·I2 . Сероводородная кислота характеризуется константами диссоциации К1 = ([H+ ] * [HS- ]) / [H2 S] = 1·10-7 и К2 = ([H+ ] * [S2- ]) / [HS- ] = 1·10-14 , т. е. она несколько слабее угольной. Децинормальный раствор Н2 S имеет рН = 4,1.Получение.
С водородом сера в обычных условиях не соединяется. Лишь при нагревании протекает обратимая реакция:
Н2 + S = Н2 S + 21 кДж
равновесие которой около 350 °С смещено вправо, а при повышении температуры смещается влево. Практически сероводород получают обычно действием разбавленных кислот на сульфид железа:
--> ЧИТАТЬ ПОЛНОСТЬЮ <--