Контрольная работа: Адсорбция поверхностно-активных веществ (ПАВ)
Контрольная работа
по биологии
2009
Содержание
1. Влияние природы ПАВ и поверхности твердого тела на адсорбцию ПАВ
2. Моделирование поверхности и методы определения адсорбции
2.1 Дисперсные системы
2.2 Макроскопические поверхности
3. Анализ адсорбции ПАВ на основе уравнения Ленгмюра
1. Влияние природы ПАВ и поверхности твердого тела на адсорбцию ПАВ
Адсорбция ПАВ на поверхности твердых тел имеет важное значение для многих промышленных процессов, например при диспергировании твердых тел в водных средах, в моющем действии, при солюбилизации различных химических веществ и др. Многие такие процессы связаны с диспергированием твердых тел в воде. Показателен расчет, из которого следует, что в одном литре краски на водной основе площадь поверхности равна - 15000 м и эта площадь доступна для адсорбции поверхностно-активных веществ. Таким образом, адсорбция ПАВ в подобных системах является важнейшей характеристикой, определяющей их свойства.
Адсорбция ПАВ зависит главным образом от двух факторов: от взаимодействия ПАВ с поверхностью и от гидрофобное ПАВ, обеспечивающей так называемый гидрофобный эффект. Этот эффект, безусловно, тесно связан со структурой молекул ПАВ и, следовательно, с растворимостью ПАВ в воде. Было установлено, что этот эффект является главной движущей силой адсорбции ПАВ в большинстве случаев. Например, взаимодействие ПАВ с поверхностью играет небольшую роль, если эти поверхности гидрофобны, поскольку молекулы ПАВ адсорбируются на гидрофобных поверхностях за счет образования контактов гидрофобных участков молекул с поверхностью, а гидрофильные групп остаются в контакте с раствором. Такая картина аналогична образованию мицелл: при адсорбции гидрофобные участки молекул переносятся из водного окружения в гидрофобное. И действительно, свободная энергия адсорбции ПАВ на гидрофобных поверхностях очень близка к свободной энергии ми-целлообразования соответствующего ПАВ.
В то же время на сильно полярной поверхности и при низкой концентрации ПАВ его молекулы адсорбируются, ориентируясь полярными группами к поверхности. При повышении концентрации ПАВ на поверхности могут возникнуть структуры двух типов. При сильном притяжении между полярной группой ПАВ и поверхностью образуется монослой, в котором "головки" молекул ПАВ контактируют с поверхностью, а гидрофобные части молекул оказываются в контакте с раствором. Такая структура адсорбционного слоя создает гид рофобную поверхность, которая, в свою очередь, вызывает дальнейшую адсорбцию ПАВ по типу, характерному для гидрофобных поверхностей, что приводит к формированию на поверхности бислоев молекул ПАВ. Такая ситуация реализуется, например, при адсорбции заряженных ПАВ на противоположно заряженных поверхностях. Кроме того, гидрофобный монослой ПАВ на поверхности может возникнуть и в результате химической реакции между полярной группой ПАВ и поверхностью. В качестве примера можно привести адсорбцию анионных алкилксантогенатов на поверхности сульфидных минералов, что широко используется для флотации этих минералов.
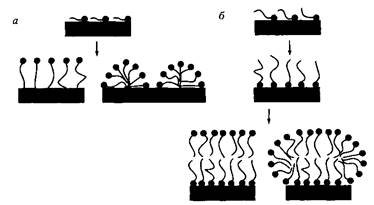
Рис.1. Поверхностно-активные вещества адсорбируются на неполярных поверхностях с образованием гидрофобных контактов с поверхностью, а на полярных поверхностях с образованием контактов полярных групп ПАВ с поверхностью
В том случае, если адсорбция происходит при высоких концентрациях, а между полярными группами ПАВ и поверхностью наблюдается притяжение умеренной силы, на поверхности возникают мицеллы или другие агрегаты ПАВ из-за гораздо более сильного притяжения между гидрофобными частями молекул. Образование агрегатов на поверхности контролируется балансом взаимодействий полярных групп с поверхностью и гидрофобных радикалов ПАВ друг с другом.
Поскольку критический параметр упаковки отражает как раз баланс взаимодействий между гидрофобными частями молекул и их полярными группами, КПУ регулирует и адсорбцию ПАВ независимо от степени гидрофильности или гидрофобности поверхности. Адсорбция, как правило, увеличивается при увеличении КПУ, так как при этом молекулы ПАВ упаковываются на поверхности более плотно и с большим выигрышем в энергии.
Обычно ПАВ в водных растворах используются в условиях, соответствующих низким значениям КПУ.
При определенных условиях это значение КПУ можно увеличить, а следовательно, повысить адсорбцию ПАВ. Ниже перечислены способы, которыми можно добиться увеличения КПУ в системах, где присутствует одно ионное ПАВ с неразветвленным гидрофобным радикалом:
1) Заменить ПАВ на другое ПАВ с более длинным углеводородным остатком.
2) Заменить ПАВ на другое ПАВ с разветвленным углеводородным остатком.
3) Использовать ПАВ с двумя углеводородными цепями.
4) Добавить в систему длинноцепочечный спирт, амин или другие гидрофобные дифильные компоненты.
5) Добавить в систему гидрофобное неионное ПАВ.
6) Ввести в систему небольшое количество противоположно заряженного ПАВ.
7) Добавить в систему соль.
Пункт 1 - это известное правило Траубе, которое утверждает, что адсорбция органических веществ из водных растворов сильно и закономерно возрастает в гомологическом ряду.
Увеличить КПУ в системе, содержащей одно неионное ПАВ с неразветвленным углеводородным радикалом, можно с помощью следующих приемов:
1) Заменить ПАВ на другое, с более длинным углеводородным остатком.
2) Заменить ПАВ на другое ПАВ с разветвленным углеводородным отстатком.
--> ЧИТАТЬ ПОЛНОСТЬЮ <--