Контрольная работа: Производство глинозема
3) при Na2 O: R2 O3 <1 образуются два типа твердых растворов: Na2 O·Al2 O3 – Na2 O·Fe2 O3 и β·Al2 O3 – β ·Fe2 O3 или Na2 O·11(Al, Fe)2 O3 ;
Невыгодно добавлять в шихту соды сверх одного моля на моль Al2 O3 + Fe2 O3 , так как избыток соды образует при обжиге с силикатом кальция соединения, которые очень медленно разлагаются в воде и щелочах, что вызывает повышенные потери щелочи.
Взаимодействие между Na 2 CO 3 , Al 2 O 3 , Fe 2 O 3 и SiO 2
Эта система отражает основные превращения, протекающие при спекании малокремнистого боксита с содой. Высокое извлечение Al2 O3 и Na2 O из спеков при такой системе возможно лишь для бокситов с небольшим содержанием кремнезема, которые выгоднее перерабатывать по способу Байера. Но иногда выгодно небольшую долю таких бокситов перерабатывать спеканием (параллельная схема сочетания способов для термической каустификации соды.
Такая бокситовая шихта называется двухкомпонентной (боксит+сода).
При рассмотрении условий спекания смеси Na2 CO3 , Al2 O3 и SiO2 указывалось, что спеки состоят в основном из алюмината и алюмосиликата натрия.
При добавлении Fe2 O3 в спеке появляется феррит натрия в количестве, определяемом молярным отношением Na2 CO3 к Al2 O3 + Fe2 O3 . Если соды достаточно для полного связывания Al2 O3 и Fe2 O3 , вся окись железа превращается в феррит натрия получается в спеке лишь столько, сколько соды осталось от связывания SiO2 и Al2 O3 .
При выщелачивании спека феррит натрия разлагается, освобождая каустическую щелочь, которая повышает стойкость алюминатных растворов. Поэтому соду обычно вводят на полное связывание Al2 O3 и Fe2 O3 .
Таким образом спекание смеси Na2 CO3 , Al2 O3 , Fe2 O3 и SiO2 дает спек, состоящий из алюмината, алюмосиликата и феррита натрия. При этих условиях зависимость между выходом Al2 O3 (![]() %) и процентным содержанием кремнезема (S) и глинозема (a) в боксите выражается следующим равенством:
%) и процентным содержанием кремнезема (S) и глинозема (a) в боксите выражается следующим равенством:
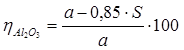
Если состав шихты выражен в молях:
![]()
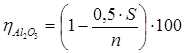
где S и n – количество молей SiO2 и Na2 O на 1 моль Al2 O3 в боксите.
Образованием твердых растворов между алюмосиликатом и ферритом натрия могут объясняться повышенные потери щелочи против стехиометрии на образование алюмосиликате натрия при выщелачивании спека из содобокситовой шихты.
Полное извлечение Al2 O3 и Na2 O возможно, когда в шихте с=2S, т.е. когда на каждый моль SiO2 в шихту вводится 2 моля СаО и на 1 моль Al2 O3 приходится 1 моль Na2 O.
Насыщенной шихтой называется такая, когда весь кремнезем связывается в двухкальцевый силикат, а вся окись алюминия и вся окись железа – соответственно в алюминат и феррит натрия, т.е. в ней соблюдаются следующие молярные соотношения: СаО:SiO2 =2,0; Na2 O:Al2 O3 =1,0; Na2 O:Fe2 O3 =1,0.
При спекании руд с умеренным содержанием Fe2 O3 и SiO2 насыщенная шихта обеспечивает практически полное извлечение Al2 O3 и Na2 O, и называется нормальной. Кроме того при нормальной шихте наблюдается широкая площадка спекообразования, что облегчает обжиг, уменьшая опасность образования кольцевых настылей. При насыщенной шихте образуется самый простой состав спека.
Химические реакции при спекании ненасыщенных шихт ещё недостаточно изучены, а состав спеков более сложены, часть глинозема в них находится не только в составе алюмината натрия, но и в составе соединений, из которых Al2 O3 не извлекается при выщелачивании. Поэтому выход Al2 O3 из спеков такой шихты меньше, чем из спеков насыщенной.
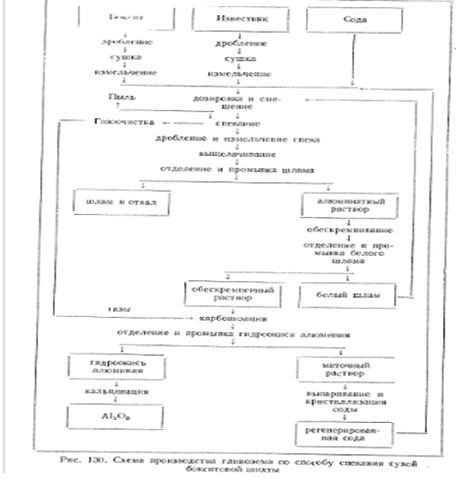
Физико-химические свойства спеков
Алюминатные спеки имеют сложный химический и фазовый состав, который определяется в основном шихтовкой исходных компонентов и режимом процесса спекания. Основным составляющими спеков являются β-2СаО·SiO2 и щелочные алюминаты состава Na2 O·Al2 O3 и K2 O·Al2 O3 , а при переработке сырья с высоким содержанием железа – еще и щелочные ферриты состава Na2 O·Fe2 O3 . Наряду с этим в спеках могут присутствовать в небольших количествах титанат натрия Na2 O·TiO2 , алюминаты кальция, геленит анортит – CaO·Hl2 O·2SiO2 , феррит кальция и другие соединения типа: mNa2 O·pCaO·nSiO2 ; mNa2 O·nFe2 O3 ·pSiO2 .
При оптимально выбранных соотношениях исходных компонентов в шихте и оптимальных режимах спекания в алюминатных спеках в основном присутствуют алюминат натрия (Na2 O·Al2 O3 ) и (β-2СаО·SiO2 ), которые образуют изотропную фазу. Щелочные алюминаты, находящиеся в изотропной фазе, растворяются в воде и щелочных растворах.
В настоящее время считается, что основные фазы присутствуют в спека в самостоятельном виде, а двухкальциевый силикат с алюминатом натрия и алюминат натрия с ферритом натрия частично могут образовывать между собой твердые растворы.
Физические свойства спека обусловлены, в основном, гранулометрическим составом шихты и режимом ее спекания, а также режимом охлаждения спека.
Как правило, алюминатные спеки представляют собой пористые частицы шарообразной формы с относительно равномерным распределением фаз по всему объему. Насыпная масса и пористость спеков сильно зависят от температурного режима спекания.
Гранулометрический состав спеков определяется условиями его получения и степенью дробления перед выщелачиванием. Гранулометрический состав, общая пористость и плотность определяют насыпную массу спека: с увеличением пористости и крупности спека насыпная масса уменьшается.
Важнейшей характеристикой спека является его пористость. За меру общей пористости спека принимается процентное отношение объема пор к общему объему спека. Для бокситовых спеков это отношение составляет обычно 10-20%. Выщелачивание спеков ведут водой, щелочными или алюминатными растворами, которые могут содержать карбонат натрия. При этом происходит растворение алюмината натрия (калия), гидролиз ферритов и смешанных алюмоферритов с переходом в расвор едкого натра (калия), а также разложение части двухкальциевого силиката в результате взаимодействия его со щелочью или карбонатом натрия.
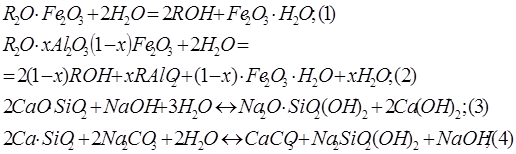
В результате растворения алюмината натрия и протекания реакций происходит извлечение ценных компонентов (глинозема и щелочи) в раствор.
Степень извлечения этих составляющих спека зависит от многих факторов: химического состава и физических свойств спека, режима выщелачивания, аппаратурной схемы выщелачивания и др.
В результате реакции (3) и (4) кремнезем переходит в раствор, и образуются гидроокись и карбонат кальция. Эти соединения вступают во взаимодействие с алюминатом натрия, образуя малорастворимые гидроалюмосиликаты натрия (ГаСН) и кальция (гидрогранаты), которые являются источником потерь глинозема и щелочи (потери в результате протекания вторичных реакций):
![]()

В зависимости от условий выщелачивания образуются гидрогранаты, у которых число SiO2 молей на моль Al2 O3 колеблется от 0,1 до 1.
Установлено, что основная доля потерь глинозема при выщелачивании крупнодробленых спеков связана с образованием гидрогранатов.