Контрольная работа: Вычисление теплового эффекта реакций
r – радиус частицы, м;
R – универсальная газовая постоянная, 8,314 Дж/моль · К;
T – абсолютная температура, К;
число 3,14.
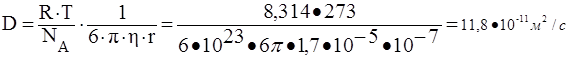
![]()
ответ на второй вопрос задания:

![]()
Таким образом, средний сдвиг частицы уменьшиться в 10 раз.
Ответ: ![]() , уменьшится в 10 раз.
, уменьшится в 10 раз.
80. Адсорбция ионов на твердой поверхности. Понятие об ионитах. Обратимая ионообменная адсорбция – основа ионообменной хроматографии.
Физические процессы молекулярной адсорбции на твердой поверхности описываются уравнениями Ленгмюра и Фрейндлиха.
Уравнение Ленгмюра:
![]() ,
,
где Г – величина адсорбции, кмоль/кг или кмоль/м2 ;
Гmax – величина предельной адсорбции, кмоль/кг (кмоль/м2 );
С – концентрация раствора, кмоль/л;
а – константа равновесия адсорбции.
Это уравнение хорошо описывает адсорбцию для малых и больших концентраций растворов (или давлений газа).
Эмпирическое уравнение Фрейндлиха:
![]() ,
,
где Г – величина адсорбции, кмоль/кг (кмоль/м2 );
n – количество вещества-адсорбтива, кмоль;
m – масса адсорбента, кг;
К – константа (при С = 1 моль/л К = Г);
1/а – константа (адсорбционный показатель); зависит от природы адсорбента и температуры. 1/а = 0,1–1.
Адсорбционная хроматография основана на различии сорбируемости разделяемых веществ адсорбентом (твёрдое тело с развитой поверхностью); распределительная хроматография — на разной растворимости компонентов смеси в неподвижной фазе (высококипящая жидкость, нанесённая на твёрдый макропористый носитель) и элюенте (следует иметь в виду, что при распределительном механизме разделения на перемещение зон компонентов частичное влияние оказывает и адсорбционное взаимодействие анализируемых компонентов с твёрдым сорбентом).
Ионообменная хроматография основана на различии констант ионообменного равновесия между неподвижной фазой (ионитом) и компонентами разделяемой смеси.
Если на поверхности адсорбента уже адсобирован электролит, то при контакте этого адсорбента с другим электролитом почти всегда в той или иной степени происходит ионообменная адсорбция. Она наблюдается на поверхности с достаточно выраженным двойным электрическим слоем. Подвижные противоионы электрического слоя способны обмениваться на другие ионы того же знака, находящиеся в растворе.