Курсовая работа: Азотная кислота
Каталитическое окисление аммиака – многостадийный гетерогенно-каталитический процесс, протекающий во внешнедиффузионной области и лимитируемый диффузией аммиака к поверхности катализатора. Ряд гипотез относительно механизма окисления аммиака на платиноидных катализаторах сводится к предположениям об образовании в процессе окисления NH3 нестойких промежуточных соединений, которые в результате распада и перегруппировки дают оксид азота(II) и элементный азот.
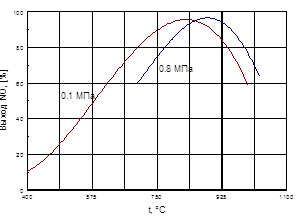
Скорость каталитического окисления аммиака по реакции (1) очень высока. За десятитысячные доли секунды степень превращения аммиака в оксид азота (II) достигает 97–98% при атмосферном давлении и 95–96% под давлением до 0,88–0,98 МПа. Однако выход оксида азота(II) может быть различным на одном и том же катализаторе в зависимости от выбранных технологических параметров - температуры, давления, линейной скорости газа, содержания аммиака в аммиачно-воздушной смеси, напряженности катализатора, числа сеток и некоторых других факторов.
 |
|
Большое значение имеет температура зажигания катализатора, которая зависит от состава катализатора и в меньшей степени от состава аммиачно-воздушной смеси. На платине реакция окисления аммиака начинается при 195 °С. Особенностью окисления является то, что сначала происходит так называемое мягкое окисление аммиака до молекулярного азота. Заметное количество оксида азота(II) начинает появляться при 300 °С. С ростом температуры выход оксида азота(II) растет, достигая максимального значения 96% на чистой платине и 99% на сплавах Pt–Pd–Rh. Проведение процесса при высоких температурах помимо увеличения выхода оксида азота(II) имеет и другие преимущества: растет скорость реакции окисления аммиака и уменьшается время контактирования. Так, при повышении температуры с 650 до 900 °С время контактирования сокращается с 5·10-4 до 1,1·10-4 c. Но при повышении температуры увеличиваются потери дорогостоящей платины, т.е. ухудшаются экономические показатели процесса. Для экономичного проведения окисления аммиака рекомендуются следующие условия:
| Давление, Мпа | 0.1 | 0.304–0.51 | 0.71–1.011 |
| Температура, °С | 780–800 | 850–870 | 880–920 |
Повышение температуры с 780 до 850 °С, приводит к увеличению прямых потерь катализатора почти вдвое.
При выборе температуры конверсии необходимо также учитывать наличие примесей в аммиачно-воздушной смеси. Температура должна быть тем выше, чем больше примесей содержится в исходной смеси.
Влияние давления. С ростом давления наблюдается снижение выхода оксида азота(II). Поэтому проектирование и сооружение установок с использованием повышенного давления на стадии конверсии аммиака сдерживались. Вместе с тем использование высокого давления при окислении аммиака позволяет повысить производительность агрегата, уменьшить размеры аппаратов. Этот факт в связи со стремлением к увеличению единичной мощности агрегатов приобретает все большее значение. На современных крупных агрегатах производства азотной кислоты процесс окисления аммиака осуществляется под давлением 0,41– 0,73 МПа.
Основным условием получения высоких выходов NO под давлением выше атмосферного являются повышение температуры и времени контактирования (увеличение числа сеток).
?????????? ???????? ? ???????? ????????? ????? ????????? ???????? ???????? ???? ? ????????????? ????????????, ??? ? ???? ??????? ??????? ? ??????????? ????? ?????????????? ?????. ????????, ??? ????? ?????????, ??? ????????, ???????? ???????? ????, ????????????? ????????????, ????? ??????? ????? ????? ? ??? ?????? ?????? ????????? ??? ????????? ???????? ?????? NO ?????? ??????????? ? ?????? ?????????????.
Влияние концентрации аммиака. Для окисления аммиака, как уже указывалось, применяют воздух. Поэтому концентрация NH3 в аммиачно-воздушной смеси определяется в том числе содержанием кислорода в воздухе. Согласно уравнению реакции 4NH3 + 5O2 = 4NO +6H2O для полного окисления 1 моль аммиака необходимо 1.25 моль кислорода. Исходя из этого, определим максимально возможное содержание аммиака в аммиачно-воздушной смеси (объемные доли,%).
Однако при соотношении O2: NH3 = 1,25 даже при атмосферном давлении выход оксида азота(II) не превышает 60–80%. Кроме того, при содержании в смеси 14.4% NH3, пришлось бы работать в области взрывоопасных концентраций. Нижний предел взрываемости аммиачно-воздушной смеси при атмосферном давления составляет 13,8% NH3.
|
|
|
 | 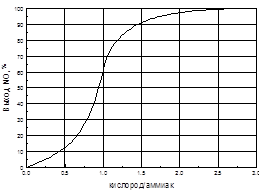 |
Таким образом, при использовании воздуха максимально возможной концентрацией аммиака в аммиачно-воздушной смеси, при которой достигается высокий выход NO, является 11,0–11,5%, и соотношение O2: NH3 = 1,7 при температурах 870 – 920 °С. На рис.3 представлена зависимость выхода NO от соотношения O2: NH3, в аммиачно-воздушной смеси. Для получения высокого выхода NO необходим примерно 30% -ный избыток кислорода сверх стехиометрического. Это связано с тем, что поверхность платинового катализатора должна быть постоянно насыщена кислородом (в отсутствие кислорода аммиак уже при 500 °С начинает разлагаться на азот и кислород).
Катализаторы. Превосходство платины по активности и селективности над всеми другими видами катализаторов было показано в 1902 г. Оствальдом. Характерно, что активность к реакции окисления аммиака проявляет подавляющее большинство металлов и их соединений, но высокий выход NO (выше 90%) обеспечивают очень немногие из них.
Обладая высокой активностью и селективностью, платина имеет низкую температуру зажигания ~200 °С, хорошую пластичность, тягучесть. Недостаток платины – ее быстрое разрушение при высоких температурах под воздействием больших скоростных потоков реагентов и катал изаторных ядов. Это приводит к потерям дорогостоящего катализатора и снижению выхода NO, что и явилось причиной поисков каталитически активных сплавов платины с другими металлами.
Проведенные промышленные испытания показали стабильную работу катализаторов из платины с добавками палладия, а также из тройного сплава Pt–Rh–Pd; это и послужило основанием для их промышленной реализации. Наибольшее распространение получили следующие катализаторы окисления аммиака (ГОСТ 3193-59):
Pt + 4% Pd + 3.5% Rh – для работы при атмосферном давлении и Pt + 7,5% Rh – при повышенном давлении.
Используемые для контактного окисления NH3 катализаторы изготавливают в виде сеток. Такая форма катализатора удобна в эксплуатации, связана с минимальными затратами металла, позволяет применять наиболее простои и удобный в эксплуатации тип контактного аппарата. В России применяются сетки из проволоки диаметром 0,09 мм (ГОСТ 3193-74), размер стороны ячейки 0,22 мм, число ячеек на 1 см длины – 32, на 1 см2 – 1024.
Платинородиевые (ГИАП-1) и платинородиевопалладиевые (сплав № 5) катализаторы весьма чувствительны к ряду примесей, которые содержатся в аммиаке и воздухе. К таким примесям относятся гидриды фосфора и мышьяка, фтор и его соединения, дихлорэтан, минеральные масла, ацетилен, диоксид серы, сероводород и др. Наиболее сильными ядами катализатора являются соединения серы и фтора. Примеси заметно снижают селективность катализатора, способствуют увеличению потерь платины. Для поддержания стабильной степени конверсии аммиака необходима тщательная очистка аммиачно-воздушной смеси и от механических примесей, особенно от оксидов железа и пыли железного катализатора синтеза аммиака. Пыль и оксиды железа, попадая на катализаторные сетки, засоряют их. уменьшая поверхность соприкосновения газов с поверхностью катализатора, и снижают степень окисления аммиака.
Чистоту исходных веществ в производстве азотной кислоты обеспечивают двумя путями – осуществлением дальнего забора воздуха и усовершенствованием систем очистки воздуха и аммиака.
В процессе реакции окисления аммиака поверхность платиноидных сеток сильно разрыхляется, эластичные нити сеток становятся хрупкими. При этом поверхность сетки увеличивается примерно в 30 раз Сначала это ведет к повышению каталитической активности катализатора, а затем к разрушению сеток. Практикой установлены следующие сроки работы катализаторных сеток: для работы под атмосферным давлением – до 14 мес. под давлением 0,73 МПа 8–9 мес.
Время контактирования. Реакция окисления аммиака происходит во внешнедиффузионной области, и поэтому увеличение объемной скорости оказывает положительное влияние на интенсивность процесса. С повышением, до определенного предела, объемной скорости поток газовой смеси становится более турбулентным, что увеличивает скорость диффузии исходных веществ к поверхности катализатора. Наряду с этим уменьшается время соприкосновения газовой смеси с горячими стенками аппаратов, что снижает возможность окисления аммиака до азота. С уменьшением времени контактирования выход NO увеличивается и при t = 1·10-4 с достигает максимума (рис.4). При дальнейшем росте объемной скорости (уменьшении t) возможен проскок аммиака, который за контактной зоной превращается в элементарный азот при окислении кислородом. Не исключена также возможность образования азота при взаимодействии аммиака с оксидом азота(II).
В заводских условиях в зависимости от качества катализатора и точности соблюдения заданного технологического режима достигается значительная селективность процесса, и выход оксида азота(II) составляет 98%. При оптимальных условиях проведения процесса и правильном подборе конструкционных материалов побочные реакции не имеют существенного значения.
|
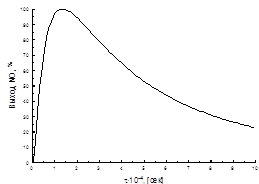 |
Окисление оксида азота (II)
Нитрозные газы, полученные при окислении аммиака, содержат оксид азота(II), азот, кислород и пары воды. При переработке нитрозных газов в азотную кислоту необходимо окислить оксид азота(II) до диоксида. Реакция окисления обратима,
2NO + O2 Û 2NO2 + 124 кДж
протекает с уменьшением объема и сопровождается выделением теплоты. Следовательно, в соответствии с принципом Ле Шателье, снижение температуры и повышение давления способствуют смещению равновесия реакции вправо, т.е. в сторону образования NO2. Ниже приведены значения константы равновесия реакции окисления для различных температур.
| t, °С | 20 | 100 | 200 | 300 | 500 | 900 |
| Kp | 1.24·1013 | 1.82·107 | 7.41·103 | 45.5 | 8.5·10-2 | 1.51·10-4 |
Из которых видно, что при температурах до 100 °С равновесие реакции практически полностью сдвинуто в сторону образования NO2. При более высокой температуре равновесие смещается в левую сторону и при температуре выше 700 °С образования диоксида азота практически не происходит. В связи с этим в горячих нитрозных газах, выходящих из контактного аппарата, NO2 отсутствует, и для его получения газовую смесь необходимо охладить до температуры ниже 100 °С.
![]()
Как видно из уравнения для константы равновесия при повышении парциального давления кислорода парциальное давление оксида азота(IV) также увеличится так как от общего давления константа равновесия зависит очень мало.
Окисление оксида азота(II) – самая медленная стадия производства азотной кислоты. Скорость реакции окисления, определяющую скорость всего процесса, можно выразить следующим образом:
![]()