Курсовая работа: Изучение процесса восстановления серебра в водных растворах
2. Колориметр фотоэлектрический Analyticjena;
3. рН – метр марки 150М;
4. Электрическая плитка «Фея-2»;
5. Микроволновая печь LGMS – 1724U.
2.2 Методы исследования
2.2.1 Получение наночастиц серебра
К раствору нитрата серебра определенной концентрации добавляли раствор восстановителя (глюкозы, аскорбиновой кислоты, боргидрида натрия, фарм.препарата «Аскорбиновая кислота с глюкозой»). Соотношение объемов 1:1. Приготовленные растворы подвергали нагреванию на плитке (t=96-98С) в течение 120мин и СВЧ облучению в микроволновой печи в течение 10 минут (режим – max).
После синтеза гидрозоли серебра исследовались электронно-микроскопическим методом, а также визуально отмечалось изменение окраски растворов и/или образования осадка. Спектры поглощения Ag-гидрозоля регистрировали при комнатной температуре в области 300-700 нм на спектрофотометре Analiticjena (кювета (Q) – 1см).
2.2.2 Приготовление раствора на основе фармацевтического препарата «Аскорбиновая кислота с глюкозой»
Состав фармацевтического препарата: аскорбиновая кислота = 0,100г; глюкоза (декстроза) = 0,877г; крахмал = 0,023г. Расчет вели на 100мл раствора приготовленного на основе таблетки с учетом, что концентрация аскорбиновой кислоты = 0,02М. m(навески таблетки) = 3,5199г: m(аскорбиновой кислоты) = 0,3520г; m(глюкозы) = 3,0870г; m(крахмал) = 0,0896г. Таблетки растирали в фарфоровой ступке, взвешивали и растворяли в дистиллированной воде, после чего раствор фильтровали для удаления крахмала.
2.3 Обсуждение результатов
После проведенных исследований, было установлено, что эффективными восстановителями являются боргидрид натрия и глюкоза. В дальнейшем в работе использовался восстановитель глюкоза, так как он является более экологически безопасным. Также важно отметить, что визуально было отмечено различие в окраске, полученных растворов: при восстановлении боргидридом натрия раствор черного цвета, что свидетельствует о частицах серебра более крупного размера (ассоциация частиц); при восстановлении глюкозой раствор светло-коричневого(желтого) цвета, что указывает на наличие более мелких частиц серебра.
Полученные данные, а также спектры исходных растворов представлены на рисунках 2 – 5.
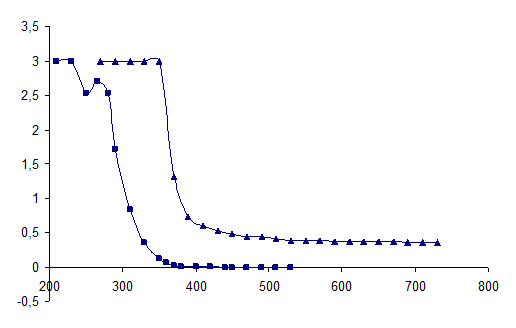
Рисунок 2 - Спектры оптического поглощения исходных растворов
(■ – аскорбиновой кислоты, ▲ – таблетки).
2.3.1 Изучение влияния концентрации AgNO3 на величину плазмонного пика
Приготовление растворов проводили в соответствии с методикой, указанной в п.2.2.1. Концентрацию растворов AgNO3 варьировали в интервале 0,0001М – 0,005М. Концентрация глюкозы была постоянна и равна 0,01М.
Полученные результаты представлены на рисунке 6.
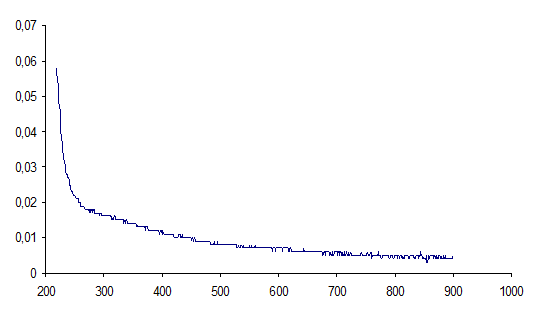
Рисунок 3 - Спектры оптического поглощения исходного раствора глюкозы
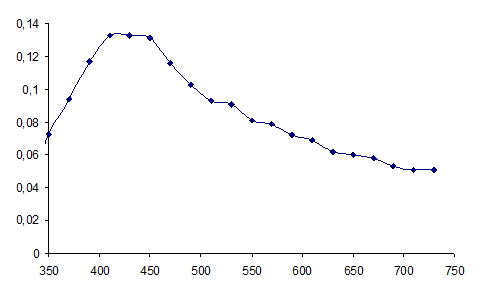
Рисунок 4 - Спектры оптического поглощения гидрозоля серебра, полученного восстановлением AgNO3 глюкозой.
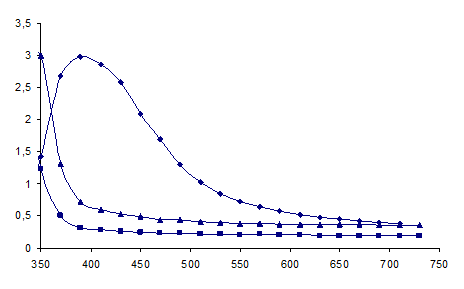
Рисунок 5 - Спектры оптического поглощения гидрозоля серебра, полученного восстановлением AgNO3 (■ – аскорбиновой кислотой, ♦ - боргидридом натрия,
▲ – таблеткой).
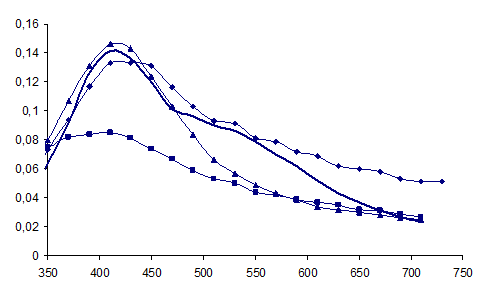
Рисунок 6 - Спектры оптического поглощения гидрозоля серебра, полученного восстановлением AgNO3 глюкозой(■ – С(AgNO3 ) = 0,0001М,
♦ - С(AgNO3 ) = 0,0005М, -- – С(AgNO3 ) = 0,001М;▲ – С(AgNO3 ) = 0,005М).