Курсовая работа: Окись этилена
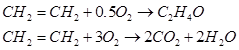
Обычно до окиси этилена окисляется не больше 55 – 60% этилена, а 40 – 45% его полностью сгорает до CО2 и Н2 О.
В промышленных установках прямого окисления используются контактные аппараты с неподвижным или с псевдоожиженным слоем катализатора.
Реактор с неподвижным слоем катализатора, работающий под давлением до 21 атм., представляет собой кожухо-трубный аппарат, трубки которого заполнены зерненным катализатором. Так как окислы железа каталитически ускоряют реакцию полного окисления этилена, трубки изготавливают из хромоникелевых аустенитных сталей или из обычных углеродистых сталей и серебрят изнутри. Благодаря малому сечению трубок реагирующие газы проходят по ним с большой скоростью. Таким образом, достигается повышенная теплоотдача от газа к стенкам трубок и сравнительно равномерное охлаждение контактной массы. Интенсивный отвод реакционного тепла в этом процессе весьма важен, так как при температуре свыше 300°С может происходить полное окисление этилена.
Окись этилена извлекают из контактных газов в скрубберах, орошаемых водой, затем отгоняют из водного раствора, осушают и конденсируют. Транспортируют окись этилена в жидком виде в стальных баллонах. Если целевым продуктом производства является этиленгликоль, контактные газы промывают горячим 1%-ным раствором серной кислоты, в результате чего окись этилена гидратируется до этиленгликоля ![]() .
.
Изучен и разработан процесс получения окиси этилена каталитическим окислением этилена в псевдоожиженном слое катализатора. Благодаря высокому коэффициенту теплоотдачи в псевдоожиженном слое катализатора (значительно большему, чем в аппаратах с неподвижным слоем катализатора) при окислении требуется меньшая поверхность теплообмена, а следовательно, и меньшие габариты реакционных аппаратов.
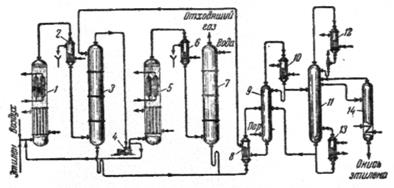
Рис. 2.2. Схема производства окиси этилена прямым окислением этилена в псевдоожиженном слое катализатора.
1) реактор первой ступени; 2, 6) холодильники; 3) абсорбер первой ступени; 4) компрессор; 5) реактор второй ступени; 7) абсорбер второй ступени; 8) теплообменник; 9) отпарная колонна; 10, 12) дефлегматоры; 11) ректификационная колонна; 13) кипятильник; 14) разделительная колонна.
В нижней части реакционного аппарата помещены трубы, охлаждаемые высокотемпературным теплоносителем, циркулирующим в межтрубном пространстве. Над трубами расположены охлаждающие элементы, а еще выше фильтры из пористой окиси алюминия. Равномерное распределение псевдоожиженного катализаторапо трубам реактора достигается благодаря тому, что аппарат заполняют катализатором до уровня, значительно превышающего высоту труб (над трубной решеткой создается слой катализатора. Равномерность подачи этилена во все трубы автоматически регулируется специальными приборами.
Для данного процесса требуется прочный катализатор, не требующий регенерации или реактивации в течение длительного времени и не подвергающийся заметному истиранию.
Процесс проводят под давлением в две ступени. Смесь этилена и воздуха нагнетается в контактный реактор 1 первой ступени, где до 50% этилена превращается в окись этилена. Продукты реакции охлаждаются в холодильнике 2 , после чего в абсорбере 3 первой ступени из них извлекается окись этилена.
Часть непрореагировавших газов возвращают в реактор 1 , а остальной газ подают в реактор 5 второй ступени. Общая степень превращения этилена во второй ступени окисления составляет 70%.
Из контактных газов после второй ступени окисления окись этилена извлекают водой в абсорбере 7 второй ступени. Из абсорберов 3 и 7 водный раствор окиси этилена через теплообменник 8 направляют в отпарную колонну 9. Отгоняемая из этой колонны паро-газовая смесь поступает через дефлегматор 10 на разделение в ректификационную колонну 11 . Окончательная очистка окиси этилена от CO2 производится в колонне 14. Получаемый по этому способу продукт представляет собой 99,5%-ную окись этилена.
При прямом окислении расход этилена несколько выше, чем при хлоргидринном методе. Однако этот недостаток вполне окупается другими достоинствами метода прямого окисления, который следует считать весьма перспективным.
2.3. Гомогенное газофазное окисление этилена в окись этилена
При прямом гомогенном окислении этилена кислородом образуется ряд ценных продуктов: окись этилена, формальдегид, органические кислоты. сейчас разрабатываются методы синтеза окиси этилена гомогенным окислением этилена в газовой фазе, так как для этого процесса не требуется затрат ни дорогого катализатора, ни хлора. Кроме того, при этом способе получения окиси этилена не требуются этилен и воздух такой высокой степени очистки, как при каталитическом окислении этилена. К недостаткам этого метода относятся многообразие образующихся продуктов и низкая селективность, что объясняется цепной природой происходящих превращений и высокой температурой. Однако развитие теории цепных процессов открывает новые пути совершенствования реакций газофазного окисления этилена.
Рассмотрим влияние условий на процесс образования окиси этилена. Первым фактором мы рассмотрим влияние температуры.
При температуре ниже 300°С этилен не взаимодействует с кислородом, медленное окисление начинается при 300°С![]() . С повышением температуры скорость процесса резко возрастает. Оптимальной температурой считают ту, при которой 65% поданного в зону реакции кислорода вступает во взаимодействие с этиленом.
. С повышением температуры скорость процесса резко возрастает. Оптимальной температурой считают ту, при которой 65% поданного в зону реакции кислорода вступает во взаимодействие с этиленом.
При температуре ниже 400°С степень превращения кислорода за один проход составляет примерно 35%. При температуре выше 550°С резко возрастает скорость окисления этилена до двуокиси углерода и воды, а скорость образования окиси этилена уменьшается.

Рис. 2.3. Влияние температуры на глубину окисления этилена.
На рис. 2.3 представлена температурная зависимость степени превращения исходных компонентов при прямом окислении этилена. Состав исходной смеси – 80% С2 Н4 и 12% О, время реакции 20 сек; стеклянный реактор длиной ~500 мм и диаметром 46 мм. Из рассмотрения кривых, представленных на рис. 2.3 можно сделать выводы:
1. С ростом температуры степень конверсии этилена возрастает.
2. Количество реагирующего кислорода сначала быстро растет с повышением температуры – при 360°С в реакцию вступает более 80% исходного кислорода. Выше этой температуры кривая расхода кислорода
резко изменяет свой наклон и асимптотически приближается к 100%![]() .
.
В данном процессе возможно протекание нескольких побочных реакций. В частности возможно при температурах 320 - 335ºС образование формальдегида:
![]()
Другой побочной реакцией, которая может идти в этих условиях, является образование бирадикала диметиленоксида и дальнейшее его взаимодействие с этиленом с образованием пропилена и формальдегида:
![]()
Такой процесс наблюдался при взаимодействии окиси этилена с этиленом при температурах выше 400°С. При температурах ниже 350°С образование пропилена не происходило![]() .
.
Исследования показали влияние на процессы окисления этилена добавления небольших количеств озона, который ускорял процессы окисления. Это можно считать доказательством цепного механизма окисления этилена в окись этилена![]() .
.
В наше время существуют полупромышленные установки для получения окиси этилена методом гомогенного окисления.
Схема процесса приведена на рис. 2.4. Реакционная смесь после реактора 2 поступает в холодильник 7 и далее в скруббер 9, где большая часть образующихся продуктов поглощается водой. Газовая смесь после скруббера вновь возвращается в реактор; предварительно к ней добавляют этан и кислород. Основными продуктами реакции являются окись этилена, уксусный и муравьиный альдегид, перекись водорода, окись и двуокись углерода. Оптимальный выход окиси этилена (36%) соответствует степени конверсии кислорода менее 35%.

Рис. 2.4. Схема установки для гомогенного окисления смеси этилена и этана.
1) змеевик для обогрева и охлаждения реактора, 2) реактор, 3) вентиль для подачи кислорода, 4) циркуляционный насос, 5) вентиль для подачи реакционной смеси, 6) вентиль для подачи рециркуляционного газа, 7) холодильник. 8) вентиль для отвода избыточных газов, 9) скруббер, 10) насос орошения скруббера, 11) холодильник для адсорбента, 12) вентиль для подачи адсорбента на ректификацию, 13) насос для отвода адсорбента.