Курсовая работа: Определение способности почвенных бактерий к разложению синтетических моющих средств
Характерная особенность неионогенных ПАВ – жидкое состояние и малое пенообразование в водных растворах.
Неионогенные ПАВ разделяют на группы, различающиеся строением гидрофобной части молекулы, в зависимости от того, какие вещества послужили основой получения полигликолевых эфиров. На основе спиртов получают оксиэтилированные спирты RO(C2 H4 O) nH; на основе карбоновых кислот – оксиэтилированные жирные кислоты RCOO(C2 H4 O) nH; на основе алкилфенолов и алкилнафтолов – оксиэтилированные алкилфенолы RC6 H4 O(C2 H4 O) nH; на основе аминов, амидов, имидазолинов-оксиэтилированные алкиламины RN[(C2 H4 O) nH]2 ; на основе сульфамидов и меркаптанов – ПАВ типа RSO2 NC(C2 H4 O) nH]2 и RS(C2 H4 O) nH.
Гидрофильную группу в молекуле НПАВ могут образовывать, помимо окиси этилена, и другие соединения. Так, довольно широко применяются НПАВ – сложные эфиры маннита и сорбита, которые называют соответственно маннитаты и сорбитаты или спаны. Оксиэтилированные эфиры сорбита и маннита нашли распространение под названием «твины». Хорошо известны НПАВ, в состав которых, наряду с окисью этилена, входят остатки окиси пропилена – так называемые блок-сополимеры. Токсическое действие неионогенных поверхностно-активных веществ определяется главным образом неполярной частью молекулы, при этом оно более выражено при наличии в последней ароматического кольца (Ставская, 1981).
Неионогенными ПАВ являются продукты конденсации гликозидов с жирными спиртами, карбоновыми кислотами и этиленоксидом.
Получение неионогенных ПАВ в большинстве случаев основано на реакции присоединения этиленоксида при повышенной температуре под давлением в присутствии катализаторов (0,1–0,5% CH3ONa, KOH или NaOH).
Неионогенные ПАВ менее чувствительны к солям, обусловливающим жесткость воды, чем анионактивные и катионактивные ПАВ. Смачивающая способность неионогенных ПАВ зависит от структуры; оптимальной смачивающей способностью обладает ПАВ разветвленного строения:
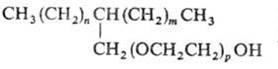
Неионогенные ПАВ хорошо совмещаются с другими ПАВ и часто включаются в рецептуры моющих средств.
Разнообразие химического строения НПАВ, создает трудности при анализе этих веществ и приводит к получению противоречивых результатов при изучении их биоразлагаемости (Ставская, 1981).
В данной работе проводились исследования микроорганизмов-деструкторов ПАВ. Используемые микроорганизмы выделялись из почвы. В качестве селективного агента использовался полиакриламид (ПАА). Полиакриламид – твердое аморфное белое или частично прозрачное вещество без запаха, растворимое в воде. Молекулярная масса составляет до 5500000. ПАА используется как флокулянт при осветлении сточных вод, коагулянт в металлургии, флотореагент, диспергатор, загуститель. Он содержится в сточных водах сульфатцеллюлозных заводов и обогатительных фабрик. В воде ПАА постепенно гидролизуется до аммониевой соли полиакриловой кислоты. Молекулярный вес полиакриламида зависит от степени гидролиза. Бывает жидкий, в виде сухих порошков и в форме эмульсии.
Химическая структура полиакриламида
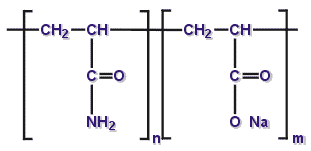
Способность ПАА к химическим превращениям с образованием различных ионных производных, разветвленных и сшитых продуктов расширяет области применения полимеров. Рассмотрим наиболее важные химические свойства ПАА (Савицкая, 1969).
ПАА легко гидролизуется в присутствии кислот и щелочей. Взаимодействует с формальдегидом в щелочной среде (рН 8–10) при 20 о С с образованием полиметилолакриламида, который применяется для аппретирования тканей (пропитка или обработка поверхности с целью придания несминаемости и жесткости), обезвоживания осадков сточных вод и обогащения железных руд.
При обработке ПАА формальдегидом и вторичным амином в щелочной среде образуется аминометилированный полимер, который по флокулирующей способности превосходит исходный полимер.
Реакция сульфометилирования необходима для получения анионных производных ПАА при взаимодействии его с формальдегидом и бисульфитом натрия в щелочной среде (рН 13).
В составе макромолекул наряду с сульфометилированными группами могут содержаться карбоксилатные группы (вследствие щелочного гидролиза амидных групп), а также непрореагировавшие амидные группы. В этом случае получаются эффективные структурообразователи грунтов, антистатические агенты для текстильных материалов и флокулянты для различных типов суспензий (Савицкая, 1969).
Реакции сшивки ПАА применяют для получения водопоглощающих изделий, пленок, защитных покрытий и капсул для лекарств, семян, удобрений. Образование трехмерных структур возможно также при действии на ПАА кислотами (Петрянова-Соколова, 1987).
1.4 Влияние поверхностно-активных веществ на микроорганизмы
Многие синтетические поверхностно-активные вещества обладают антимикробными свойствами. (Ставская, 1981).
Кроме природной устойчивости некоторых микроорганизмов к биоцидным препаратам, микроорганизмы быстро адаптируются к неблагоприятным факторам, в том числе и к воздействию антимикробных средств. Этот феномен объясняется, в первую очередь, выживанием в условиях контакта с биоцидом наиболее устойчивых (резистентных) штаммов бактериальной популяции. В итоге, вследствие мутации, выживают клетки, имеющие измененный ген. Описаны случаи размножения потенциально патогенных микроорганизмов в растворах, предназначенных для дезинфекции, адаптации к терапевтическим дозам антибиотиков и полирезистентности к десяткам антимикробных средств.
Антимикробное действие ПАВ зависит, прежде всего, от типа соединения. Наиболее высокое бактерицидное действие проявляют катионные вещества, неионогенные – слабое, анионактивные занимают промежуточное положение.
Анионные ПАВ влияют главным образом на грамположительные бактерии (Ставская, 1981, цит. Kaminski, 1963). Антимикробный эффект АПАВ зависит от их химического строения. Чем больше атомов углерода, тем сильнее действие соединения. Активность анионных соединений усиливается при снижении рН среды (Ставская, 1981, цит. Flett, 1945).
Неионогенные вещества характеризуются более слабым антимикробным действием; некоторые из них совсем не обладают активностью. Характер влияния на микроорганизмы зависит от химического строения НПАВ. Твины не только не угнетают микроорганизмы, но даже стимулируют их рост (Ставская, 1981, цит. Stinson, 1971). В присутствии неионогенных ПАВ в значительных концентрациях не наблюдается спороношения у мицелиальных грибов, хотя и происходит их рост (Ставская, 1981, цит. Furuta 1945).
Катионные ПАВ активны по отношению к грамположительным и грамотрицательным микроорганизмам. По отношению к грибам катионные вещества наиболее активны (Ставская, 1981, цит. Furuta, 1945). В присутствии полисахаридов (агар-агара, крахмала, целлюлозы) и белковых веществ (казеина, сыворотки крови, пептона, желатины, альбумина) снижается антимикробная активность ряда катионных и амфотерных ПАВ. Причем бактериостатическое действие на грамотрицательные бактерии снижается в большей степени, чем на грамположительные, в то время как бактерицидное действие уменьшается одинаково (Ставская, 1981, цит. Koppensteiner, 1974).
Для катионных ПАВ мишенями являются карбоксильные группы аминокислот и кислых полисахаридов бактерий, а для анионных ПАВ – кетонные группы белков, аминогруппы соответствующих углеводов и липидов, а также фосфатные группы тейхоевых кислот.
В естественных условиях микробные клетки обладают общим отрицательным зарядом, поэтому наиболее широкое практическое применение нашли катионные ПАВ, которые губительно действуют на грамположительные и грамотрицательные бактерии, дрожжевые и нитчатые грибы. Но в клетке также имеются молекулы, несущие положительные заряды, поэтому и анионные ПАВ губительно действуют на микроорганизмы, но при более высоких концентрациях.
Сильное дестабилизирующее действие на мембраны клеток оказывают низкомолекулярные катионные ПАВ (цитилпиридиний хлорид, хлоргексидин, алкилди-метил бензил аммоний хлорид) (Поликарпов, 2005).
Много исследований посвящено изучению механизма антимикробного действия ПАВ. Известно, что химические вещества могут влиять на микроорганизмы специфически и неспецифически. Специфически – при очень низких концентрациях антимикробного соединения, которое может реагировать с определенными компонентами клетки, нарушая их нормальное функционирование. Неспецифическое действие на клетку обычно проявляется при достаточно высоких концентрациях веществ. Оно может быть связано с неблагоприятным для микроорганизма изменением поверхностного натяжения, рН, с установлением высокого осмотического давления и т.д. Что касается ПАВ, то до сих пор не существует единого мнения, как – специфически или неспецифически – влияют они на микроорганизмы.
Большинство исследователей предполагают, что ПАВ действуют на микроорганизмы специфически. Эту мысль подтверждает тот факт, что неионогенные ПАВ, которые понижают поверхностное натяжение, почти не обладают антимикробной активностью (Ставская, 1981).