Курсовая работа: Совершенствование лекарств и новые фармацевтические технологии
Любое исследование на человеке должно быть хорошо организовано и проводиться под контролем специалистов. Неправильно проведенные испытания признаются неэтичными. В связи с этим большое внимание уделяется планированию клинических испытаний.
Для того чтобы в работе врачей не проявлялись узкопрофессиональные интересы, которые не всегда отвечают интересам больного и общества, а также с целью обеспечения прав человека, во многих странах мира (США, Великобритания, Германия и др.) созданы специальные этические комитеты, призванные контролировать научные исследования лекарств на людях. Этический комитет создан и в Украине.
Приняты международные акты об этических аспектах проведения медицинских исследований на людях, например, Нюрнбергский кодекс (1947), в котором отражены вопросы защиты интересов человека, в частности, неприкосновенности его здоровья, а также Хельсинская декларация (1964), содержащая рекомендации для врачей по биомедицинским исследованиям на людях. Изложенные в них положения носят рекомендательный характер и в то же время не освобождают от уголовной, гражданской и моральной ответственности, предусмотренной законодательствами этих стран.
Медико-правовые основы этой системы гарантируют как безопасность и своевременное адекватное лечение больных, так и обеспечение общества наиболее эффективными и безопасными лекарствами. Только на основе официальных испытаний, методически верно спланированных, объективно оценивающих состояние больных, а также научно проанализированных экспериментальных данных можно сделать правильные выводы о свойствах новых лекарств.
Программы клинических испытаний для различных фармакоте-рапевтических групп лекарственных препаратов могут значительно отличаться. Однако имеется ряд основных положений, которые всегда отражаются в программе: четкая формулировка целей и задач испытания; определение критериев выбора для испытаний; указание методов распределения больных в испытуемую и контрольную группы; число больных в каждой группе; метод установления эффективных доз лекарственного препарата; длительность и метод проведения испытания контролируемого препарата; указание препарата сравнения и/или плацебо; методы количественной оценки действия используемого препарата (подлежащие регистрации показатели); методы статистической обработки полученных результатов (рис. 2.3).
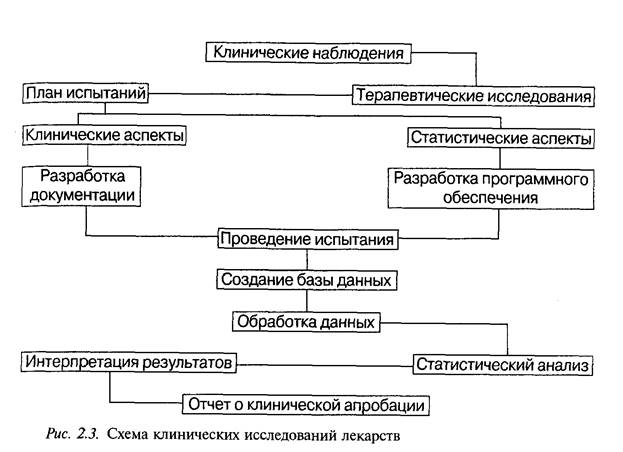
Программа клинических испытаний проходит обязательную экспертизу в комиссии по вопросам этики.
Участвующие в испытании нового препарата пациенты (добровольцы) должны получить информацию о сути и возможных последствиях испытаний, ожидаемой эффективности лекарства, степени риска, заключить договор о страховании жизни и здоровья в порядке, предусмотренном законодательством, а во время испытаний находиться под постоянным наблюдением квалифицированного персонала. В случае возникновения угрозы здоровью или жизни пациента, а также по желанию пациента или его законного представителя, руководитель клинических испытаний обязан приостановить испытания. Кроме того, клинические испытания приостанавливаются в случае отсутствия или недостаточной эффективности лекарства, а также нарушения этических норм.
Клиническая апробация генерических препаратов в Украине проводится по программе "Ограниченные клинические испытания" по установлению их биоэквивалентности.
В процессе клинических испытаний лекарства выделяют четыре взаимосвязанные фазы: 1 и 2 — дорегистрационные; 3 и 4 — пострегистрационные.
Первая фаза исследования проводятся на ограниченном числе больных (20-50 человек). Цель — установление переносимости лекарственного препарата.
Вторая фаза — на 60-300 больных при наличии основной и контрольной групп и использовании одного или нескольких препаратов сравнения (эталонов), желательно с одинаковым механизмом действия. Цель — проведение контролируемого терапевтического (пилотного) исследования препарата (определение диапазонов: доза — режим применения и, если возможно, доза — эффект) для оптимального обеспечения дальнейших испытаний. Критериями оценки обычно служат клинические, лабораторные и инструментальные показатели.
Третья фаза — на 250-1000 человек и более. Цель — установить краткосрочный и долгосрочный баланс безопасность — эффективность лекарственного препарата, определить его общую и относительную терапевтическую ценность; изучить характер встречающихся побочных реакций, факторы, изменяющие его действие (взаимодействие с другими лекарственными препаратами и др.). Испытания должны быть максимально приближенными к предполагаемым условиям использования данного лекарственного препарата.
Результаты клинического испытания заносятся в индивидуальную стандартную карту каждого больного. В конце испытания полученные результаты суммируются, обрабатываются статистически и оформляются в виде отчета (в соответствии с требованиями ГНЭЦЛС), который заканчивается аргументированными выводами.
Отчет о клинических испытаниях лекарственного препарата направляется в ГНЭЦЛС, где подвергается тщательной экспертизе. Конечным результатом экспертизы всех поступивших в ГНЭЦЛС материалов является инструкция по применению лекарственного препарата, регламентирующая его применение в клинических условиях.
Лекарственный препарат может быть рекомендован к кли?