Курсовая работа: Загальна характеристика напівпровідникових матеріалів
До складних напівпровідникових матеріалів відносять також тирит, сіліт, ферит, аморфні стекла й ін.
По ступені досконалості решітки всі кристали можна розділити на ідеальні й реальні, а по сполуці — на стехіометричні й нестехіометричні.
Ідеальні — це кристали, кожний атом яких перебуває у положенні, які характеризують мінімумом потенційної енергії, тобто упорядковано розташований як стосовно своїх найближчих сусідніх атомів, так і до атомів усього об'єму кристала. Стехіометричністю прийнято називати пропорційність масової сполуки вхідних елементів атомним масам у хімічній формулі речовини, що утворить даний, кристал. Якщо масова сполука кристалічної речовини пропорційна його хімічній формулі, кристал має стехіометрична сполука. Таким чином, ідеальні кристали по сполуці є стехіометричні.
Більшість напівпровідникових матеріалів являє собою кристалічні тверді речовини з упорядкованою періодичною структурою. При описі різних структур користуються наступними термінами:
- елементарний осередок, що представляє собою найменший об'єм кристалічної речовини у вигляді паралелепіпеда, переміщаючи який уздовж трьох незалежних напрямків, можна одержати кристал;
- постійна решітки, обумовлена як довжина елементарного осередку уздовж однієї з осей;
- кристалографічні осі, що показують напрямки кристала й визначають ребра елементарного осередку.
Розглянемо основні типи кристалічних решіток.
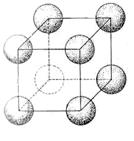
Рисунок 1 - Розташування атомів у простій кубічній решітці [1]
Проста кубічна решітка (рис. 1) складається з атомів, що лежать у вершинах куба. Типовим матеріалом з такою структурою є хлористий цезій, у решітці якого послідовно чергуються позитивні іони цезію й негативні іони хлору.
Гранецентрована кубічна решітка (рис. 2, а) більш складніша, чим проста кубічна, тому що в ній атоми розміщені не тільки у вершинах куба, але й у середині кожної грані. Типовими матеріалами з такою структурою є хлористий натрій (рис. 2, б) і алюміній.

Рисунок 2 - Розташування атомів у гранецентрованій кубічній решітці[1]: а) Загальний вид: 1-хлор; 2-натрій; б) Решітка іонного кристала хлористого натрію
Об’ємноцентрована кубічна решітка складається з атомів, розташованих у кутах і в центрі куба (але не на його гранях). Типовим матеріалом з такою структурою є залізо при нормальній температурі.
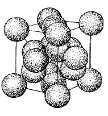
Рисунок 3 - Решітка типу алмаза [1]
Крім цих порівняно простих, структур існують більше складні, але також з кубічним елементарним осередком. Найбільш важливої з них є решітка типу алмаза (рис. 3).
Більшість напівпровідникових матеріалів після кристалізації мають решітку типу алмаза. Основну роль у цій решітці грає наявність тетраедричних зв'язків; кожний атом з'єднаний із чотирма найближчими атомами валентними зв'язками. Решітка типу алмаза являє собою модифікацію гранецентрованої кубічної решітки й складається із двох гранецентрованих решіток, зрушених відносно один одного на l /4 діагоналі осередку. У решітці цього типу ребра елементарного осередку не збігаються з напрямками валентних зв'язків[1] .
1.1 Германій
Германій Ge ставиться до IV групи періодичної системи елементів. Атомна маса 72,59. Температура плавлення 937° С. Зміст германія в земній корі невелике й становить близько 0,001%. У незначних кількостях германій утримується в цинкових рудах, вугільного пилу, золі, сажі й морській воді. Германій майже не має своїх руд. Єдина руда германія – германіт – містить набагато більше міді, заліза й цинку, чим германія. Видобуток германія – складний технологічний процес.
В твердому стані германій — типовий ковалентний кристалічний матеріал, що володіє характерним блиском. Механічна обробка германія утруднена, а на звичайних токарських, свердлильних і фрезерних верстатах взагалі неможлива, тому що це дуже твердий тендітний матеріал.
Кристалічний германій хімічно стійкий на повітрі при кімнатній температурі; при температурі вище 600° С окисляється до двоокису германія Ge02 . Вода на германій не діє, у соляній НС1, азотній HN03 кислотах германій не розчиняється. Активно розчиняють германій при кімнатній температурі царська горілка (суміш соляної й азотної кислот), розчин перекису водню, різні травники (суміші кислот). У розчинах киплячих лугів КІН і NaOH германій добре розчиняється, а в холодні мало розчинний. Додавання в розчини лугів перекису водню підвищує розчинність германія. У розплавлених лугах германій швидко розчиняється з утворенням розчинних у воді германітов. Розплавлені вуглекислий і азотнокислий натрій також швидко розчиняють германій з виділенням відповідного газу.
В напівпровідниковій технології широко використають кварцові й графітові тиглі, касети, контейнери й інші вироби.
Основними сполуками германія є двоокис, моноокис і тетрахлорид германія.
Двоокис германія Ge02 — аморфна або кристалічна речовина. Аморфну (склоподібна) модифікацію одержують швидким охолодженням розплавленого двоокису германія. У присутності каталізаторів склоподібна модифікація переходить у кристалічну тетрагональну, котра потім перетворюється в гексагональну. У більшості випадків двоокис, що утвориться в багатьох процесах, германія являє собою суміш аморфної й гексагональної модифікацій [1].
Двоокис германія розчиняється в соляний і сарною кислотах, а також у лузі.
Двоокис германія — порошок білих кольорів, використовуваний для виробництва напівпровідникового полікристалічного й монокристалічного германія, випускають трьох груп: ГД1, ГД2 і ГДЗ, які відрізняються друг від друга змістом основної речовини й домішок.
Моноокис германія Ge утворюються в результаті диспропорційності або в процесі відновлення двоокису германія. У деяких випадках вона утвориться в розчинах. Моноокис германія має аморфну структуру. У воді моноокис германія практично не розчиняється, а в сарною й соляний кислотах розчиняється повільно.