Реферат: Абсорбция газов
Абсорбция газов (лат. absorptio, от absorbeo-поглощаю), объемное поглощение газов и паров жидкостью (абсорбентом) с образованием раствора. Применение абсорбции в технике для разделения и очистки газов, выделения паров из паро-газовых смесей основано на разл. р-римости газов и паров в жидкостях. Процесс, обратный абсорбции., наз. десорбцией; его используют для выделения из р-ра поглощенного газа и регенерации абсорбента. Поглощение газов металлами (напр., водорода палладием) наз. окклюзией. асорбция .- частный случай сорбции.
Различают физ. и хим. абсорбцию. При физической абсорбции энергия взаимод. молекул газа и абсорбента в р-ре не превышает 20 кДж/моль. При химической абсорбции (или абсорбция с хим. р-цией, часто наз. хемосорбцией) молекулы растворенного газа реагируют с активным компонентом абсорбента-хемосорбентом (энергия взаимод. молекул более 25 кДж/моль) либо в р-ре происходит диссоциация или ассоциация молекул газа. Промежут. варианты абсорбции характеризуются энергией взаимод. молекул 20-30 кДж/моль. К таким процессам относится растворение с образованием водородной связи, в частности А. ацетилена диметилформамидом.
Статика абсорбции. Характеризует термодинамич. равновесие р-ра с паро-газовой смесью, а также материальный и энергетич. балансы процесса. При физ. абсорбции с образованием идеального р-ра для р-рите-ля и растворенного газа во всем интервале изменения состава в соответствии с законом Рауля растворимость газа:
![]()
где Р°2- давление паров над чистым сжиженным газом при данной т-ре системы; р2 - парциальное давление газа; звездочкой обозначаются параметры в-ва в условиях равновесия. Индексы "1" и "2" относятся соотв. к р-рителю и газу. Идеальная р-римость x*2,ид-ф-ция только т-ры, св-ва р-ри-теля влияния на нее не оказывают.
Зависимость р-римости газов х*2 от их парциального давления при физ. абсорбции в бесконечно разбавленном р-ре (х2 ->0) и при низких давлениях Р в системе описывается законом Генри (рис. 1, прямые 1-3):
![]()
где КH-коэф. Генри, изменяющийся с изменением т-ры. Если абсорбция проводят под давлением, но х*2 ->0, р-римость газа можно рассчитать по уравнению Кричевского - Казарновского:
![]()
где Кф-коэф. физ. р-римости, равный КH при х2-> 0 и Р-> -> 0; f*2-летучесть газа;![]() -парциальный мольный объем растворенного газа в жидкой фазе при бесконечном разбавлении; R- универсальная газовая постоянная; Po1-давление насыщ. паров чистого р-рителя при абс. т-ре системы Т. Если 0 < х*2
-парциальный мольный объем растворенного газа в жидкой фазе при бесконечном разбавлении; R- универсальная газовая постоянная; Po1-давление насыщ. паров чистого р-рителя при абс. т-ре системы Т. Если 0 < х*2![]() (0,05-0,1) молярной доли (разбавленные р-ры), то при низких давлениях справедливо ур-ние Сеченова:
(0,05-0,1) молярной доли (разбавленные р-ры), то при низких давлениях справедливо ур-ние Сеченова:
![]()
где А1,2-коэф., не зависящий от состава р-ра. 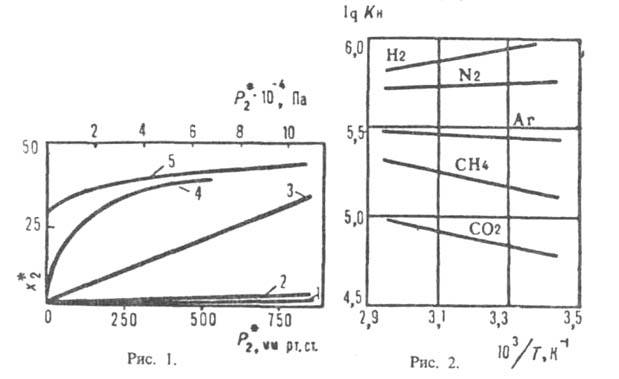
Рис. 1. Зависимость р-римости х2* нек-рых газов в жидкостях парциального давления газов над растворами: I- СО2 в воде при 20 °С; 2-СО2 в пропиленкар-бонате при 25 С; 3 С2Н4 в диметилформамиде при 25 °С; 4-СО, в водном о-ое содержащем 25% К2СО3 и 10% диэтаноламина при 60°C 5-СО, в 2,5 н водном р-ре моноэтаноламина при 20°С; х2* - в м3 газа (при нормальных условиях - 20°С и 0,1 МПа) на 1 м3 жидкости. 2
Рис. 2. Зависимость коэф. Генри (в мм рт. ст./молярные доли) для р-ров газов в додекане от т-ры.
Зависимость растворимости газа от температуры как при физ., так и при хим. абсорбции приближенно описывается ур-нием:
![]()
где![]() -тепловой эффект растворения газа. Если р-р при А. нагревается,
-тепловой эффект растворения газа. Если р-р при А. нагревается,![]() . С изменением т-ры
. С изменением т-ры![]() обычно либо остается постоянной, либо незначительно изменяется. Р-римость газа в смешанном растворителе (содержащем малополярные компоненты) можно оценить по соотношению:
обычно либо остается постоянной, либо незначительно изменяется. Р-римость газа в смешанном растворителе (содержащем малополярные компоненты) можно оценить по соотношению: 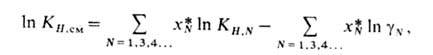
где КН.си, КН.N-коэф. Генри соотв. для газа в смеси р-рителей и для р-ров этого газа в чистых компонентах р-рителя;![]() -коэф. активности компонентов р-рителя (молярные доли
-коэф. активности компонентов р-рителя (молярные доли![]() относятся к смеси р-рителей, свободной от растворенного газа).
относятся к смеси р-рителей, свободной от растворенного газа).
Нек-рые данные о р-римости газов приведены в таблице, где газы и р-рители расположены в порядке возрастания энергетич. параметров![]() и
и![]() потенциала Леннард-Джонса. Эти параметры м. б. использованы для приближенной оценки р-римости газов при низких давлениях по ур-нию:
потенциала Леннард-Джонса. Эти параметры м. б. использованы для приближенной оценки р-римости газов при низких давлениях по ур-нию:
![]()
где![]() -р-римость в 1 м3 газа, приведенная к нормальным условиям (20 °С, 0,1 МПа) на 1 м3 абсорбента; kв- константа Больцмана; Р0, T0-соотв. давление и т-ра при нормальных условиях; Р, Г-то же при рабочих условиях. Р-римость умеренно растворимых газов в данном р-рителе возрастает линейно с увеличением
-р-римость в 1 м3 газа, приведенная к нормальным условиям (20 °С, 0,1 МПа) на 1 м3 абсорбента; kв- константа Больцмана; Р0, T0-соотв. давление и т-ра при нормальных условиях; Р, Г-то же при рабочих условиях. Р-римость умеренно растворимых газов в данном р-рителе возрастает линейно с увеличением![]()
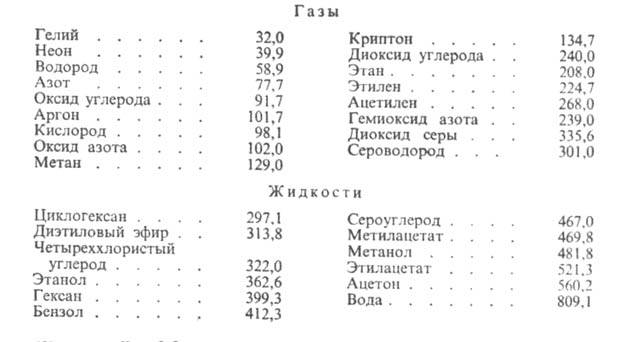
Ниже приведены значения параметров потенциала Лен-нард-Джонса![]() (в К) для газов
(в К) для газов![]() и жидкостей
и жидкостей![]() :
: 
Тепловой эффект растворения газа АЯ линейно изменяется с увеличением![]() ; соотв. р-римость плохо р-римых газов
; соотв. р-римость плохо р-римых газов![]() , в основном Не, Ne, H2, N2, CO, Аr, О2 и NO, с возрастанием т-ры увеличивается (за исключением водных р-ров), а р-римость хорошо р-римых газов
, в основном Не, Ne, H2, N2, CO, Аr, О2 и NO, с возрастанием т-ры увеличивается (за исключением водных р-ров), а р-римость хорошо р-римых газов![]() уменьшается. Типичные примеры для бесконечно разбавленных р-ров приведены на рис. 2. Р-римость таких газов, как H2S, COS, SO2, HC1, NH3, C12, обычно значительно выше, чем рассчитанная по ур-нию (1), вследствие специфич. взаимод. с молекулами р-рителя.
уменьшается. Типичные примеры для бесконечно разбавленных р-ров приведены на рис. 2. Р-римость таких газов, как H2S, COS, SO2, HC1, NH3, C12, обычно значительно выше, чем рассчитанная по ур-нию (1), вследствие специфич. взаимод. с молекулами р-рителя.
При хим. абсорбции поглотит. способность абсорбента (емкость, соответствующая предельному кол-ву газа, к-рый поглощается единицей объема абсорбента) и![]() больше, чем при физ. абсорбция. При необратимой р-ции (напр., при поглощении СО2 р-рами NaOH с образованием Na2CO3) равновесное давление газа над р-ром равно нулю, пока в р-ре есть непрореагировавший абсорбент, и поглотит. способность определяется стехиометрией р-ции. При обратимой р-ции давление газа над р-ром равно нулю, но по сравнению с физ. абсорбцией резко изменяется характер зависимости р-римости газа от давления (рис. 1, кривые 4,5). Так в простейшем случае, когда в р-ре происходит только одна р-ция и активности компонентов р-ра равны их концентрациям, имеем:
больше, чем при физ. абсорбция. При необратимой р-ции (напр., при поглощении СО2 р-рами NaOH с образованием Na2CO3) равновесное давление газа над р-ром равно нулю, пока в р-ре есть непрореагировавший абсорбент, и поглотит. способность определяется стехиометрией р-ции. При обратимой р-ции давление газа над р-ром равно нулю, но по сравнению с физ. абсорбцией резко изменяется характер зависимости р-римости газа от давления (рис. 1, кривые 4,5). Так в простейшем случае, когда в р-ре происходит только одна р-ция и активности компонентов р-ра равны их концентрациям, имеем:
![]()
где Кх = ASKфKP-константа равновесия системы газ-жидкость; Кр — константа равновесия р-ции;![]()
![]() -равновесная степень превращения абсорбента; x1- начальная концентрация абсорбента; h-число молей продуктов р-ции на 1 моль прореагировавшего газа; j-число молей абсорбента, вступивших во взаимод. с 1 молем растворенного газа; A5-коэф., зависящий от стехиометрии.
-равновесная степень превращения абсорбента; x1- начальная концентрация абсорбента; h-число молей продуктов р-ции на 1 моль прореагировавшего газа; j-число молей абсорбента, вступивших во взаимод. с 1 молем растворенного газа; A5-коэф., зависящий от стехиометрии.
Коэф. ускорения абсорбции могут быть достаточно велики. Так, в случае поглощения СО2 в насадочной колонне при одинаковых нагрузках по фазам, т-ре и давлении, используя 2 н. водный р-р КОН (15% К содержится в р-ре в виде карбоната), можно получить![]() по сравнению с физ. абсорбцией СО2 водой. Гипотетич. идеальный р-ритель, не обладающий сопротивлением переносу в жидкой фазе и имеющий бесконечно большую реакц. способность, обеспечил бы
по сравнению с физ. абсорбцией СО2 водой. Гипотетич. идеальный р-ритель, не обладающий сопротивлением переносу в жидкой фазе и имеющий бесконечно большую реакц. способность, обеспечил бы![]()
Увеличение![]() и
и![]() (иногда в неск. раз) может происходить под влиянием поверхностной конвекции, вызываемой локальными градиентами поверхностного натяжения, к-рые возникают в ряде случаев в результате массоотдачи, особенно при одноврем. протекании р-ций (напр., при абсорбции СО2 водными р-рами моноэтаноламина). Это необходимо учитывать при подборе новых хемосорбентов. Значение
(иногда в неск. раз) может происходить под влиянием поверхностной конвекции, вызываемой локальными градиентами поверхностного натяжения, к-рые возникают в ряде случаев в результате массоотдачи, особенно при одноврем. протекании р-ций (напр., при абсорбции СО2 водными р-рами моноэтаноламина). Это необходимо учитывать при подборе новых хемосорбентов. Значение![]() если р-ция приводит к возникновению поверхностной конвекции, следует определять на основе коэф. массоотдачи при физ. абсорбции, найденного в условиях воздействия на процесс конвективных микропотоков вблизи границы раздела фаз.
если р-ция приводит к возникновению поверхностной конвекции, следует определять на основе коэф. массоотдачи при физ. абсорбции, найденного в условиях воздействия на процесс конвективных микропотоков вблизи границы раздела фаз.
При расчете скорости абсорбции часто используют коэф. массо-передачи, определяемые по гипотетич. поверхностным составам и, следовательно, по гипотетич. движущим силам. Обычно принимают, что коэф. массопередачи, отнесенный к концентрации в газе, Кг [кмоль/(м2 *МПа*с)] обусловлен движущей силой (у2-у*2), где у*2-молярная доля поглощаемого компонента в газе, к-рая отвечает равновесию с жидкостью, имеющей средний объемный состав х2; у2 -средний объемный состав газа в данном сечении аппарата. Тогда получим:
--> ЧИТАТЬ ПОЛНОСТЬЮ <--