Реферат: Борорганические соединения
Борорганические соединения, содержат атом В, связанный с органическим остатком. Включают: органобораны RnBX3-n(n = 1-3); нейтральные комплексы RnX3-nB*L (и = 1-3); органобораты M[RnBX4_n] (n = 1-4); борониевые соли [R(X)BL2]Y, где Х-Н, Hal, ОН, OR', SeR', NH2, NR2, NHNHR', SO4 и т.д., М - катион металла, NH4 или др., L - эфир, амин, сульфид, фосфин и др., Y - анион. К борорганическим соединениям также относят соед., содержащие В в цикле (борацикланы), внутрикомплексные соед. и органокарбораны (см. Карбораны). Синтезированы диборные [напр., R2B—BR2, R2BNHNHBR2, C6H4(BR2)2] и полиборные соединения. Во всех этих в-вах координационное число бора 3 или 4. Наиб. изучены алкил-, ци-клоалкил-, арил-, алкенил- и аллилбораны, а также борацикланы.
В органоборанах атом В и три связанных с ним атома лежат в одной плоскости, а вакантная 2р-орбиталь перпендикулярна к ней; углы RBX близки к 120° (исключение-1-бораадамантан). Трифенил-, три(1-нафтил)-, тримезитилборан и их гомологи в твердом состоянии и в р-рах при низких т-рах имеют конформацию трехлопастного пропеллера. Производные четырехкоординированного В имеют строение правильного или искаженного тетраэдра.
Большинство органоборанов мономерны; нек-рые ассоциированы за счет межмол. координации [как, напр., в (R2BONH2)2], трехцентровых двухэлектронных [напр., в (R2BH2)2] или водородных связей.
Молекулы бороксолов (RBO)3, боразолов (RBNR')3 и сосд. типа (RBS)3 представляют собой шестичленные циклы.
Органобораны - к-ты Льюиса; с основаниями (NH3, R'M, R'OM) дают комплексные соед., напр. (C2H5)3B*NH3, и органобораты, напр. М [R3BC![]() CR'], M [R3BCN]. Комплексообразование с аминами используется для количеств. оценки стерич. напряжений.
CR'], M [R3BCN]. Комплексообразование с аминами используется для количеств. оценки стерич. напряжений.
При изучении борорганических соединений широко применяется спектроскопия ЯМР 11В, поскольку величины хим. сдвигов 11В определяются строением и числом заместителей при атоме В. Связь В—С ковалентная, слабополярная. Органобораны RBX2 не способны диссоциировать с образованием карбаннонов (в отличие от солей последних).
Длина связи В—С уменьшается в ряду В—Сsp3 > В—Csp2 > В—Сsр, а также при уменьшении координационного числа бора. Напр., длины связей В—С (нм) составляют: для (СН3)3В 0, 15783, для (CH3)2BF 0, 155, для (С6Н5)3В 0, 152, для НС![]() CBF2 0, 1513; для (CH3)3B*N(CH3)3 0, 165, для (С6Н5)4В- 0, 164-0, 169.
CBF2 0, 1513; для (CH3)3B*N(CH3)3 0, 165, для (С6Н5)4В- 0, 164-0, 169.
Энергия (Е)связи В—С в триалкилборанах (342-368 кДж/моль) близка к энергии связи С—С в алканах (355-368 кДж/моль). Связи В—Сsр2 прочнее связей В—Csp3. Напр., в (СН3)3В Е = 363 кДж/моль, в CH3BF2 400 кДж/моль, в (С6Н5)2ВВг 460 кДж/моль.
По хим. св-вам борорганические соединения отличаются от орг. соед. Li, Mg, Al и др. металлов. Так, алкил- и арилбораны не реагируют с СО2, орг. галогенидами, эпоксидами, производными карбоновых к-т и т.д. Триалкилбораны, трициклоалкилбораны и алифатич. борацикланы не расщепляются водой, спиртами, аминами, кетонами и сложными эфирами, р-рами неорг. к-т и щелочей до 100-130°С. Это позволяет проводить многие р-ции борорганических соединений в водных и спиртовых р-рах. Однако в гидридах (R2BH)2 и (RBH2)2 связи В—Н легко расщепляются водой и спиртами.
Низшие члены рядов R3B, R2BX, а также борацикланы самовоспламеняются на воздухе (по зеленому цвету пламени судят о наличии В в соед.). Четырехкоординационные соед. В, как правило, устойчивы на воздухе.
Триарилбораны с Na или его амальгамой дают ярко-окрашенные анион-радикалы![]() или
или![]() ; R2BHal(R=Alk, Ar) с К или Na-радикалы R2B, к-рые стабилизируются основаниями, напр. пиридином.
; R2BHal(R=Alk, Ar) с К или Na-радикалы R2B, к-рые стабилизируются основаниями, напр. пиридином.
Борорганические соединения легко окисляются Н2О2 в щелочной среде, СrO3, КМnО4 и др. При гидролизе или ацидолизе органоборанов![]() всегда образуются RH и
всегда образуются RH и![]() (или
(или![]() ); р-ции экзотермичны, т.к. связь В—О очень прочна.
); р-ции экзотермичны, т.к. связь В—О очень прочна.
В большинстве борорганических соединений борсодержащую группу можно заменить практически на любую функц. группу, Н, D, металл, орг. остаток и т.д., напр.:
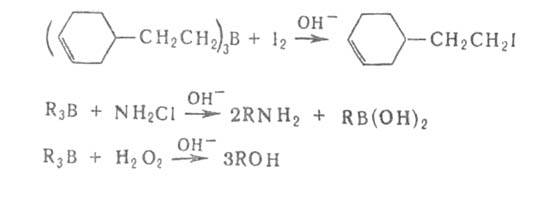
Разработаны также способы наращивания углеродной цепи при атоме бора на любое число атомов С с одновременным введением функц. группы. Органобораны электрофильны, а органобораты нуклеофильны. Первая стадия большинства р-ций органоборанов - образование комплексов типа R3B*L или боратов
Р-ции![]() борорганических соединений можно разделить на след. типы:
борорганических соединений можно разделить на след. типы:
1. Обмен функц. групп при атоме В, напр.:
![]()
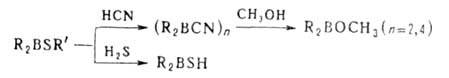
2. Электрофильное деборирование, включает протолиз, галодеборирование арилборанов, взаимод. с солями нек-рых металлов и обменные р-ции.
Протолиз борорганических соединений реагентами НХ (Н2О, ROH, RCOOH, ![]() дикетоны, R2NH и др.) широко используется для получения разл. типов борорганических соединений, защиты и определения ОН- и NH2-групп, обезвоживания кристаллогидратов, в акваметрии. Протолиз - промежут. стадия разл. р-ций, в частности "цис-гидрирования" ацетиленов, олефинов и др. непредельных соед.:
дикетоны, R2NH и др.) широко используется для получения разл. типов борорганических соединений, защиты и определения ОН- и NH2-групп, обезвоживания кристаллогидратов, в акваметрии. Протолиз - промежут. стадия разл. р-ций, в частности "цис-гидрирования" ацетиленов, олефинов и др. непредельных соед.:
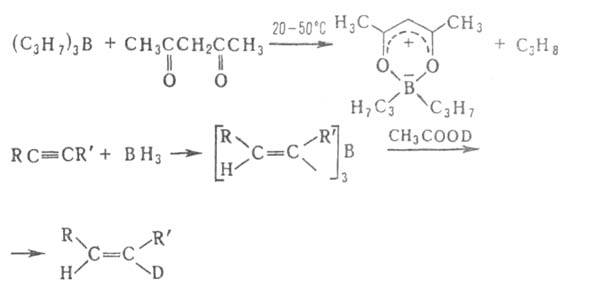
Триалкилбораны и алифатич. борацикланы реагируют с Н2О, ROH, R2NH, . H2S, щелочами и неорг. к-тами при 150-200 °С с разрывом одной связи В—С; при этом образуются R2BX, RH, H2 и олефин.
В присут. каталитич. кол-в меркаптанов (и следов О2) или (СН3)3ССООН т-ра р-ции м. б. снижена до 20-70°С. Многие борорганические соединения расщепляются карбоновыми к-тами с образованием углеводородов (при этом конфигурация атома С в![]() положении не меняется): R3B + R'COOH - > 3RH.
положении не меняется): R3B + R'COOH - > 3RH.
Алкинилбораны расщепляются водой и спиртами при 0°С, арил- и винилбораны - водой, спиртами и карбоновыми к-тами при 20-80°С (исключение - тримезитилборан), напр.:

Протолиз бензил- и аллилборанов осуществляется с перегруппировкой:
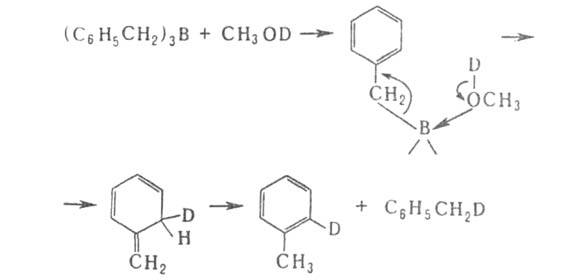
Арилбораны взаимод. с галогенами с образованием арилгалогенидов.
Типичные р-ции электроф. замещения - переметаллирование, используются для получения металлоорганич. соед., напр.:
--> ЧИТАТЬ ПОЛНОСТЬЮ <--