Реферат: Дисперсность
Существует две группы способов получения дисперсных систем:
1. Способы диспергирования заключаются в раздроблении тела до коллоидного состояния (мукомольное производство).
2. Способы конденсации заключаются в укрупнении частиц, атомов, молекул до частиц коллоидных размеров (химическая реакция с образованием осадка).
Молекулярно-кинетические свойства дисперсных систем
Все молекулярно-кинетические свойства вызваны хаотическим тепловым движением молекул дисперсионной среды, которое складывается из поступательного, вращательного и колебательного движения молекул.
Молекулы жидкой и газообразной дисперсионной среды находятся в постоянном движении и сталкиваются между собой. Среднее расстояние, проходимое молекулой до столкновения с соседней, называют средней длиной свободного пробега. Молекулы обладают различной кинетической энергией. При данной температуре среднее значение кинетической энергии молекул остается постоянным, составляя для одной молекулы и одного моля:
![]() ;
; ![]() ,
,
где m – масса одной молекулы;
M – масса одного моля;
v – скорость движения молекул;
k – константа Больцмана;
R – универсальная газовая постоянная.
Флуктуация значений кинетической энергии молекул дисперсионной среды (т.е. отклонение от среднего) и является причиной молекулярно-кинетических свойств.
Изучение молекулярно-кинетических свойств возможно в результате применения статистических методов исследования, действительных для систем, состоящих из множества элементов (молекул). Исходя из допущения о беспорядочности движения отдельных молекул, теория определяет наиболее вероятное сочетание для систем из множества объектов. Молекулярно-кинетические свойства проявляются в жидкой и газообразной среде, молекулы которых обладают определенно подвижностью.
Броуновское движение
Броуновским называют непрерывное, хаотическое, равновероятное для всех направлений движение мелких частиц, взвешенных в жидкостях или газах, за счет воздействия молекул дисперсионной среды.
Мельчайшие частицы незначительной массы испытывают неодинаковые удары со стороны молекул дисперсионной среды, возникает сила, движущая частицу, направление и импульс силы, непрерывно меняются, поэтому частица совершает хаотические движения.

Определили эти изменения и связали их с молекулярно-кинетическими свойствами среды в 1907 году А. Эйнштейн и М. Смолуховский. В основе расчета – не истинный путь частицы дисперсной фазы, а сдвиг частиц. Если путь частицы определяется ломаной линией, то сдвиг х характеризует изменение координат частицы за определенный отрезок времени. Средний сдвиг определяет среднеквадратичное смещение частицы:
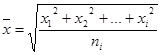 ,
,
где х 1 , х 2 , х i – сдвиг частиц за определенное время.
Теория броуновского движения исходит из представления о взаимодействии случайной силы f (t), характеризующей удары молекул, силы F t , зависящей от времени, и силы трения при движении частиц дисперсной фазы в дисперсионной среде со скоростью v. Уравнение броуровского движения (уравнение Ланжевена) имеет вид: ![]() , где m – масса частицы; h - коэффициент вязкости дисперсионной среды. Для больших промежутков времени (t>>m /h) инерцией частиц (m (dv / d t) можно пренебречь. После интегрирования уравнения
, где m – масса частицы; h - коэффициент вязкости дисперсионной среды. Для больших промежутков времени (t>>m /h) инерцией частиц (m (dv / d t) можно пренебречь. После интегрирования уравнения 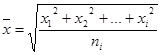 при условии, что среднее произведение импульсов случайной силы равно нулю, среднее значение флуктуации (средний сдвиг) равно:
при условии, что среднее произведение импульсов случайной силы равно нулю, среднее значение флуктуации (средний сдвиг) равно: 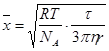 , где t - время; r – радиус частиц дисперсной фазы; N A – число Авогадро частиц.
, где t - время; r – радиус частиц дисперсной фазы; N A – число Авогадро частиц.
В этой формуле ![]() характеризует молекулярно-кинетические свойства дисперсионной среды, h - ее вязкость, r – радиус частиц – параметр, относящийся к дисперсной фазе, а время t определяет взаимодействие дисперсионной среды с дисперсной фазой.
характеризует молекулярно-кинетические свойства дисперсионной среды, h - ее вязкость, r – радиус частиц – параметр, относящийся к дисперсной фазе, а время t определяет взаимодействие дисперсионной среды с дисперсной фазой.
Кроме поступательного, возможно вращательное броуновское движение для двухмерных частиц и частиц неправильной формы (нитей, волокон, хлопьев и т.д.).
Броуновское движение наиболее интенсивно проявляется в высокодисперсных системах (размеры частиц 10-9 ¸ 10-7 м), несмотря на то, что молекулы дисперсионной среды действуют также и на частицы средне- и грубодисперсных систем. Но в связи со значительным размером частиц число ударов молекул резко увеличивается. По законам статистики, импульс действия сил со стороны молекул среды взаимно компенсируется, а значительная масса и инерция крупных частиц оставляет воздействие молекул без последствий.
Тема 1.1.2. Диффузия
Диффузией называют самопроизвольное распространение вещества из области с большей концентрацией в область с меньшей концентрацией. Различают следующие виды диффузии: молекулярную, ионную и коллоидных частиц.
 Ионная диффузия связана с самопроизвольным перемещением ионов.
Ионная диффузия связана с самопроизвольным перемещением ионов.
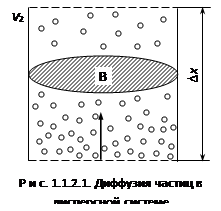
Диффузия высокодисперсных коллоидных частиц показана на рис. 1.1.2.1. В нижней части концентрация частиц больше, чем в верхней, т.е.
v1 >v2 (где ![]() , м3 – численная
, м3 – численная
концентрация частиц, N – число частиц дисперсной фазы, V д.с. – объем дисперсной системы). Диффузия направлена из области с большей концентрации в область с меньшей концентрацией, т.е. снизу вверх (на рис. показано стрелкой). Диффузия характеризуется определенной скоростью перемещения вещества через поперечное сечение В , которая равна ![]() .
.
На расстоянии Dх разность концентраций составит v 2 – v 1 , т к. v 1 >v 2 , эта величина отрицательна. Изменение концентрации, отнесенное к единице расстояния, называют градиентом концентрации ![]() или (в дифф. форме)
или (в дифф. форме) ![]() .
.
Скорость перемещения вещества пропорциональна градиенту концентрации и площади В , через которую происходит движение диффузионного потока, т.е.
![]() ;
; ![]() -
-
- основное уравнение диффузии в дифференциальной форме.
Скорость диффузии (![]() ) величина положительная, а градиент концентрации
) величина положительная, а градиент концентрации ![]() - отрицателен.; поэтому перед правой частью уравнения – знак «минус». Коэффициент пропорциональности D – это коэффициент диффузии . Основное уравнение справедливо для всех видов диффузии , в т.ч. и для коллоидных частиц. В интегральной форме оно применимо для двух процессов – стационарного и нестационарного:
- отрицателен.; поэтому перед правой частью уравнения – знак «минус». Коэффициент пропорциональности D – это коэффициент диффузии . Основное уравнение справедливо для всех видов диффузии , в т.ч. и для коллоидных частиц. В интегральной форме оно применимо для двух процессов – стационарного и нестационарного: