Реферат: Формальная кинетика сложных реакций
2.1) Прежде, чем решить ввести один из основных приёмов формальной кинетики, целесообразно напомнить необходимые сведения о решении линейного неоднородного дифференциального уравнения первого порядка.
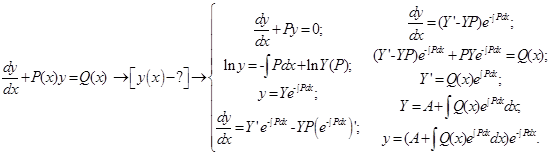
2.2) Далее обратимся к нашей конкретной химической задаче. Рассмотрим двухстадийный механизм последовательного превращения, в котором обе элементарные стадии являются реакциями 1-го порядка:
![]() Положим [A]0=[B]¥=a (рис.8). Упростим обозначения концентраций:
Положим [A]0=[B]¥=a (рис.8). Упростим обозначения концентраций: ![]() Составим и решим систему кинетических уравнений:
Составим и решим систему кинетических уравнений:
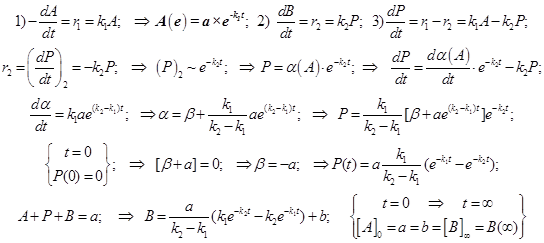
Получается сводка уравнений для концентраций реагента, промежуточного соединения и продукта:
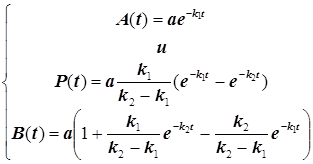 (3.6)
(3.6)
2.3) а) Если значительно превалирует константа скорости 1-й стадии, то промежуточный продукт накапливается в значительных количествах. 2-я стадия лимитирующая и определяет вид кинетической кривой для накопления продукта B. Кинетическая кривая второй стадии представлена в виде почти чистой спадающей экспоненты, максимум на кривой превращения промежуточного продукта появляется спустя очень малый начальный период времени (индукционный период). Идеальная экспонента (это кинетическая кривая первого порядка для превращения промежуточного продукта) оказывается в этом случае верхней асимптотой, и к ней стремится реальная кривая превращения промежуточного продукта.
б) Если значительно превалирует константа скорости 2-й стадии, то промежуточный продукт находится в системе в минимальных количествах, 1-я стадия лимитирующая и определяет вид кинетической кривой накопления продукта B. Вторая стадия на графике как бы не просматривается.
в) Может иметь место случай сравнимых скоростей обеих стадий реакции. Это случай и более сложный, и менее однозначный. Эти положения достаточно легко иллюстрируются графически (см. учебник Краснова).
Двусторонние (обратимые) реакции первого порядка
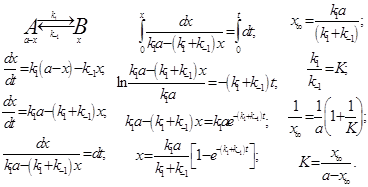
Проблема систематического описания сложных реакций сложна, и в наиболее общем виде решается лишь численными (и не аналитическими) методами... Разработаны различные аналоговые методы, позволяющие даже в очень непростых случаях эффективно графически моделировать кинетические кривые. Вместе с тем часто есть возможность избежать последовательного решения системы дифференциальных уравнений, заменяя точные решения приближёнными. Не располагая возможностью рассмотреть всю проблему в полном объёме, мы вынуждены ограничиться лишь несколькими характерными примерами …
1) Метод квазистационарных концентраций Боденштейна
Рассмотрим примеры сложных реакций, представляющих собою суперпозицию последовательных и параллельных превращений и введём некоторые важные приёмы их описания:
|
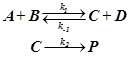
протекает по двум или более путям. Этот принцип чрезвычайно важен при анализе внутримолекулярных процессов типа циклических движений марковских перескоков в виде трёхпозиционного вращения.
См. примеры.
Пример 3.1. Рассмотрим кинетическую схему реакции: 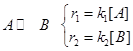
и ту же самую реакцию в присутствие протонов: 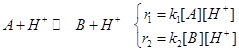
Скорость реакции равна: ![]()
И в условиях равновесия приходим к сомнительному результату вида:
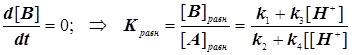 (4.7)
(4.7)
Возникает парадокс, согласно которому константа равновесия, вопреки незыблемым установкам термодинамики, выглядит зависимой от концентрации протонов. Для его устранения вводится принцип детального равновесия. Он состоит в том, что система кинетических уравнений дополняется условиями детального равновесия:
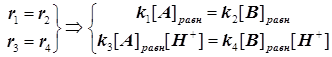 (4.8)
(4.8)
В результате концентрация протонов исчезает из выражения константы скорости, а именно:
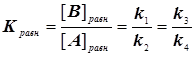 (4.9)
(4.9)
Пример 3.2. Рассмотрим кинетику циклического превращения вида:
Если уравнение скорости реакции включает сумму различных членов для прямой реакции, что указывает на возможность нескольких путей её протекания, то принцип детального равновесия требует, чтобы каждый член в выражении для скорости прямой реакции был скомпенсирован при равновесии соответствующим членом в выражении для скорости обратной реакции.
4) Мономолекулярные реакции. Схема Линдемана.