Реферат: Химическая кинетика и равновесие
![]() бимолекулярная (
бимолекулярная (![]() )
)
![]() тримолекулярная.
тримолекулярная.
Больше 3‑х не бывает, т.к. столкновение более 3‑х частиц сразу – маловероятно.
Когда реакция идёт в несколько стадий, то общая ![]() реакции =
реакции = ![]() наиболее медленной стадии (лимитирующей стадии).
наиболее медленной стадии (лимитирующей стадии).
Зависимость скорости реакции от температуры определяется эмпирическим правилом Вант-Гоффа : при увеличении температуры на ![]() , скорость химической реакции увеличивается в 2 – 4 раза:
, скорость химической реакции увеличивается в 2 – 4 раза: ![]() .
.
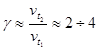
![]() ,
,
где ![]() – температурный коэффициент скорости химической реакции
– температурный коэффициент скорости химической реакции 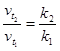 .
.
Не всякое столкновение молекул сопровождается их взаимодействием. Большинство молекул отскакивают как упругие шарики. И только активные при столкновении взаимодействуют друг с другом. Активные молекулы обладают некоторой избыточной ![]() но сравнению с неактивными молекулами, поэтому в активных молекулах связи между ними ослаблены.
но сравнению с неактивными молекулами, поэтому в активных молекулах связи между ними ослаблены.
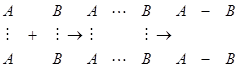
Энергия для перевода молекулы в активное состояние – энергия активации ![]() . Чем она меньше, тем больше частиц реагируют, тем больше скорость химической реакции.
. Чем она меньше, тем больше частиц реагируют, тем больше скорость химической реакции.
Величина ![]() зависит от природы реагирующих веществ. Она меньше
зависит от природы реагирующих веществ. Она меньше ![]() диссоциации – наименее прочной связи в реагентах.
диссоциации – наименее прочной связи в реагентах.
Изменение ![]() в ходе реакции:
в ходе реакции:
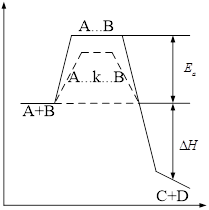
![]() выделяется (экзотермическая)
выделяется (экзотермическая)
С увеличением температуры число активных молекул растёт, поэтому ![]() увеличивается.
увеличивается.
Константа ![]() химической реакции связана с
химической реакции связана с
![]() :
: ![]() ,
,
где ![]() – предэкспоненциальный множитель (связан с вероятностью и числом столкновений).
– предэкспоненциальный множитель (связан с вероятностью и числом столкновений).
В зависимости от природы реагирующих веществ и условий их взаимодействия, в элементарных актах реакций могут принимать участие атомы, молекулы, радикалы или ионы.
Свободные радикалы чрезвычайно реакционноспособны, ![]() активных радикальных реакций очень мала (
активных радикальных реакций очень мала (![]() ).
).
Образование свободных радикалов может происходить в процессе распада веществ при температуре, освещении, под действием ядерных излучений, при электроразряде, сильных механических воздействиях.
Многие реакции протекают по цепному механизму . Особенность цепных реакций состоит в том, что один первичный акт активации приводит к превращению огромного числа молекул исходных веществ.
Например: ![]() .
.
При обычной температуре и рассеянном освещении реакция протекает крайне медленно. При нагревании смеси газов или действия света, богатого УФ лучами (прямой солнечный свет, свет от горящего ![]() ) смесь взрывается.
) смесь взрывается.
Эта реакция протекает через отдельные элементарные процессы. Прежде всего, за счёт поглощения кванта энергии УФ лучей (или температуры) молекула ![]() диссоциируется на свободные радикалы – атомы
диссоциируется на свободные радикалы – атомы ![]() :
: ![]() , затем
, затем ![]() , затем
, затем ![]() и т.д.
и т.д.
Естественно, возможно столкновение свободных радикалов и друг с другом, что приводит к обрыву цепей: ![]() .
.
Кроме температуры на реакционную способность веществ существенное влияние оказывает свет. Воздействие света (видимого, УФ) на реакции изучает раздел химии – фотохимия.
Фотохимические процессы весьма разнообразны. При фотохимическом действии молекулы реагирующих веществ, поглощая кванты света, возбуждаются, т.е. становятся реакционноспособными или распадаются на ионы и свободные радикалы. На фотохимических процессах основана фотография – воздействие света на светочувствительные материалы (фотосинтез).
Одним из наиболее распространённых в химической практике методов ускорения химических реакций является катализ . Катализаторы – вещества, изменяющие ![]() химической реакции за счёт участия в промежуточном химическом взаимодействии с компонентами реакции, но восстанавливающие после каждого цикла промежуточного взаимодействия свой химический состав.
химической реакции за счёт участия в промежуточном химическом взаимодействии с компонентами реакции, но восстанавливающие после каждого цикла промежуточного взаимодействия свой химический состав.