Реферат: Методы изучения масс микрочастиц
В 1815 році для пояснення розташування атомних ваг елементів поблизу цілочисельних значень Проут (1786-1850 рр.) запропонував гіпотезу про те, що всі елементи походять з водню шляхом його конденсації. З цієї гіпотези, звичайно, випливало, що атомні ваги всіх елементів повинні бути цілими, кратними атомній вазі водню.
На початку XIX ст. ідея Проута знайшла гарячих прихильників і не менш гарячих противників. Прихильників привертала простота його гіпотези. Противники свої заперечення аргументували тим, що з гіпотези Проута випливає точна цілочисельність атомних ваг елементів, яка насправді не має місця. При цьому вони доводили, що чим вища точність вимірювання атомних ваг елементів, тим помітніше це розходження. Крім того, хлор і деякі інші елементі явно мають нецілочисельну атомну вагу.
3. Загадка нецілочисленності атомної ваги елементів
В ХІХ ст. Дальтон запропонував п’ять постулатів, які лягли в основу сучасної хімії. І сам Дальтон одним необгрунтованим формулюванням заплутав дослідників.
В своєму п’ятому постулаті він дав визначення поняття "елемент" або "хімічний елемент" таким чином: всі атоми одного і того ж елемента однакові і рівні по вазі. В сучасній науці хімічними елементами називають речовини, що мають постійні властивості і не подільні на інші складові ніяким хімічним втручанням. Друга частина його визначення - рівність по вазі всіх атомів даного елемента - чиста гіпотеза
Лише в 1886 р. Вільям Крукс висунув іншу точку зору. Крукс добре розумів, що до тих пір, поки атомна вага елементів визначається не для окремих атомів, а як середня вага дуже великого їх числа, то пропозиція про різну атомну вагу окремих атомів одночасно і того ж елемента не може бути обгрунтованою. Крукс запропонував правильну думку про те, що у атомів даного елемента, які мають різну вагу, повинні бути різні оптичні спектри. При подальшому дослідженні вияснилось, що спостережувані ним спектри справді належали іншим елементам, які були присутні в досліджуваній речовині у вигляді домішок.
Тепер ми знаємо, що Крукс був правий і що атоми одного і того ж елемента але різної ваги існують і дійсно дають різні спектри. Крім того, тепер зрозуміло, чому їх не змогли побачити тоді: розділення таких атомів дифузією малоефективне і потребує застосування надзвичайно тонкої методики, якої на той час не було.
Ідея про атоми одного елемента, які мають різну вагу, була на довгий час (на цілі десятиліття) відкинута.
Тільки в 1916 р. в зв’язку з розвитком досліджень по радіоактивності Фредерік Содді висловив ідею про речовини, ідентичні по своїх хімічних властивостях, але які мають різну атомну вагу. Було показано існування речовини з однаковими хімічними властивостями і різною атомною вагою.
Содді запропонував такі речовини називати ізотопами (по грецьки i d u z - однаковий, t o p o z - місце).
4. Зважування "мішка" атомів
Багато років хіміки мали справу лише з відносними атомними вагами елементів. Коли потрібно було розробити методи визначення абсолютної ваги атомів, то на допомогу прийшли фізики. Вони застосували свої дуже чутливі методи дослідження.
Таким чином, поставлена мета була досягнута: була визначена маса атомів різних елементів. Однак як і слід було очікувати від методу зважування мішка зерен, для кожного елемента було лише середнє значення маси даного типу атомів.
В звичайному стані атом будь-якої речовини електрично нейтральний. Якщо його розділити, то одержуються дві частки і обидві електрично заряджені. Їх називають іонами. При цьому негативним іоном є електрон, а позитивним - ядро атома з декількома електронами, що залишились. Позитивний іон є носієм індивідуальності атома, а також майже всієї його маси (більше 99,9%). Таким чином, бажаючи визначити масу атома, ми можемо зважити відповідний позитивний іон.
Подивимось, як цим скористався Томсон для визначення маси іонів. Потрібно було одержати пучок позитивних іонів. Для цього він виготовив установку (рис. 1) на якій посудина С через відповідні отвори О1 і О2 заповнюється досліджуваним газом. До електродів А і К прикладено високу напругу ~(3-5)×104 В. Під дією напруги електрони вириваються із атомів і газ в посудині іонізується. Електрони прямують до позитивно зарядженого електрода +А , а позитивні іони - відповідно до негативного електрода -К . В негативному електроді зроблено циліндричний отвір - канал, через який пучок позитивних іонів виводиться в ліву частину установки. Попутно ці іони проходять між зарядженими електродами +U і -U та полюсами магніту, що утворюють магнітне поле (див. рис. 1).
Для виключення взаємного впливу і можливих спотворень обидві частини установки розділили магнітним екраном, що зроблений з м’якого заліза. Таким чином, пучок іонів досягає фотопластинки вже зазнавши відхилення в електричному і магнітному полях. Екран служить для візуального спостереження зміщення пучка іонів і використовується при налагоджуванні установки.
Якщо б іони мали однакові заряди, масу і швидкість, то при включенні електричного поля вони відхилялися б вниз і потрапили в точку 1 (рис. 1). Точка 0 відповідає невідхиленому пучку. При тих же умовах і включенні лише магнітного поля іони відхилились би і потрапили в точку 2. При включенні обох полів одночасно іони потрапляють в точку 3. Однак це справедливо лише при однакових
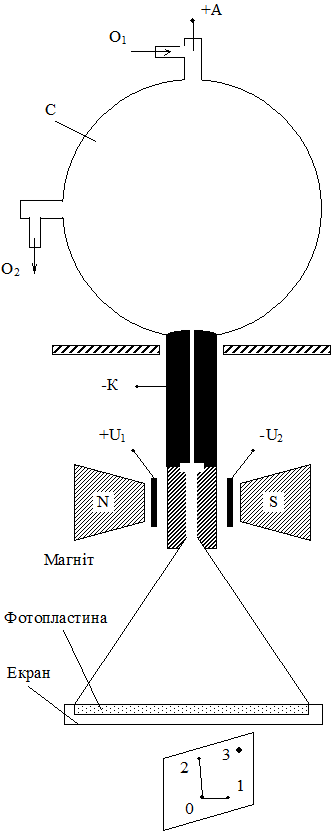
Рис. 1. Принципова схема установки Томсона для визначення маси іонів.
зарядах, масах і швидкостях іонів. Чи справджується ця умова в даній установці? Виявилось, що заряд більшості іонів рівний +1 (в одиницях елементарного заряду), а в деяких +2. При цьому розрізнити такі іони не складає великих труднощів. Що стосується швидкості, то вона зовсім не однакова для різних іонів.
Таким чином реальною умовою досліду є твердження, коли заряди і маси іонів однакові, а швидкість різна. При цьому під дією електричного і магнітного полів іони потрапляють вже не в одну і ту ж точку, а в залежності від швидкості розміщуються по відрізку параболи. Якщо в посудині С міститься не один газ, а суміш декількох, то пучок позитивних іонів складається з декількох груп іонів з різною масою. Тоді на фотопластинці одержується зображення декількох відрізків параболи. Причому кожен відрізок відповідає іонам з однією і тою ж масою.
Метод парабол вперше дозволив виміряти масу окремих іонів, а не середню масу великого їх числа.
5. Визначення мас ізотопів з допомогою мас-спектрографа
В 1919 р. Астон запропонував новий метод фокусування пучка іонів, який дозволив в значній мірі обійти недоліки методу параболи. Розроблений і побудований Астоном пристрій дістав назву мас-спектрографа.
Розглянемо схему і будову мас-спектрографа Астона (рис. 2). Пристрій складається з джерела іонів, двох вузьких паралельних щілин Щ1 і Щ2 , двох паралельних пластин П1 і П2 , до яких прикладена напруга, діафрагми, потужного постійного магніту, екрана і фотопластинки. Джерело іонів складається із посудини, заповненої досліджуваним газом,
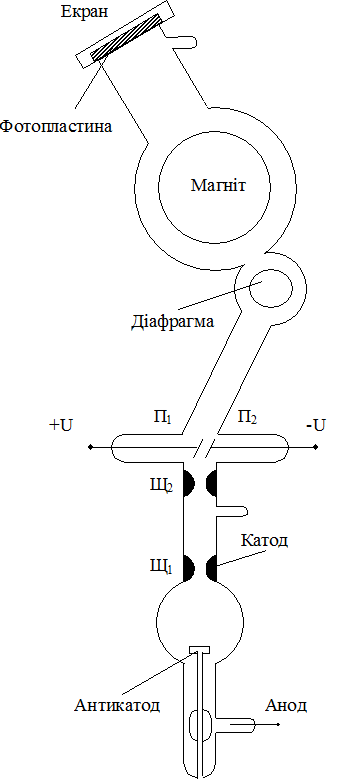
Рис. 2. Принципова схема мас-спектрографа Астона.
анода, катода з щілиною Щ1 і антикатода. Між анодом і катодом прикладено високу напругу від 2×104 до 5×104 В, яка і дає іонізацію.
Іони, що створені в посудині джерела, проходячи через щілини Щ1 і Щ2 , складають вузький пучок частинок. Цей пучок відхиляється в електричному полі, причому кут відхилення обернено пропорційний енергії частинки ![]() . Таким чином проходить розкладання пучка іонів по енергії. Потім цей пучок іонів потрапляє в однорідне магнітне поле, яке напрямлене так, щоб відхилити іони в зворотній бік. Магнітне поле відхиляє іони на кут, обернено пропорційний імпульсу часток mV . При проходженні іонів послідовно через електричне і магнітне поля ті з іонів, у яких питомий заряд e /m однаковий, збираються на екрані чи фотопластинці в одній і тій же точці.
. Таким чином проходить розкладання пучка іонів по енергії. Потім цей пучок іонів потрапляє в однорідне магнітне поле, яке напрямлене так, щоб відхилити іони в зворотній бік. Магнітне поле відхиляє іони на кут, обернено пропорційний імпульсу часток mV . При проходженні іонів послідовно через електричне і магнітне поля ті з іонів, у яких питомий заряд e /m однаковий, збираються на екрані чи фотопластинці в одній і тій же точці.
Якщо в початковому пучку наявні іони різних ізотопів, то внаслідок різниці їх питомих зарядів вони фокусуються в різних місцях екрану і складають там зображення у вигляді окремих ліній. Визначення маси того чи іншого ізотопу проводиться порівнянням ліній від досліджуваного ізотопу з еталонними лініями, одержаними на тій же спектрограмі від ізотопів, маса яких відома. Відношення відстаней між ними дає змогу визначити відношення їх мас.
Вже перший мас-спектрометр Астона, побудований на цьому принципу і працюючий з 1919 по 1925 рр., дозволив виміряти атомні ваги ізотопів з похибкою менше 1%. Однак різниця атомної ваги деяких ізотопів від цілочисельних значень складає лише одиниці процентів. Тому така точність не змогла задовольнити вчених.
В 1925 р. Астон удосконалив свій мас-спектрограф і довів його роздільну здатність до 10-4 , тобто 0,01%. Для цього довжина шляху іонів в пристрої була збільшена вдвоє, покращена форма відхиляючих пластин, стабілізація магнітного поля і т.д.
В подальші роки Демнестер, потім Смаліо і Маттаун, а потім Нір розробили деякі нові принципи фокусування іонів і побудувавши відповідні пристрої, досягли вищої точності вимірювання маси ізотопів. Висока чутливість пристрою Ніра дозволила виявити наявність даного ізотопу, змішаного з іншими, навіть якщо його відносний ваговий вміст складав лише 1/100000.
В 1937 р. на своєму третьому, ще більш удосконаленому мас-спектрографі Астон одержав спектрограми чіткіші, різкіші і з більшою дисперсією, тобто з великим зміщенням положення ліній при зміні маси ізотопу. Це дозволило йому визначити атомну вагу ізотопів з точністю до п’ятого знаку. Таким чином, похибка його вимірювань складала лише тисячні долі процента. Самим легким позитивним іоном є протон - ядро атома водню. В 50-х роках нашого століття була визначена маса протона mp =1,6724×10-27 кг з похибкою біля 0,002%. По даних одержаних до 1972 р. маса протона складає (1,6726513±0,0000087)×10-27 кг, тобто вона знайдена з похибкою 0,0005%.
6. Залежність маси електрона від швидкості
Для того, щоб зважити електрон, Томсон користувався таким же пристроєм, але при цьому змінив полярність на електродах колби джерела і таким чином вивів через щілину пучок негативно заряджених частинок ‑ електронів.
Умова фокусування для електронів така ж, як і для позитивних іонів, тільки у відповідності з протилежним знаком заряду їх відхилення відбувається в інший бік. Знаючи величину напруженості електричного і магнітного полів в пристрої і вимірявши зміщення плями на екрані або фотопластинці, Томсон зміг обчислити питомий заряд електрона e/m . Так як заряд електрона вже був відомий, то він зміг знайти і масу електрона, яка була рівною me =9´10-31 кг, що приблизно в 2000 раз менше маси іона водню.