Реферат: Методы определения активности катализаторов
1. Прямое измерение скорости реакции в каждом опыте.
2. Легкость достижения постоянства температуры в реакторе, даже для реакций со значительным тепловым эффектом, благодаря интенсивной циркуляции и соответственно малому изменению степени превращения в слое катализатора [1].
3. Осуществление процесса в режиме, аналогичном полному смешению при практическом отсутствии перепадов концентраций, скоростей и температур.
4. Возможность работы с любым количеством катализатора
вплоть до одной гранулы, при любых размерах гранул и соотношениях размеров гранул и реактора.
5. Высокая линейная скорость реакционной смеси, что облегчает устранение искажений, связанных с переносом вещества к наружной поверхности зерен катализатора, т. е. внешне-диффузионным торможением.
Искажение, связанное с Переносом внутри зерен (т. е. внутри-диффузионное торможение) сохраняется. Его снятие требует уменьшения размера зерен катализатора при испытании. Сохраняя неизменным химический состав и меняя размеры зерен катализатора, можно выявить влияние пористой структуры на активность контактной массы, т.е. определить внутри-диффузионное торможение при различных размерах, а также максимальный размер зерен, соответствующий переходу от внутридиффузионной к кинетической области.
К недостаткам проточно-циркуляционного метода можно отнести: 1) сложность аппаратурного оформления; 2) необходимость достаточных количеств исходных веществ и времени для достижения стационарного состояния, в некоторых случаях— возможное усиление побочных процессов [1].
Существенные преимущества проточно-циркуляционного метода подтверждают целесообразность его применения при изучении кинетики реакций. Схема проточно-циркуляционной установки для окисления сернистого ангидрида приведена на рис. 4. Сернистый ангидрид, азот и кислород из баллона дозируют клапаном тонкой регулировки в осушительную систему. Точный расход газов регулируют моностатом и замеряют реометром. Затем смесь газов поступает в циркуляционный контур; анализ газовой смеси на входе и выходе из цикла производят по методу Рейха. Для предотвращения «залипания» клапанов вследствие конденсации SОз производят постоянный электрообогрев клапанной коробки 10. Реактор 12 представляет, собой трубу с сеткой и впаянным карманом для термопары. Во время эксперимента реактор помещают в цилиндрическую печь с автоматической регулировкой температуры. Установка позволяет работать при температурах от 0 до 620 °С. Степень превращения х рассчитывают по формуле
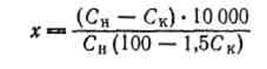 (6)
(6)
где Сн , Ск —начальная и конечная концентрации SO2 , соответственно, объемн.%.
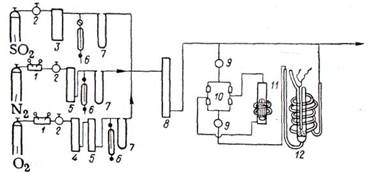
Рис. 4. Проточно-циркуляционная установка для окисления S02 : 1—редуктор; 2—вентиль тонкой регулировки; 3 — барботер с H2 SO4 ; 4—колонка с CuO; 5—колонка с ангидроном; 6—моностат с дибутил-фталатом; 7—реометр; 8—колонка с P2 O5 ; 9—ловушка; 10 —клапанная коробка; 11 — циркуляционный насос; 12—реактор.
Активность катализатора характеризуется константой скорости, рассчитанной по уравнению Борескова [1].
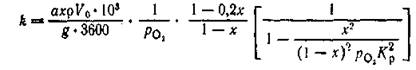 (7)
(7)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() где а — исходная концентрация SО2 , объемн.%; х — степень превращения, доли ед.; g — навеска катализатора, г; р — насыпная плотность катализатора, г/мл; V0 — скорость подачи газа, приведенная к нормальным условиям, дм3 /ч; p— парциальное давление кислорода в исходном 'газе, кгс/см2 ; /Ср — константа равновесия, кгс/см2 .
где а — исходная концентрация SО2 , объемн.%; х — степень превращения, доли ед.; g — навеска катализатора, г; р — насыпная плотность катализатора, г/мл; V0 — скорость подачи газа, приведенная к нормальным условиям, дм3 /ч; p— парциальное давление кислорода в исходном 'газе, кгс/см2 ; /Ср — константа равновесия, кгс/см2 .
Существует «дифференциальный» способ исследования каталитической активности, представляющий собой обычный проточный метод при малом количестве катализатора и больших объемах протекающей реакционной смеси, т. е. при больших объемных скоростях. Благодаря этому, изменение степени превращения в слое катализатора невелико, и количество превращенного вещества может служить мерой скорости реакции. Однако, этот метод не обеспечивает достаточную точность измерения скорости реакции.
В проточно-циркуляционных методах для расчета скорости реакции используют не малую разность концентрационной смеси на входе и выходе из слоя катализатора, а значительную разность концентраций смеси, поступающей в циркуляционный контур и выходящей из него. Благодаря этому каталитическая активность проточно-циркуляционным методом может быть измерена с гораздо большей точностью [1].
Помимо перечисленных наиболее распространенных методов существует и ряд других, позволяющих оценить активность контактных масс.
Метод изучения кинетики реакций во взвешенном слое катализатора приобретает большое значение, в частности, при моделировании производственных условий некоторых процессов. Ведение реакций во взвешенном слое требует тщательного выбора гидродинамических условий, приближающихся к моделируемому процессу. Прежде всего важно, аналогичное моделируемому процессу, отношение действительной скорости wк скорости начала взвешивания wB катализатора.[1]
Скорость начала взвешивания можно определить по формуле
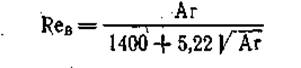 (8)
(8)
где Reв = щв d3 / н – критерий Рейнольдса; Ar = gd3 3 / н2 * ств – сг / сг - критерий Архимеда; d3 — средний размер зерен; рг , ртв — плотности газа и твердых частиц, соответственно; v — кинематический коэффициент вязкости газа.
Уравнение (8) применимо для моно- и полидисперсных слоев с частицами сферической и неправильной формы в широком диапазоне чисел Re и позволяет определять wr с точностью до ±30%.
Общей формулой для расчета широкого диапазона скоростей (в м/с) является та, в которой истинная скорость в начале взвешивания wB .B = wB /e0 (e0 —порозность слоя) составляет:
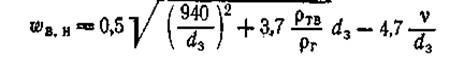 (9)
(9)
Средний размер частиц может быть определен различными способами. При достаточно узком гранулометрическом составе частиц, по форме близкой к сферической, если их размер меняется от d31до d32:
![]() (10)
(10)
При широком гранулометрическом составе путем рассева выделяют узкие фракции и рассчитывают их средний диаметр d3 по формуле (10) и долю частиц At с этим размером. Средний диаметр частиц всех фракций катализатора может быть рассчитан по формуле: