Реферат: Молекулярні механізми перенесення сигналів регуляторів функції кори надниркових залоз
Дослідження месенджерних систем, що опосередковують сигнали актг в адренокортикальних клітинах. Регуляція кортикотропіном адренокортикальної функції забезпечується здебільшого за рахунок прямого фосфорилювання cAMP-залежною ПКА специфічних білків, а також стероїдогенних факторів, що беруть участь в реакціях стероїдогенезу, змінюючи його швидкість. Не викликає сумнівів, що cAMP/ПКА-залежна месенджерна система не є єдиною системою опосередкування дії АКТГ в клітині. Гормон здатний активувати різні протеїнкінази, проте інші сигнальні каскади, залучені до перенесення сигналів АКТГ, досліджені значно менше, ніж cAMP/ПКА-залежний. Особливу увагу дослідників в цьому аспекті привернула протеїнкіназа С. Відомо, що деякі протеїни можуть одночасно бути субстратами для кількох кіназ, що є важливим загальним принципом інтеграції пострецепторних сигналів в клітині. Це істотно ускладнює розуміння механізмів опосередкування регуляторних сигналів АКТГ та можливої взаємодії між різними месенджерними системами. Потрібно також зазначити, що механізми дії АКТГ досліджувались раніше здебільшого на лініях пухлинних клітин надниркових залоз, спробу оцінки дії гормону на умовно нормальних тканинах надниркових залоз людини ми провели вперше.
Участь цAMФ-залежної ПКА та серин/треонінової протеїнкінази С в реалізації ефектів АКТГ. На початку досліджень необхідним було з’ясування специфіки механізмів перенесення регуляторного сигналу АКТГ в корі надниркових залоз людини із залученням цAMФ-залежної ПКА та серин/треонінової ПКС. В дослідах використовували післяопераційні умовно нормальні тканини надниркових залоз хворих, прооперованих у клініці Інституту. АКТГ in vitro у концентрації 0,2 од./100 мг тканини не призводить до активації ПКА та ПКС ні в мембранній, ні в цитозольній фракціях. При збільшенні концентрації кортикотропіну до 2 од./100 мг тканини протеїнкіназна активність у мікросомній фракції зростає у 4,5 рази порівняно з контрольними пробами у випадку ПКА та у 1,4 рази у випадку ПКС. Визначення розподілу ізоформи ПКС-a в субклітинних фракціях клітин після інкубації у середовищі з різним вмістом АКТГ за допомогою імуноблот-аналізу показало, що із збільшенням концентрації кортикотропінукількість ферменту зростала в ядерній фракції (рис. 1), не змінюючись ні в мікросомній, ні в цитозольній фракціях адренокортикоцитів. Отже, суттєва роль у трансдукції сигналу кортикотропіну в адренокортикальних клітинах людини може належати не тільки мембранозв’язаній формі ПКС, але і ядерній ПКС.
 |
 |
![]()
|
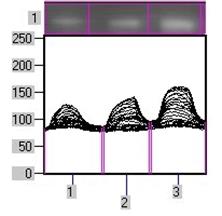
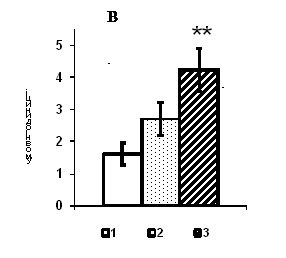
Рис. 1. Вміст a-ізоформи ПКС в ядерній фракції адренокортикоцитів умовно нормальної тканини кори надниркових залоз людини при різних концентраціях АКТГ.
А - Вестерн-блот аналіз. Б - сканограма плівки. В - узагальнені результати п’яти дослідів. 1 – контроль, 2 – АКТГ 0,2 од./100 мг тканини, 3 – АКТГ 2 од./100 мг тканини.** - вірогідний вплив АКТГ, p < 0,05; критерій Стьюдента.
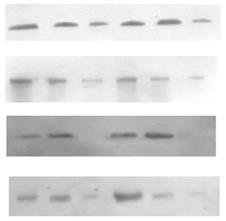
Субклітинний розподіл ПКС та експресія рецепторних тирозинкіназ в пухлинах надниркових залоз людини. Відомо, що у проліферативних процесах важливу роль відіграє ПКС, яка є важливою ланкою внутрішньоклітинних сигнальних механізмів, порушення яких призводить до ініціації та прогресії онкогенезу. Зміни рівня експресії ізоферментів ПКС та їхньої активності мають значний вплив на процеси проліферації та можуть бути залучені до процесів пухлинної трансформації у корі надниркових залоз. Тому доцільним було визначити загальну активність протеїнкінази С і розподіл ізоформ ПКС у субклітинних фракціях клітин адренокортикальних тканин надниркових залоз людини за умов норми і різноманітних патологічних станів. Визначення активності ПКС здійснювалось у цитозольній, мікросомній та ядерній фракціях пухлин та умовно нормальних тканин. Статистично вірогідна різниця спостерігається між активністю ПКС у мікросомній фракції клітин умовно нормальної та пухлинної тканин і не спостерігається у цитозолі та ядрах.В препаратах ядерної, цитозольної та мікросомної фракцій клітин кори надниркових залоз людини було проаналізовано експресію десяти ізоферментних форм ПКС. Найвищий рівень експресії спостерігався у випадку ПКС-α. На отриманих знімках чітко виявляються смуги білка у діапазоні молекулярної маси 80 кДа, що відповідає молекулярній масі α-ізоформи ПКС (рис. 2).
|
|
Експресії немає
ц м я ц м я
умовно аденома
нормальна
тканина
Рис. 2. Розподіл різних ізоформ протеїнкінази С в цитозольній (ц), мікросомній (м) та ядерній (я) субклітинних фракціях адренокортикоцитів в умовно нормальній і пухлинній тканинах надниркових залоз людини.
Ці дані узгоджуються з результатами інших авторів, які також визначали найвищий рівень експресії для α-ізоформи ПКС в адренокортикоцитах порівняно з досить незначним для інших ізоформ [Shigematsuetal., 1992].
Розподіл ПКС-a між цитозольною та мікросомальною фракціями визначається походженням тканини: в умовно нормальній тканині фермент рівномірно розподіляється між фракціями, а в аденомах (група, утворена об’єднанням всіх досліджених випадків доброякісних новоутворень) ПКС-a транслокується з цитозолю до мікросомної фракції. Найістотніша відмінність від контролю спостерігалась у випадках карцином. Для ядерної фракції не вдалося знайти певної закономірності між відносною кількістю ПКС-α та типом тканини (табл. 1). Виявлена транслокація ПКС-a розглядається нами як активація ферменту за умов дослідженої патології. Очевидно, саме ПКС-α бере активну участь у формуванні пухлин та підтримці пухлинного росту. Можливо, надекспресія цього ферменту, тривала активація ПКС внаслідок дії канцерогенних чинників або порушення метаболізму фосфоліпідних активаторів призводить до патологічної відповіді – порушення клітинного циклу та розвитку пухлин.
Отримані дані свідчать, що пухлини кори надниркових залоз характеризуються транслокацією основної ізоформи ПКС – Са2+ /фосфоліпід-залежної a-ізоформи до мікросомної фракції адренокортикоцитів і збільшенням загальної активності ПКС в мікросомній фракції пухлин. На разі можна стверджувати, що α-ізоформа ПКС в надниркових залозах може брати участь у онкогенезі і слугувати маркером малігнізації.
Таблиця 1
Розподіл a-ізоформи ПКС у цитозольній, мікросомній та ядерній фракціях клітин кори та пухлин надниркових залоз людини, %
| Тип тканини | Цитозольна фракція |
Мікросомна фракція |
Ядерна фракція |
| Умовно нормальна (8) | 46,19 ± 2,18 | 41,26 ± 1,97 | 13,62 ± 1,21 |
| Аденома (4) | 29,35 ± 3,61 | 50,40 ± 2,0 * | 17,40 ± 1,58 |
| Карцинома (4) | 26,09 ± 8,16 | 73,91 ± 8,16* | - |
Примітка. * - вірогідна різниця між цитозольною та мікросомною фракціями, р<0,05; критерій Стьюдента, кількість спостережень вказано в дужках.
Крім α-ізоформи ПКС позитивні результати було отримано для -ε, -δ, -η, -θ, -μ, -ζ ³зоформ. Розподіл ізоформ ПКС-α, -ε, -δ, -ζ μіж субклітинними фракціями наведено на рис. 2. ПКС-ε, -δ, -η, -θ, -μ βідносяться до родини нових, а ПКС-ζ до нетипових протеїнкіназ. Всі вищезгадані форми є Са2+ -незалежними, їх визначення в корі надниркових залоз було проведено вперше. Рівень експресії цих ізоферментів в корі надниркових залоз людини є досить високим, хоча меншим порівняно з Са2+ /фосфоліпід-залежною ПКС-α. За винятком δ-ізоформи, вони виявляються в усіх досліджуваних субклітинних фракціях – цитозольній, мікросомній та ядерній (рис. 2).
Розподіл ізоформ ПКС-ε, -δ, -ζ μіж цитозольною, мікросомальною та ядерною фракціями наведено у таблиці 2. У випадку ПКС-ε усереднені дані за всіма дослідженими групами демонструють переважний вміст ε-ізоформи ПКС у цитозольній фракції (табл. 2). Отже, розподіл протеїнкінази С-e не залежить від типу тканини і характеризується зсувом до цитозольної фракції. Транслокація ПКС-δ до мембранної фракції спостерігалась у випадку аденом. Розподіл ПКС-ζ є подібним до ПКС-e в аденомах. В умовно нормальній тканині різниця між цитозольною та мікросомною фракціями ставить менше 10 %. У аденомах відносний розподіл протеїнкінази С-ζ характеризується зсувом до цитозольної фракції. Частка ядерної фракції становить в досліджених групах 14-18 % (табл. 2).