Реферат: Очистка газообразных промышленных выбросов
Известковый метод. Принципиальная схема установки по очистке отходящих газов от SO2 известковым способом представлена на рис. 5. По этому способу отходящие газы подвергаются предварительной очистке от механических примесей (пыли, сажи) в батарейных циклонах 1 , после чего с помощью газодувки 2 направляются в скруббер 3, орошаемый известковым молоком.
При взаимодействии известкового молока с SO2 протекают реакции
SO2 + Н2 O = Н2 SO3 ;
Са (ОН)2 + SO2 = CaSO3 + 2H2 O.
По мере циркуляции раствора в нем накапливается соль СаSО3 . Когда концентрация ее в растворе достигнет 18—20%, раствор периодически заменяется свежим. Образовавшийся сернистокислый кальций плохо растворим в воде (0,138 г/л), поэтому в системе орошения скрубберов последовательно устанавливается кристаллизатор 5, служащий для выделения кристаллов сульфита кальция. Дальнейшее выделение CaSO3 происходит на вакуумфильтре 6. Шлам, состоящий из СаSО3 и CaSO4 , образующийся за счет реакции
2СаSO3 +O2 =2СаSO4 ,
выводится в отвал транспортером 7 и может быть использован для производства строительных материалов. Известковый метод обеспечивает практически полную очистку газов от SO2 , но требует значительного расхода извести.
Содовый метод. Сущность этого метода заключается в промывке отходящих газов водными растворами кальцинированной соды. При этом протекают реакции
Na2 CO3 + SO2 = Na2 SO + СО2 ,
Na2 SO3 + SO2 + H2 O = 2 NaHSO3 .
Процесс поглощения SO2 содовым раствором осуществляется в аппаратах насадочного или барботажного типов. Газ проходит последовательно две башни, первая из которых орошается раствором NaHSO3 , вторая — раствором Na2 SO3 . Содовый способ обеспечивает хорошую очистку отходящих газов от SO2 с одновременным получением товарной соли NaHSO3 и Na2 SO3 . Однако он не нашел широкого применения ввиду ограниченного сбыта этих солей.
Аммиачный метод. Процесс очистки выхлопных газов от SOg аммиачным методом заключается в промывке газа аммиачной водой. При этом протекает реакция
SO2 + 2NH3 + H2 O = (NH4 )2 SO3 ;
(NH4 )2 SO3 + SO2 + H2 O = 2 NH4 HSO3 .
В присутствии кислорода сульфиты окисляются до сульфатов
(NH4 )2 SO3 + ½ O2 = (NH4 )2 SO4 ;
(NH4 )HSO3 + ½ O2 = NH4 HSO4.
Так как при взаимодействии сернистого газа с аммиачной водой получаются аммиачные соли, используемые как удобрение в сельском хозяйстве, аммиачный метод очистки газов от SO2 перспективен.
Циклические методы. В основе циклических методов лежит способность двуокиси серы поглощаться при низких температурах, а затем при повышении температуры выделяться в чистом виде. В некоторых случаях для абсорбции SO2 используются твердые сорбенты. Циклические методы извлечения двуокиси серы являются наиболее эффективными и нашли применение в промышленности.
Принципиальная схема извлечения и концентрирования SO2 циклическим методом показана на рис. 6. Охлажденный и очищенный от механических примесей газ поступает в абсорберы /, орошаемые поглотителем. Очищенный газ выбрасывается в атмосферу, а поглотительный раствор нагревается в теплообменнике 3
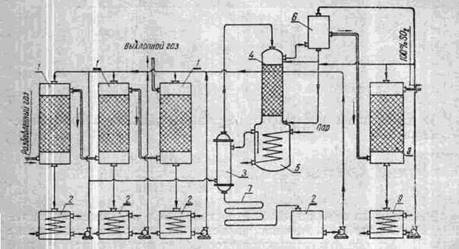
Рис. 6. Схема очистки газов от двуокиси серы циклическим методом.
и направляется в отгонную колонну 4, снабженную кипятильником 5. Смесь водяных паров с SO2 поступает в конденсатор 6, а затем в холодильную башню 8, орошаемую циркуляционной холодной водой (насыщенной SO2 ). Водяные пары конденсируются, а чистая двуокись серы извлекается из системы. Раствор охлаждают в холодильниках 7 и 9 и собирают в емкости 2.
Водный метод. Недостаток этого способа в том, что на регенерацию воды расходуется большое количество электроэнергии. Ввиду малой растворимости SO2 в воде поглотительная установка является громоздкой.
Аммиачный метод. Капитальные затраты на сооружение очистных сооружений могут быть снижены, если в качестве поглотителя использовать более абсорбционноемкие поглотители (водный раствор аммиака и др.).
Магнезитовый метод. Сущность процесса состоит в поглощении водной суспензии окиси магния
MgO + SO2 == MgSO3 .
При нагреве сульфит магния разлагается на
MgSO3 ® t =0 MgO + SO2 с получением товарного SO2 , а окись магния снова направляется на поглощение. Как и в случае аммиачного способа часть (до 10°/о) сульфита магния в растворе окисляется в сульфат
2MgSO3 + O2 = 2MgSO4 .