Реферат: Олово и его основные сплавы
снижает склонность к ликвации и повышает жидкотекучесть, поскольку он уменьшает температурный интервал кристаллизации сплавов;
способствует получению более плотного литья;
раскисляет расплав и уменьшает содержание в нем водорода;
улучшает прочностные свойства.
Из всех антифрикционных сплавов наилучшими свойствами обладают оловянные баббиты, в составе которых до 90% олова.
Мягкие и легкоплавкие свинцово-оловянные припои хорошо смачивают поверхность большинства металлов, обладают высокой пластичностью и сопротивлением усталости.
Однако область их применения ограничивается из-за недостаточной механической прочности самих припоев.
Составы оловянно-свинцовых припоев. Свойства оловянно-свинцовых припоев.
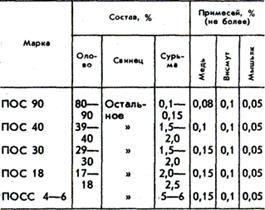
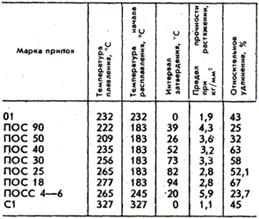
Припои имеют различное назначение, например: ПОС 90 - для паяния внутренних швов пищевой посуды (электрочайники, кастрюли и т.п.); ПОС 40 - паяние латуни, железа и медных проводов; ПОС 30 - паяние латуни, меди, железа цинковых и оцинкованных листов, белой жести, приборов, радиоаппаратуры, гибких шлангов и бандажной проволоки электромоторов.
Олово входит также в состав типографского сплава гарта, из-за чего гарт имеет низкую температуру плавления (240-350 °С) и хорошие литейные свойства.
Наконец, сплавы на основе олова очень нужны электротехнике. Важнейший материал для электроконденсаторов - станиоль; это почти чистое олово, превращенное в тонкие листы (доля других металлов в станиоле не превышает 5%).
Тот факт, что олово образует довольно многочисленные сплавы такого рода, заставляет критически отнестись к утверждению, что лишь 7% производимого в мире олова расходуется в виде химических соединений ("Краткая химическая энциклопедия", т.3, с.739). Видимо, речь здесь идет только о соединениях с неметаллами.
Соединения с неметаллами. Из этих веществ наибольшее значение имеют хлориды. В тетрахлориде олова SnCl4 растворяются иод, фосфор, сера, многие органические вещества. Поэтому и используют его главным образом как весьма специфический растворитель. Дихлорид олова SnCl2 применяют как протраву при крашении и как восстановитель при синтезе органических красителей. Те же функции в текстильном производстве еще у одного соединения элемента №50 - станната натрия Na2SnO3. Кроме того, с его помощью утяжеляют шелк.
Промышленность ограниченно использует и окислы олова. SnO применяют для получения рубинового стекла, a SnO2 - белой глазури. Золотисто-желтые кристаллы дисульфида олова SnS2 нередко называют сусальным золотом, которым "золотят" дерево, гипс. Это, если можно так выразиться, самое "антисовременное" применение соединений олова. А самое современное?
Если иметь в виду только соединения олова, то это применение станната бария BaSnO3 в радиотехнике в качестве превосходного диэлектрика. А один из изотопов олова, 119Sn, сыграл заметную роль при изучении эффекта Мессбауэра - явления, благодаря которому был создан новый метод исследования - гамма-резонансная спектроскопия. И это не единственный случай, когда древний металл сослужил службу современной науке.
На примере серого олова - одной из модификаций элемента №50 - была выявлена связь между свойствами и химической природой полупроводникового материала. И это, видимо, единственное, за что серое олово можно помянуть добрым словом: вреда оно принесло больше, тем пользы. Мы еще вернемся к этой разновидности элемента №50 после рассказа о еще одной большой и важной группе соединений олова.
Оловоорганика. Элементоорганических соединений, в состав которых входит олово, известно великое множество. Первое из них получено еще в 1852 г.
Сначала вещества этого класса получали лишь одним способом - в обменной реакции между неорганическими соединениями олова и реактивами Гриньяра. Вот пример такой реакции:
SnCl4 + 4RMgX SnR4 + 4MgXCl
(R здесь - углеводородный радикал, X - галоген).
Соединения состава SnR4 широкого практического применения не нашли.
Впервые интерес к оловоорганике возник в годы первой мировой войны. Почти все органические соединения олова, полученные к тому времени, были токсичны. В качестве отравляющих веществ эти соединения не были использованы, их токсичностью для насекомых, плесневых грибков, вредных микробов воспользовались позже. На основе ацетата трифенилолова (C6H5) 3SnOOCCH3 был создан эффективный препарат для борьбы с грибковыми заболеваниями картофеля и сахарной свеклы. У этого препарата оказалось еще одно полезное свойство: он стимулировал рост и развитие растений.
Для борьбы с грибками, развивающимися в аппаратах целлюлозно-бумажной промышленности, применяют другое вещество - гидроокись трибутилолова (С4Н9) 3SnOH. Это намного повышает производительность аппаратуры.
Много "профессий" у дилаурината дибутилолова (C4H9) 2Sn (OCOC11H23) 2. Его используют в ветеринарной практике как средство против гельминтов (глистов). Это же вещество широко применяют в химической промышленности как стабилизатор поливинилхлорида и других полимерных материалов и как катализатор. Скорость реакции образования уретанов (мономеры полиуретановых каучуков) в присутствии такого катализатора возрастает в 37 тыс. раз.
На основе оловоорганических соединений созданы эффективные инсектициды; оловоорганические стекла надежно защищают от рентгеновского облучения, полимерными свинец - и оловоорганическими красками покрывают подводные части кораблей, чтобы на них не нарастали моллюски.
Все это соединения четырехвалентного олова. Органические соединения двухвалентного олова, напротив, немногочисленны и практического применения пока почти не находят.
Серое олово. Как и многие другие элементы, олово имеет несколько аллотропических модификаций, несколько состояний. (Слово "аллотропия" переводится с греческого как "другое свойство", "другой поворот") При нормальной плюсовой температуре олово выглядит так, что никто не может усомниться в принадлежности его к классу металлов.
Белый металл, пластичный, ковкий. Кристаллы белого олова (его называют еще бета-оловом) тетрагональные. Длина ребер элементарной кристаллической решетки - 5,82 и 3,18. Но при температуре ниже 13,2°C "нормальное" состояние олова иное. Едва достигнут этот температурный порог, в кристаллической структуре оловянного слитка начинается перестройка. Белое олово превращается в порошкообразное серое, или альфа-олово, и чем ниже температура, тем больше скорость этого превращения. Максимума она достигает при минус 39°C.