Реферат: Основы физики атмосферы
Поскольку парциальное давление водяного пара, как правило, не превышает 30-50 мбар, оно мало по сравнению с давлением
воздуха (~ 1 бар). Учитывая малость отношения — <С 1, можно переписать уравнение состояние влажного воздуха в виде
![]()
Сравнивая (13.2) и (13.3), нетрудно видеть, что присутствие водяных паров дает лишь небольшую поправку к уравнению состояния, которую можно интерпретировать как сдвиг температуры. Иногда вводится так называемая виртуальная температура, т. е. для воздуха с водяным паром можно заменить уравнение состояния (13.3) соотношением вида (13.2) с другой — виртуальной температурой. Иными словами, это температура сухого воздуха, имеющего такое же давление как влажный воздух. Виртуальная температура будет несколько больше, потому что молекулярный вес пара меньше. Если происходит добавление пара с замещением молекул воздуха, то смесь становится легче и плотность падает. А для того чтобы сухой воздух имел такую же плотность, нужно поднять его температуру, тогда его плотность уменьшится. Как упоминалось выше, давление водяных паров невелико, поэтому в ряде задач без фазовых переходов влиянием водяного пара на уравнение состояния можно пренебречь.
Переход фазовый (ф.п.)- термодинамический процесс перехода вещества из одной фазы в другую;
первого рода - фазовый переход, при котором претерпевают скачки первые производные от химического потенциала (S и V );
второго рода - фазовый переход, при котором первые производные от химического потенциала непрерывны, но претерпевают скачки его вторые производные (cP , ![]() ,
, ![]() T );
T );
монотропный - односторонний ф.п., при котором переход от высокотемпературной модификации к низкотемпературной невозможен, тогда как обратный процесс осуществляется и протекает тем быстрее, чем выше температура;
энантиотропный - взаимные превращения двух кристаллических модификаций, которые могут самопроизвольно протекать как в прямом так и в обратном направлениях в зависимости от условий.
Правило фаз Гиббса - в равновесной термодинамической системе , на которую из внешних факторов оказывают влияние только 2 фактора - температура и давление (соответствуют слагаемому "2" в ур-нии), число степеней свободы (C) равно числу независимых компонентов (K) минус число фаз (Ф) плюс два: С = К - Ф + 2. Если Ф = 0, система инвариантна, Ф = 1 - моновариантна, Ф = 2- бивариантна и т.д.
Уравнение Клапейрона-Клаузиуса для фазовых превращений ![]()
равновесие "кристалл" ![]() жидкость":
жидкость": ![]()
равновесие "жидкость"![]() пар":
пар": ![]() ,
,
если насыщенный пар подчиняется ур-нию состояния идеального газа , то
при испарении ![]() ;
;![]() , при возгонке
, при возгонке ![]() ;
;![]() .
.
В интегральном виде 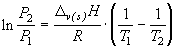
Термодинамические процессы в атмосфере
В атмосфере происходят различные термодинамические процессы, в частности, изотермические, адиабатические и другие знакомые по курсу молекулярной физики процессы. В основном атмосфера неизотермична, например, в тропосфере температура меняется с высотой довольно сильно, примерно на 6,5 °С на км. Но в областях тропопаузы, стратопаузы, мезопаузы в некоторых диапазонах высот ее приближенно можно считать изотермичной.
Как известно, распределение давления и плотности в изотермической атмосфере определяется формулой Больцмана. Разность давлений в слоистой и статичной атмосфере обусловлена весом выделенного объема воздуха:
![]()
Ось z направлена вверх. Если заменить р выражением, полученным из уравнения состояния (13.2), то получим уравнение
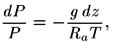
откуда после интегрирования следует формула Больцмана
![]()
где ![]() — так называемая высота однородной атмосферы.
— так называемая высота однородной атмосферы.
В соответствии с формулой Больцмана давление с высотой меняется экспоненциально, причем Н определяет масштаб спадания давления по высоте, т. е. на высоте Н давление падает в е раз. Формула для плотности будет аналогичной, потому что при постоянной температуре плотность пропорциональна давлению. Высоту однородной атмосферы можно выразить и через массу т одной молекулы:
![]()
Численная оценка дает величину около 8 км:
![]()