Реферат: Реакция альдольно-кротоновой конденсации, и ее оптимизация
При получении нитростиролов следует брать 1 моль щелочи, вести реакцию в течение 0.5 ч и после этого вылить реакционную смесь в двойное молярное количество 20%-ной соляной кислоты.
II Постановка задачи.
В рамках фундаментального исследований, проводящихся в ИОХ РАН, необходимо было осуществить синтез ряда продуктов альдольно-кротоновой конденсации: ароматических альдегидов (в качестве карбонильных компонентов) с метилалкил- и метиларилкетонами (в качестве метиленовых компонентов).
В нашу задачу также входила оптимизация методики синтеза соединений данного типа. В качестве основного приема оптимизации мы запланировали проведение реакции конденсации в насыщенном водно-спиртовом растворе исходных веществ с добавлением водного раствора щелочи. (Согласно основной литературной методике реакцию проводят в спиртовом растворе [1]) Поскольку продукты конденсации, как правило, существенно хуже растворимы, чем исходные вещества мы рассчитываем, что целевые продукты будут выделяться в виде осадка; т.е. уходить из сферы реакции, что ,по-нашему мнению, может ослабить процессы более глубокой конденсации и привести к упрощению методики выделения продуктов реакции.
Мы полагали, что особенно актуальной может оказаться такая оптимизация для синтеза соединений, содержащих 2 метиленовых компонента (например, ацетон  ), чтобы свести к минимуму образование продуктов бис-конденсации.
), чтобы свести к минимуму образование продуктов бис-конденсации.
III Обсуждение результатов.
Мы осуществили синтез 15 продуктов альдольно-кротоновой конденсации. Структура и чистота которых подтверждена методом ПМР-спектроскопии. Благодаря оптимизации методики были получены чистые вещества, выделение которых из реакционной смеси стало более простым по сравнению с выделением продуктов, по литературной методике. В частности, в большинстве случаев удалось избежать необходимости перекристаллизацию.
В результате реакции альдольно-кротоновой конденсации получены ожидаемые продукты с выходом ‑ 50-90%.
Так же мы получили практически чистый продукт моно-конденсации при реакции анисового альдегида с ацетоном.
IV Выводы.
1) Осуществили синтез 15 целевых продуктов количество. Структура подтверждена данными ПМР спектров.
2) Адаптирована и оптимизирована применительно к синтезу целевых продуктов литературная методика.
V Экспериментальная часть.
Осуществили синтез следующих продуктов:
| № | Формула | tпл o |
| 1 |
| 150-152 |
| 2 |
| 65-68 |
| 3 |
| 90-91 |
| 4 |
| 77-79 |
| 5 |
| 98-100 |
| 6 |
| 106-107 |
| 7 |
| 124-125 |
| 8 |
| 65-67 |
| 9 |
| 202-205 |
| 10 |
| 177-180 |
| 11 |
| 145-146 |
| 12 |
| 148-150 |
| 13 |
| 143-153 |
| 14 |
| 99-100 |
| 15 |
| 95-97 |
VI Спектры.

| Хим. Сдвиг | Константа спин-спинового расщепления | |
| CH3 | 721.94 | |
| H5 | 1984.22 | 1.34 |
| H6 | 1987.58 | 1.34 |
| H7 | 2200.86 | 8.05 |
| 2262.57 | 6.04 | |
| 2321.59 | 1.35 | |
| H6 | 2390.01 | 8.05 |

| Хим. Сдвиг | Константа спин-спинового расщепления | |
| H5 H6 | 1.01 | 0.0112 0.0134 0.01343 0.0906 0.1587 0.16 |
| H7 | 2.21 | 0.0156 0.0112 0.0134 0.0156 |
| H3 | 6.94 | 0.0537 |
| 7.58 | 0.0536 | |
| 7.69 | 0.0274 | |
| 8.23 | 0.029 |

| Хим. Сдвиг | Константа спин-спинового расщепления |
| 273.78 | 4.01 3.35 4.02 3.36 4.02 |
| 281.16 | |
| 339.51 | |
| 654.08 | |
| 2020.33 | |
| 2068.62 | |
| 2249.03 | |
| 2266.48 |
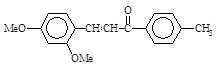
| Хим. Сдвиг | Константа спин-спинового расщепления |
| 721.27 | |
| 1158.57 | |
| 1182.72 | |
| 1974.89 | 2.63 6.03 2.01 3.36 2.01 |
| 2195.50 | 8.05 |
| 2304.83 | 15.42 |
| 2328.47 | 9.22 |
| 2394.70 | 8.05 |
| 2416.34 | 16.59 |

|
Хим. сдвиг |
Константа спин-спинового расщепления |
|
2069.83 |
8.73 6.7 6.39 |
|
2268.36 |
8.72 |
|
2332.69 |
5.43 |
|
2402.52 |
8.7 |
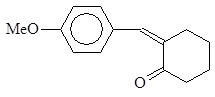
| Хим. Сдвиг | Константа спин-спинового расщепления |
| 741.18 | 12.65 6.76 |
| 841.75 | 2.01 4.7 1.34 |
| 854.49 | 2.01 9.39 5.37 5.37 |
| 1148.94 | |
| 2069.16 | 4.79 3.26 5.36 |
| 2212.02 | 8.72 7.38 8.72 12.74 |
| 2328.73 |
Общая методика
К эквимолярной смеси реагирующих веществ добавляли некоторое количество Н2 О, а затем, при перемешивании, этилового спирта до образования гомогенной смеси (раствора). Далее прибавляли концентрированный раствор щелочи ( ~ от исходного количества реагирующих веществ) и оставляли реакционную смесь при комнатной температуре до полного исчезновения исходных веществ (по данным ТСХ). Выкристаллизовавшийся продукт отфильтровывали и промывали спиртом. Если выделялось масло, то его отделяли, промывали водой и вызывали кристаллизацию. При необходимости закристаллизовавшееся масло подвергали перекристаллизации.
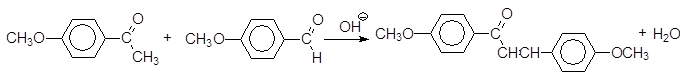
В колбу объемом 50мл поместить 2.000 г альдегида и эквимолярное количество кетона. Добавить 20 мл воды и при перемешивании долить 25 мл этилового спирта, затем долить 1 мл 8 М раствора КОН. Реакционную массу оставить при комнатной температуре с перемешиванием. Через 3 ч. Выделившиеся кристаллы отфильтровать и промыть большим количеством воду и небольшим спирта. Выход 74,07%.
Список литературы.
“Органикум” т.1 издательство “Мир” 1992 - 488 с.
“Органикум” т.2 издательство “Мир” 1992 - 472 с.
“Механизмы реакций в органической химии” Б.Сайкс издание 4-е. Москва “Химия” 1991 г
“Органическая химия” Ю.С.Шабаров Москва “Химия” 1994 г.
“Курс органической химии” А.П.Писаренко издание 3-е. Москва “Высшая школа” 1975 г.


