Реферат: Типы материальных систем, их связь и соотношение
Атомистическая гипотеза строения материи, выдвинутая в античностиДемокритом, была возрождена в XVIII в. химиком Дж.Дальтоном, который принял атомный вес водорода за единицу и сопоставил с ним атомные веса других газов. Благодаря трудам Дж. Дальтона стали изучаться физико-химические свойства атома.
В физику представления об атомах как о последних неделимых структурных элементах материи пришли из химии. Собственно физические исследования атома начинаются в конце XIX в., когда французским физикомА.Беккерелем было открыто явление радиоактивности, которое заключалось в самопроизвольном превращении атомов одних элементов в атомы других элементов.
Понятие «Микромир» охватывает фундаментальные и элементарные частицы, ядра, атомы и молекулы.
Элементарные частицы – это частицы, входящие в состав прежде «неделимого» атома. К ним относят также и те частицы, которые получают при помощи мощных ускорителей частиц. Есть элементарные частицы, которые возникают при прохождении через атмосферу космических лучей, они существуют миллионные доли секунды, затем распадаются, превращаются в другие элементарные частицы или испускают энергию в форме излучения. К наиболее известным элементарным частицам относятся электрон, фотон, пи-мезон, мюон, нейтрино. В строгом смысле слова элементарные частицы не должны содержать в себе какие-либо другие частицы. Однако далеко не все из наиболее известных элементарных частиц удовлетворяют этому требованию. Было обнаружено, что элементарные частицы могут взаимно превращаться, т.е. не являются «последними кирпичиками» мироздания. В настоящее время уже известны сотни элементарных частиц, хотя согласно теории их число не должно быть особенно большим. Новейшие исследования, в частности, подтверждают выдвинутую ранее гипотезу о существовании еще «более элементарных» частиц – кварков.
Первой элементарной частицей, открытой в физике, стал электрон, который в 1897 году, изучая газовые разряды открыл английский физик Джозеф Томсон и измерил отношение его заряда к массе: поскольку электроны имеют отрицательный заряд, а атом в целом электрически нейтрален, то было сделано предположение о наличии помимо электрона и положительно заряженной частицы. Электрон — один из основных структурных элементов вещества; электронные оболочки атомов определяют оптические, электрические, магнитные и химические свойства атомов и молекул, а также большинство свойств твердых тел.
В обычном употреблении физики называют элементарными такие частицы, которые не являются атомами и атомными ядрами, за исключением протона и нейтрона. После установления сложной структуры многих элементарных частиц потребовалось ввести новое понятие – фундаментальные частицы,под которыми понимаются микрочастицы, внутреннюю структуру которой нельзя представить в виде объединения других свободной частиц.
Во всех взаимодействиях элементарные частицы ведут себя как единое целое. Характеристиками элементарных частиц являются, кроме массы покоя, электрического заряда, спина, также такие специфические характеристики (квантовые числа), как барионный заряд, лептонный заряд, гиперзаряд, странность и т.п.
В настоящее время достаточно много известно об атомарном строении вещества и элементарных частицах. Поскольку элементарные частицы способны к взаимным превращениям, это не позволяет рассматривать их, так же как и атом, в качестве простейших, неизменных «кирпичиков мироздания». Число элементарных частиц очень велико. Всего открыто более 350 элементарных частиц, из которых стабильны лишь фотон, электронное и мюонное нейтрино, электрон, протон и их античастицы (каждая элементарная частица, за исключением абсолютно нейтральных, имеет свою античастицу). Остальные элементарные частицы самопроизвольно распадаются за время от 103 с (свободный нейтрон) до 10-22 - 10-24 с (резонансы).
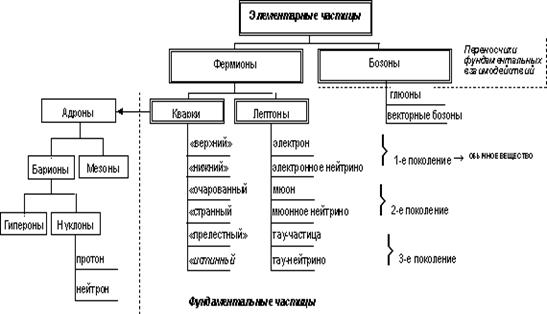
Существует несколько групп элементарных частиц, различающихся по своим свойствам и характеру взаимодействия, которые принято делить на две большие группы: фермионы и бозоны (см. рисунок).
Согласно современным представлениям, структура элементарных частиц описывается посредством непрерывно возникающих и снова распадающихся «виртуальных» частиц . Например, мезон строится из виртуального нуклона и антинуклона, которые в процессе аннигиляции (лат. annihilatio , букв. уничтожение) непрерывно исчезают, а затем образуются снова.
Формальное привлечение виртуальных частиц означает, что внутреннюю структуру элементарных частиц невозможно описать через другие частицы.
Удовлетворительной теории происхождения и структуры элементарных частиц пока нет. Многие ученые считают, что такую теорию можно создать только при учете космологических обстоятельств. Большое значение имеет исследование рождения элементарных частиц из вакуума в сильных гравитационных и электромагнитных полях, поскольку здесь устанавливается связь микро- и мегамиров. Фундаментальные взаимодействия во Вселенной, в мегамире определяют структуру элементарных частиц и их превращения. Очевидно, потребуется выработка новых понятий для адекватного описания структуры материального мира.
Атомом (от греч. atomos - неделимый) называют часть вещества микроскопических размеров и массы, мельчайшую частицу химического элемента, сохраняющую его свойства. Атомы состоят из элементарных частиц и имеют сложную внутреннюю структуру, представляя собой целостную ядерно-электронную систему. В центре атома находится положительно заряженное ядро, в котором сосредоточена почти вся масса атома; вокруг движутся электроны, образующие электронные оболочки, размеры которых (~10-8 см) определяют размеры атома. Ядро атома состоит из протонов и нейтронов. Число электронов в атоме равно числу протонов в ядре (заряд всех электронов атома равен заряду ядра), число протонов равно порядковому номеру элемента в периодической системе. Атомы могут присоединять или отдавать электроны, становясь отрицательно или положительно заряженными ионами. Химические свойства атомов определяются в основном числом электронов во внешней оболочке; соединяясь химически, атомы образуют молекулы.
Важная характеристика атома — его внутренняя энергия, которая может принимать лишь определенные (дискретные) значения, соответствующие устойчивым состояниям атома, и изменяется только скачкообразно путем квантового перехода. Поглощая определенную порцию энергии, атом переходит в возбужденное состояние (на более высокий уровень энергии). Из возбужденного состояния атом, испуская фотон, может перейти в состояние с меньшей энергией (на более низкий уровень энергии). Уровень, соответствующий минимальной энергии атома, называется основным, остальные — возбужденными. Квантовые переходы обусловливают атомные спектры поглощения и испускания, индивидуальные для атомов всех химических элементов.
Подядром атома понимается его центральная часть, в которой сосредоточена практически вся масса атома и весь его положительный заряд. Ядро состоит из нуклонов – протонов и нейтронов (обозначение p и n). Масса протона mP = 1,673×10-27 =1,836me , mn = 1,675×10-27 = 1835,5me . Масса ядра не равна сумме масс протонов и нейтронов, входящих в него (т.н. «дефект масс»). Протон несет элементарный положительный заряд, нейтрон – частица незаряженная. Число электронов в атоме равно порядковому номеру Z элемента в таблице Менделеева, а число протонов, поскольку в целом атом нейтрален, равно числу электронов. Тогда число нейтронов в ядре определяется следующим образом: NP = A – Z , где А – массовое число, т.е. целое число, ближайшее к атомной массе элемента в таблице Менделеева, Z – зарядовое число (число протонов).
Для обозначения ядер применяется запись Z XA , где Х – символ химического элемента в таблице Менделеева. Ядра с одинаковыми Z, но разными А называются изотопами. Сейчас известно более 300 устойчивых и более 1000 неустойчивых изотопов. С неустойчивыми изотопами связано явление радиоактивности – ядерного распада.
Ядро в целом – устойчивая система, для его разрушения необходимо затратить энергию. Эта энергия называется энергией связи ядра . Энергия связи, приходящаяся на один нуклон, называется удельной энергией связи . Нуклоны в ядре удерживаются ядерными силами, представляющими сильное взаимодействие и имеют обменный характер . Ядерные силы обладают рядом свойств:
1. Ядерные силы являются короткодействующими (радиус действия порядка 10-15 м) На этих расстояниях они значительно превышают кулоновские силы отталкивания протонов. При значительном уменьшении расстояния притяжение нуклонов сменяется отталкиванием.
2. Ядерные силы обладают зарядовой независимостью, т.е. действуют как между заряженными, так и между нейтральными частицами.
3. Ядерные силы обладают свойствами насыщения. Это означает, что каждый нуклон в ядре взаимодействует лишь с ограниченным числом ближайших к нему нуклонов.
4. Ядерные силы не являются центральными. Их величина зависит от ориентации спинов частиц.
Молекулы — это очередной после атомов качественный уровень строения и эволюции вещества. Молекула – микрочастица, образованная из атомов и способная к самостоятельному существованию, обладающая его главными химическими свойствами. Имеет постоянный состав входящих в нее атомных ядер и фиксированное число электронов и обладает совокупностью свойств, позволяющих отличать молекулы одного вида от молекул другого. Число атомов в молекуле может быть различным: от двух до сотен тысяч.
Молекулы простых веществ состоят из одинаковых атомов, сложных – из разных атомов. Существует большое количество соединений, молекулы которых состоят из многих тысяч атомов - макромолекулы.
Подчеркивая целостность молекул, органическое единство их составных частей, современное естествознание характеризует движение молекул как движение самостоятельных и целостных систем, а не как простую сумму разрозненных движений отдельных образующих их частиц (атомов, ядер и электронов). Те взаимодействия молекул, которые не сопровождаются изменением их структуры, изучаются физикой и называются физическими. Взаимодействия же молекул, приводящие к их качественным взаимопревращениям, перестройке их внутренних связей, называются химическими и изучаются химией.
3. Макромир
В истории изучения природы выделяют два этапа - донаучный и научный.
Донаучный, илинатурфилософский, охватывает период от античности до становления экспериментального естествознания в XVI—XVII вв. В этот период учения о природе носили чисто натурфилософский характер: наблюдаемые природные явления объяснялись на основе умозрительных философских принципов.
Наиболее значимой для последующего развития естественных наук была концепция дискретного строения материи атомизм, согласно которому все тела состоят из атомов — мельчайших в мире частиц. Поскольку современные научные представления о структурных уровнях организации материи были выработаны в ходе критического переосмысления представлений классической науки, применимых только к объектам макроуровня, то начинать исследование нужно с концепций классической физики.