Реферат: Золь-гель метод
Наиболее распространенным способом получения дисперсных осадков оксидов металлов, в том числе и ТiO2, является осаждение из растворов соответствующих солей аммиаком, щелочами и карбонатами щелочных металлов. Многочисленные исследования показали, что минимальный размер первичных частиц не зависит от природы осадителя и составляет 45 ± 10 А. В зависимости от условий проведения синтеза первичные частицы срастаются в агрегаты различных размеров. Степень агрегации зависит от многих факторов и регулируется условиями синтеза. При варьировании температуры, продолжительности синтеза и рН среды можно получать диоксид титана в различном фазовом состоянии: аморфный ТiO2, анатаз, брукит или рутил.[3, 943]
В настоящем обзоре обобщены исследования по синтезу наноразмерного диоксида титана, регулированию и стабилизации дисперсности, морфологии и фазового состава наночастиц ТiO2, а также рассмотрены перспективы их использования в нанобиотехнологии.
золь гель наночастица титан
Влияние условий синтеза на дисперсность, фазовый состав и свойства диоксида титана
По данным ранних исследований, обзор которых можно найти в книге, при проведении гидролиза различных соединений титана (алкоксидов и неорганических солей титана, главным образом TiCl4) в водных растворах первичными продуктами при низких значениях рН (2-6) являются основные соли переменного состава. При более высоких значениях рН образуются гидратированные формы диоксида титана, которым приписывают формулу Тi(ОН)2 или ТiO2*nH2O, где п зависит от условий старения и сушки.
Свежеосажденный гидратированный диоксид титана(4) обладает большой адсорбционной способностью по отношению как к катионам, так и к анионам; содержание и природа примесей в ТiO2 зависят от рН среды при осаждении, природы осадителя и исходного соединения титана. По данным просвечивающей электронной микроскопии (ПЭМ), гель представляет собой сферические непористые частицы размером 30-60 А, агрегирующиеся в цепи или гроздья. Удельная поверхность геля (S), колеблется от 250 до 500 м2 -г-1 и зависит от условий осаждения и наличия примесей.
При проведении гидролиза в гидротермальных условиях удельная поверхность образующегося гидратированного диоксида титана также существенно зависит от температуры и продолжительности процесса. По данным авторов работы, на степень кристаллизации продукта гидротермального гидролиза оказывает существенное влияние исходная концентрация TiCl4, которая определяет кислотность реакционной среды.
Продемонстрирован простой и доступный метод получения чистого и стабильного наноразмерного ТiO2(анатаза) в мягких гидротермальных условиях при использовании в качестве предшественника TiCl4. Проведение сольвотер-мального гидролиза этоксида титана в безводном этаноле с добавлением строго определенного количества ультрачистой воды в мягких условиях (< 200°С, 2 ч) также приводит к чистому ультратонкодисперсному нанокристаллическому анатазу с высокой удельной поверхностью (до 250 м2 -г-1 ).
При термической обработке гелей гидратированных форм диоксида титана происходит их кристаллизация с образованием безводного ТiO2. В зависимости от температуры прокаливания возможны полиморфные превращения гидратированного ТiO2 в анатаз, рутил или брукит, сопровождающиеся изменением удельной поверхности и пористой структуры. Так, по данным исследования, при температурах ниже 600°С идет процесс кристаллизации с образованием анатаза практически при неизменных значениях объема пор и удельной поверхности. При более высоких температурах наблюдается переход анатаза в рутил, сопровождающийся резким уменьшением и объема пор, и удельной поверхности. На температуру полиморфного превращения также большое влияние могут оказывать минеральные примеси. Многочисленными данными показано, что помимо фазового состава условия термической обработки гелей ТiO2 определяют и другие важные эксплуатационные характеристики диоксида титана — морфологию и размер частиц.
Наиболее распространенными способами получения ТiO2 являются сульфатный (из ильменита) и хлоридный (из TiCI4), причем переработка тетрахлорида титана проводится по трем разным схемам: гидротермальный гидролиз, парофазный гидролиз или сжигание в токе кислорода. В последнее время все большее значение приобретает золь-гель-метод, который позволяет получать наноразмерные частицы ТiO2 с заданными структурой и свойствами и, следовательно, представляет интерес с точки зрения развития нанотехнологий.[3, 944] Титансодержащими предшественниками в золь-гель-методе служат алкоксиды титана или тетрахлорид титана.
В следующих разделах рассмотрены работы, в которых достигнуты наиболее значимые результаты с точки зрения регулирования дисперсности, морфологии, фазового состава и стабильности наноразмерного ТiO2 .
Синтез наноразмерного Т iO 2 из алкоксидов титана, исследование дисперсности и фазового состава
Для синтеза ТiO2 из алкоксидов титана наиболее предпочтительны тетраизопропоксид (далее изопропоксид) титана и тетрабутоксид (далее бутоксид) титана.
Коллоидные растворы ТiO2, различающиеся размером частиц и устойчивостью, были получены из Ti(OPri )4, модифицированного ацетилацетоном, при использовании органических растворителей различной полярности и с разным молярным объемом. По данным рентгенофазового анализа (РФА), независимо от природы используемого при гидролизе органического растворителя все свежеприготовленные золи, полученные с добавлением или без добавления ацетилацетона, содержат аморфный ТiO2, который превращается в нанокристаллическую фазу анатаза при нагревании до 450°С. Однако использование растворителей с малым молярным объемом и модифицирование предшественника ацетилацетоном приводят к стабилизации коллоидного раствора ТiO2, что и является основным результатом цитируемой работы. Методом ИК-спектроскопии показано образование хелатного комплекса между изопропоксидом титана и ацетилацетоном (рис. 6), что, по мнению авторов, приводит к замедлению гидролиза и конденсации и, следовательно, к уменьшению степени агломерации частиц ТiO2, а влияние растворителя на размер агрегатов (рис. 7) объяснено с точки зрения параметров растворимости Хансена. Установлены параметры растворимости Хансена для ТiO2, полученного в различных растворителях в присутствии ацетилацетона, которые могут быть полезны при синтезе стабильного коллоидного ТiO2.
Данные о размере частиц ТiO2 в коллоидных растворах и степени их агрегации в сухих порошках получены с помощью методов светового рассеяния, сканирующей электронной микроскопии (СЭМ) и ПЭМ.
Изопропоксид титана, диэтаноламин (ДЭА) и этанол (в соотношении 3:1:20 по объему) были использованы в качестве исходных реагентов для получения золя ТiO2 При этом важен порядок смешения компонентов, так как введение EtOH перед добавлением ДЭА приводит к очень быстрому осаждению ТiO2, что обусловлено высокой реакционной способностью алкоксида в этаноле. Поэтому сначала смешивают половину объема спирта с ДЭА, затем добавляют изопропоксид титана, перемешивают в течение 30 мин и только после этого добавляют остальное количество ЕtOН, полученную смесь интенсивно перемешивают при комнатной температуре. Золь стабилен в течение недели, после чего переходит в гель. Отмечено, что при уменьшении времени перемешивания золя наблюдается значительное увеличение его стабильности. Стабильность золя также существенно возрастает в условиях низкой влажности. В ходе высушивания образуется ксерогель, который существенно «усаживается» по сравнению с исходным гелем (происходит уменьшение объема в 5- 10 раз).
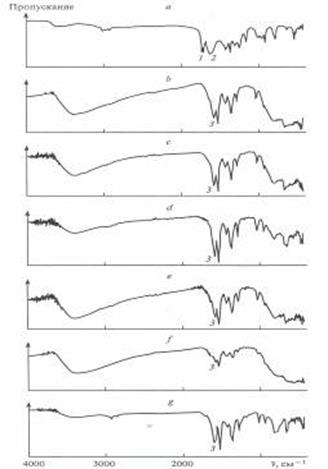
Рис. 6. ИК-Спектры ацетилацетона (а) и золей диоксида титана, полученных в присутствии ацетилацетона в различных органических растворителях: в ТГФ (b), ацетоне (с), бутаноле (d), хлороформе (e), толуоле (f), гексане (g). 1 — пик группы С=0 кето-формы, 2 — пик группы С = 0 енольной формы, 3 — пик группы С=0 хелатного комплекса.
Фаза чистого анатаза с размером частиц 10-20 нм может быть получена в результате очень простого низкотемпературного (100°С) синтеза в автоклаве с использованием лишь воды в качестве среды и изопропоксида титана как предшественника (без добавок). Размер, форма и фазовый состав частиц изучены методами РФА и ПЭМ.
В работе исследованы наночастицы ТiO2, полученные гидролизом Ti(OPri )4 при различных значениях рН среды. Для дальнейшего приготовления нанопорошка с узким распределением частиц по размерам была применена пептизация конечной суспензии. Отмечено влияние рН на размер и морфологию частиц нанопорошков. По данным РФА, СЭМи ПЭМ, свежеприготовленные порошки полностью состояли из кристаллической фазы анатаза. Лишь порошок, полученный из сильнокислого раствора, состоял из мелких аморфных сферических частиц.[3,945] Показано, что переход анатаза в рутил происходит при температурах ниже 600°С.
В исследовании для приготовления коллоидного раствора TiO2 использованы изопропоксид титана и смесь изопропилового спирта с соляной кислотой. В результате гидролиза изопропоксида получался коллоидный раствор ТЮ2 с концентрацией 0.9 моль *л -1 .
Авторы работы для получения наноструктурных пленок готовили золь TiO2 из изопропоксида титана и смеси этанола с соляной кислотой (молярное соотношение Тi(OPri )4 : НС1: EtOH : Н2 0 = 1:1.1:10 :10) с последующим добавлением раствора метилцеллюлозы (МЦ). Показано, что при увеличении содержания воды и разбавлении золя гелеобразование замедляется.
Из золей диоксида титана прокаливанием получали нано-порошок TiO2 , из которого готовили гомогенные суспензии, необходимые для создания пленок. Стабильность суспензий TiO2 была исследована по скорости седиментации. Варьировалась концентрация нанопорошка анатаза в жидкой среде (5-10 мас.%) с добавлением и без добавления МЦ. Показано, что скорость оседания нанопорошка ТiO2 резко уменьшается в присутствии МЦ. Так, в 5- и 10%-ной суспензиях без добавления МЦ оседание происходит в течение 1 ч и 30 мин соответственно, в присутствии МЦ 5%-ная суспензия устойчива в течение 3 сут, а 10%-ная — в течение 10 ч. Таким образом, МЦ выступает в качестве диспергирующего агента. Данные СЭМ свидетельствуют о заметном улучшении гомогенности и однородности пленок ТiO2 и увеличении их удельной поверхности в присутствии МЦ .
Синтез наноразмерного Ti02 золь-гель-методом на основе изопропоксида титана может быть проведен в присутствии другой добавки — пептида поли-L-лизина (PLL).В этом случае пептид является не только диспергирующей, но и структуроопределяющей добавкой: лишь в присутствии PLL образуются частицы TiO2 трубчатой формы (рис.8,a). Такая форма частиц сохраняется и после прокаливания при 700°С (рис.8,b). Прокаливание при той же температуре образца, полученного без пептида PLL, приводит к диоксиду титана с нерегулярной структурой (рис.9). По данным РФА, диоксид титана, полученный в присутствии PLL и прокаленный при 700°С, представляет собой анатаз с примесью рутила. На микрофотографиях, сделанных методом ПЭМ, наночастицы с дифракционной картиной анатаза проявляются в виде спаренных трубок диаметром около 20 нм с Y-образным сцеплением в нижней части или в форме наностержней диаметром от 10 до 25 нм. [3,946] Материалы на основе наноразмерного ТiO2 с трубчатой структурой могут быть успешно использованы в медицине, биотехнологии, микроэлектронике, оптике и др.[3, 947]

Рис. 7. СЭМ-Микрофотографии золей диоксида титана, полученных в присутствии ацетилацетона в среде ацетона (а), бута-нола (6), толуола (c,e) и гексана (d,f)Снимки e и fполучены при большем увеличении.

Рис.8. СЭМ-Микрофотографии ТiO2 , полученного в присутствии поли-L-лизина. a— свежеприготовленный образец, b— образец после прокаливания при 700°С.
