Статья: Масс-спектрометрическая оценка уровня включения дейтерия и углерода-13 в молекулы аминокислот бактериальных объектов
Московская государственная академия тонкой химической технологии им. М.В. Ломоносова, 117571, г. Москва, просп. Вернадского, д.86
Методом высокочувствительной масс-спектрометрии электронного удара исследованы уровни включения стабильных изотопов дейтерия 2 H и углерода-13 13 С в молекулы секретируемых аминокислот L -фенилаланинпродуцирующего штамма Brevibacterium methylicum и L -лейцинпродуцирующего штамма Methylobacillus flagellatum и аминокислотные остатки суммарных белков биомассы при выращивании бактерий на средах, содержащих в качестве источников стабильных изотопов (2 Н)метанол, (13 С)метанол и 2 Н2 О. Также осуществлено включение L -[2,3,4,5,6-2 Н]фенилаланина, L -[3,5-2 Н]тирозина и L -[2,4,5,6,7-2 Н]триптофана в бактериородопсин, синтезируемый Halobacterium halobium ЕТ 1001. Для масс-спектрометрического анализа мультикомпонентные смеси аминокислот в составе культуральных жидкостей и белковых гидролизатов (гидролиз в 6 М 2 НСl (3% фенол) и 2 М Ва(ОН)2 ), превращали в N-бензилоксикарбонил-производные аминокислот и метиловые эфиры N-диметиламинонафталин-5-сульфонил-производных аминокислот, которые препаративно разделеляли методом обращенно-фазовой высокоэффективной жидкостной хроматографии. Полученные [2 H]- и [13 C]аминокислоты представляли собой смеси, различающиеся количеством включённых в молекулу изотопов. Уровни включения 2 Н и 13 С в молекулы секретируемых аминокислот и аминокислотные остатки суммарных белков биомассы меняются в зависимости от содержания меченых субстратов в ростовых средах и различаются для разных аминокислот (до 10% для L -лейцина/изолейцина и до 97.5% для L -аланина).
Ключевые слова: стабильные изотопы; метилотрофные бактерии; галофильные бактерии; выращивание на 2 Н2 О; изотопномеченые аминокислоты, бактериородопсин
ВВЕДЕНИЕ
Обогащение молекул стабильными изотопами (2 Н, 13 С, 15 N и другие) в настоящее время является важным методом в разнопрофильных биохимических и метаболических исследованиях с использованием аминокислот и других биологически активных соединений (БАС) [1-3]. Тенденции к предпочтительному применению стабильных изотопов по сравнению с их радиоактивными аналогами обусловлены отсутствием радиационной опасности и возможностью определения локализации метки в молекуле методами высокого разрешения, включая ЯМР [4], ИК- [5] и лазерную спектроскопию [6] и масс-спектрометрию [7]. Развитие этих методов детекции стабильных изотопов за последние годы позволило повысить эффективность биологических исследований, а также изучать структуру и механизм действия клеточных БАС на молекулярном уровне [8, 9]. В частности, аминокислоты, меченные 2 Н, 13 С, 15 N с различными уровнями изотопного включения, применяются для изучения пространственной структуры и конформационных изменений белков [10], взаимодействия белковых молекул [11], а также в химических синтезах широкого круга изотопномеченых соединений на их основе. Например, меченый L -фенилаланин использован в синтезах пептидных гормонов и нейротрансмиттеров [12].
Важным моментом в исследованиях с применением меченых аминокислот, является их доступность. Изотопномеченые аминокислоты могут быть получены с использованием химических, ферментативных и биосинтетических методов. Однако химические синтезы часто многостадийны, требуют больших расходов ценных реагентов и меченых субстратов и приводят в результате к продукту, представляющему собой рацемическую смесь D - и L - форм, для разделения которых требуются специальные методы [13]. Более тонкие синтезы меченых аминокислот связаны с использованием комбинации химических и ферментативных подходов [14-16].
Для многих целей и прежде всего для структурных исследований белков биотехнология предлагает альтернативный химическому синтезу путь получения аминокислот, меченных стабильными изотопами, который приводит к высоким выходам синтезируемых продуктов, к эффективному включению изотопов в молекулы, и, самое главное, к сохранению природной конфигурации синтезируемых соединений. При биосинтетическом получении меченых аминокислот используют несколько подходов, один из которых заключается в равномерном обогащении синтезируемых соединений по всему углеродному скелету молекулы за счёт выращивания штаммов продуцентов на средах, содержащих в качестве источников стабильных изотопов следующие субстраты: 15 NН4 Сl [17], (13 С)метанол, (2 Н)метанол [18], и 2 Н2 О [19]. Этот подход включает в себя также комплексное использование химических компонентов биомассы, выращенной в присутствии стабильных изотопов, для выделения и фракционирования нужных изотопномеченых соединений. Другой подход заключается в сайт-специфическом обогащении аминокислот по определённым положениям молекул за счёт ассимиляции клеткой меченых предшественников, например, [1,4- 13 С]сукцината, [1, 2- 13 С]ацетата, [1- 13 С]лактата и др. [20, 21]. Методы получения изотопномеченых аминокислот в аспекте их использования для ЯМР-исследований белков более подробно изложены в работах ЛеМастера [22].
Настоящая работа является продолжением исследований [23-25], направленных на биосинтетическое получение [2 Н]- и [13 С]аминокислот за счёт утилизации низкомолекулярных меченых субстратов - (2 Н)метанола, (13 С)метанола и 2 Н2 О в клетках микроорганизмов и реализацию возможности определения стабильных изотопов методом масс-спектрометрии электронного удара. Чувствительность масс-спектрометрии составляет 10-9 -10-11 нмоль, что существенно выше, чем при использовании ИК- и ЯМР-спектроскопии. Данный метод в сочетании с обращённо-фазовой ВЭЖХ хорошо зарекомендовал себя для исследования уровня изотопного обогащения молекул аминокислот в составе их мультикомпонентных смесей, каковыми являются препараты культуральных жидкостей штаммов-продуцентов аминокислот и гидролизаты белков, полученные со сред, содержащих стабильные изотопы.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Объектами исследования служили полученные в результате мутагенеза L -фенилаланинпродуцирующий штамм факультативных метилотрофных бактерий Brevibacterium methylicum , ассимилирующий метанол по рибулозо-5-монофосфатному пути фиксации углерода, и L -лейцинпродуцирующий штамм облигатных метилотрофных бактерий Methylobacillus flagellatum , реализующий 2-кето-3-дезоксиглюконатальдолазный вариант рибулозо-5-монофосфатного пути фиксации углерода. Для компенсации ауксотрофности по L -лейцину и L -изолейцину эти аминокислоты добавляли в ростовые среды в протонированном виде. При этом уровни накопления L -фенилаланина и L -лейцина в культуральных жидкостях штаммов-продуцентов достигали величины 0.8 и 1.0 г/л соответственно [23]. Включение дейтерия в молекулы секретируемых аминокислот и суммарных белков биомассы осуществляли за счёт выращивания штамма B. methylicum на средах с 2 Н2 О и обычным метанолом, так как уровень включения 2 Н в молекулы аминокислоты за счёт ассимиляции (2 Н)метанола незначителен [25].
Поскольку в клетке происходит ассимиляция водорода (дейтерия) из Н2 О (2 Н2 O)среды, мы подбирали условия включения дейтерия в молекулы аминокислот и белков при ступенчатом возрастании концентрации 2 Н2 O в ростовых средах, как показано в табл. 1. Рост бактерий на 2 H2 O-cодержащих средах характеризуется увеличением продолжительности лаг-фазы, времени клеточной генерации и снижением выходов микробной биомассы (табл. 1), поэтому было необходимо проводить адаптацию бактерий к 2 Н2 О. Метод адаптации штамма B. methylicum к росту на 2 Н2 О при сохранении способности к биосинтезу L -фенилаланина описан в работе [23]. В данной работе были исследованы образцы культуральной жидкости B. methylicum и гидролизаты биомассы, полученные в ходе многоступенчатой адаптации бактерий к тяжёлой воде на средах с различным содержанием 2 Н2 О (от 24.5 до 98% 2 Н2 О*). Поскольку данный штамм метилотрофных бактерий удалось адаптировать к росту на 2 Н2 О, исследование уровней включения дейтерия в молекулы аминокислот представлялось наиболее интересным.
В отличие от культивирования на 2 Н2 О-среде, где необходимо проводить клеточную адаптацию к дейтерию, при получении [13 С]аминокислот за счет утилизации 13 СН3 ОН данный этап не является обязательным, поскольку этот изотопный субстрат не оказывает негативного биостатического эффекта на ростовые характеристики метилотрофов (см. табл. 1). Поэтому в случае M. flagellatum включение 13 С в молекулы аминокислот осуществляли в одну стадию при выращивании бактерий на водных средах, содержащих 1% (13 C)метанол.
Таблица 1
Влияние изотопного состава среды на рост штаммов B. methylicum и M. flagellatum
| Номер опыта | Среда выращивания | Величина лаг-фазы, ч | Выход биомассы, % от контроля | Время генерации, ч |
| 1 | 0 | 24.0 | 100 | 2.2 |
| 2 | 24.5 | 32.1 | 90.6 | 2.4 |
| 3 | 49.0 | 40.5 | 70.1 | 3.0 |
| 4 | 73.5 | 45.8 | 56.4 | 3.5 |
| 5 | 98.0 | 60.5 | 32.9 | 4.4 |
| 6 | CН3 ОН | 0 | 100 | 1.1 |
| 7 | 13 СН3 ОН | 0.1 | 72.0 | 1.0 |
В качестве другой модельной системы для включения изотопной метки в молекулы белков, использовали бактериородопсин [26], синтезируемый в мембране Halobacterium halobium ЕТ 1001 . Выбор для этих целей бактериородопсина, функционирующего как АТP-зависимая транслоказа в клетках галофильных бактерий, был продиктован возможностью исследования с его помощью процессов функционирования мембранных белков in vivo в условиях изотопного обогащения среды дейтерием. Для включения дейтериевой метки в молекулу бактериородопсина использовали метод сайт-специфического обогащения белка за счёт выращивания H. halobium ЕТ 1001 на синтетической среде с дейтерийсодержащими аналогами ароматических аминокислот - L -[2,3,4,5,6-2 Н]фенилаланином, L -[3,5-2 Н]тирозином и L -[2,4,5,6,7-2 Н]триптофаном.
Основные этапы при выделении [2 H]-и [13 C]-аминокислот заключались в выращивании штаммов-продуцентов на средах с мечеными субстратами - (2 Н)метанолом, (13 С)метанолом и 2 Н2 О или L -[2,3,4,5,6-2 Н]фенилаланином, L -[3,5-2 Н]тирозином и L -[2,4,5,6,7-2 Н]триптофаном (бактериородопсин), отделении культуральных жидкостей, содержащих секретируемые аминокислоты, от микробной биомассы, разрушении клеток, выделении фракции суммарных белков биомассы и бактериородопсина с последующим их гидролизом, дериватизации смесей аминокислот дансилхлоридом, бензилоксикарбонилхлоридом и диазометаном, разделении метиловых эфиров N-Dns-производных аминокислот и N-Cbz-производных аминокислот методом обращённо-фазовой ВЭЖХ, масс-спектрометрии электронного удара полученных производных аминокислот.
2 Н- и 13 C-Содержащие аминокислоты выделяли из лиофилизованных культуральных жидкостей штаммов-продуцентов аминокислот B. methylicum и M. flagellatum , а также в составе гидролизатов суммарных белков биомассы. При выделении фракции суммарных белков необходимо учитывать наличие в них углеводов, липидов и пигментов. В работе использовали богатые по белку штаммы бактерий со сравнительно небольшим содержанием углеводов в них. Гидролизу в качестве фракции суммарных белков подвергали остаток после исчерпывающего отделения липидов и пигментов экстракцией органическими растворителями (метанол-хлороформ-ацетон). В редких случаях для полного отделения от сопутствующих компонентов прибегали к солюбилизации белков в SDS или высаливании их сульфатом аммония.
Выделение и очистку индивидуальных белков с целью дальнейшего изучения их пространственной структуры целесообразно осуществлять методом солюбилизации с использованием подходящих детергентов (см. [27]) что особенно важно для бактериородопсина, являющегося высокоспиральным белком. Поэтому при выделении бактериородопсина из пурпурных мембран галофильной бактерии H. halobium ЕТ 1001 мы солюбилизовали его в 0.5% растворе SDS с сохранением a-спиральной конфигурации белка [28], а далее осаждали его метанолом. Гомогенность очищенного бактериородопсина была подтверждена электрофорезом в 12.5% ПААГ в присутствии 0.1% SDS.
Гидролиз дейтериймеченых белков проводили в условиях предотвращения реакций изотопного обмена водорода на дейтерий в ходе гидролиза и сохранения остатков ароматических аминокислот в белке. Были рассмотрены два альтернативных варианта проведения гидролиза - кислотный и щелочной. Кислотный гидролиз белка в стандартных условиях (6 М HCl, 24 ч, 1100 С), как известно, приводит к полному разрушению триптофана и частичному разрушению серина, треонина и некоторых других аминокислот [29]. Другим значительным недостатком при проведении гидролиза в HCl является изотопный (1 Н-2 Н)-обмен ароматических протонов (дейтеронов) в молекулах триптофана, тирозина и гистидина, а также протонов (дейтеронов) при атоме С3 аспарагиновой и С4 глутаминовой кислот [30]. Поэтому, чтобы получить реальные данные о биосинтетическом включении дейтерия в молекулы аминокислот необходимо проводить гидролиз белка с использованием дейтерированных реагентов (6 М 2 НCl с 3% фенолом (в 2 Н2 O)). Другой вариант гидролиза белка заключался в использовании 2 М Ba(OH)2 (1100 C, 24 ч). В этих условиях гидролиза белка реакций изотопного обмена водорода на дейтерий в ароматических аминокислотах - тирозине и триптофане не происходит, а триптофан не разрушается. Оба метода гидролиза показали хорошие результаты по сохранению ароматических аминокислот в гидролизатах белка и содержанию дейтерия в молекулах аминокислот. Необходимо подчеркнуть, однако, что для препаративного получения дейтерированных аминокислот из белка микроорганизмов целесообразнее использовать гидролиз в 2 НСl в 2 Н2 О (в присутствии добавки фенола для сохранения ароматических аминокислот), позволяющего избежать рацемизации. Для изучения же уровня включения стабильных изотопов в остатки ароматических кислот бактериородопсина и в аналитических целях лучше применять гидролиз белка в растворе Ва(ОН)2 , при котором отсутствует (1 Н-2 Н)-обмен в аминокислотах и сохраняются остатки фенилаланина, тирозина и триптофана. При щелочном гидролизе возможная рацемизация аминокислот не влияет на результат последующего масс-спектрометрического определения уровней включения дейтерия в аминокислоты.
Для получения летучих производных аминокислоты переводили в метиловые эфиры N-Dns-аминокислот или N-Cbz-аминокислоты, которые затем разделяли методами обращенно-фазовой ВЭЖХ. Условия N-дериватизации аминокислот отрабатывали таким образом, чтобы получить в масс-спектрах как можно более интенсивные пики их молекулярных ионов М+. на уровне фона метаболитов среды. Для этого проводили прямую дериватизацию аминокислот в составе лиофилизованных культуральных жидкостей и гидролизатов суммарных белков биомассы пятикратным избытком дансилхлорида или бензилоксикарбонилхлорида.
В этих условиях для лизина, гистидина, тирозина, серина, треонина и цистеина наряду с монопроизводными образовывались ди-Dns и ди-Cbz-производные. Кроме этого, из аргинина синтезировался N-три-Dns-(Cbz)-аргинин. Поэтому в масс-спектрометрических исследованиях молекулярные ионы М+. этих соединений соответствовали ди- или три- производным.
Эффективность использования N-Cbz-производных аминокислот в обращённо-фазовой ВЭЖХ и в масс-спектрометрических исследованиях была показана ранее [31, 32]. Летучесть N-производных аминокислот при масс-спектрометрическом анализе может быть повышена за счет дополнительной дериватизации по карбоксильной группе, поэтому N-Dns-аминокислоты были переведены в их метиловые эфиры. Для предотвращения обратного изотопного обмена ароматических протонов (дейтеронов) при этерификации дейтериймеченых аминокислот, в данной работе отдали предпочтение использованию диазометана для этих целей [33]. Свежеприготовленным раствором диазометана в диэтиловом эфире обрабатывали сухие остатки смесей аминокислот. При дериватизации аминокислот диазометаном происходило дополнительное N-метилирование по a-NH-(Dns)-группе аминокислот, что приводило к появлению в масс-спектрах метиловых эфиров N-Dns-аминокислот дополнительных пиков, соответствующих соединениям с молекулярной массой на 14 массовых единиц больше исходных.
В данной работе включение изотопов 2 Н и 13 С в молекулы аминокислот мультикомпонентных смесей в составе культуральных жидкостей и белковых гидролизатов определяли методом масс-спектрометрии электронного удара. Метиловые эфиры N-Dns-производных аминокислот или N-Cbz-производные аминокислот препаративного разделяли методом обращённо-фазовой ВЭЖХ. Степени хроматографической чистоты 2 Н- и 13 С-содержащих аминокислот, выделенных из культуральных жидкостей B. methylicum и M. flagellatum и гидролизатов белков в виде их N-Cbz-производных аминокислот составили 96-98%, при выходах - 67-89%. Для отдельных аминокислот оказалось более удобным разделение в виде метиловых эфиров N-Dns-производных аминокислот. При этом степень хроматографической чистоты полученных из гидролизатов бактериородопсина метиловых эфиров N-Dns-фенилаланина, N-Dns-тирозина и N-Dns-триптофана составили 96, 97 и 98% соответственно. Данный результат важен потому, что именно метиловые эфиры N-Dns-аминокислот вследствие своей химической стабильности, наличия высокоинтенсивных молекулярных ионов М+. при высоких молекулярных массах оказались весьма удобными для масс-спектрометрических исследований и позволяют идентифицировать аминокислоты в присутствии низкомолекулярных метаболитов среды и других продуктов дериватизации. Последний факт очень важен для изучения состава пула аминокислот, секретируемых в культуральные жидкости штаммов-продуцентов.
Пути фрагментации метиловых эфиров N-Dns-фенилаланина и N-Dns-лейцина при масс-спектрометрии электронного удара приводят к формированию пиков их молекулярных ионов при m/z 412 и m/z 378 и к образованию дансильных фрагментов и продуктов их дальнейшего распада до N-диметиламинонафталина, а также к получению аминных А+ и аминоацильных фрагментов В+ (рис. 1). Показанная на рис. 1 фрагментация метиловых эфиров N-Dns-фенилаланина и N-Dns-лейцина характерна для этих производных всех других аминокислот, что позволяет проводить масс-спектрометрический мониторинг изотопномеченых аминокислот в составе интактных культуральных жидкостей штаммов-продуцентов, содержащих сумму аминокислот и других метаболитов среды, до стадии их хроматографического разделения, а также исследовать включение стабильных изотопов в аминокислоты белковых гидролизатов.

При использовании в качестве источников стабильных изотопов (13 С)метанола и 2 Н2 О, в клетке синтезируются изотопнозамещённые аминокислоты, различающиеся количеством атомов, замещённых на 13 С и 2 Н. При этом, чем выше молекулярная масса аминокислот, тем возможен больший набор ионов, соответствующих изотопнозамещённым формам. Пики при m/z 323.2; 337.4; 368.5; 382.3; 420.5 в масс-спектре [13 С]аминокислот дериватизованной культуральной жидкости M. flagellatum , полученной с водной среды, содержащей 1% (13 С)метанол (рис. 2 б ), соответствуют по массе метиловым эфирам N-Dns-глицина, N-Dns-аланина, N-Dns-валина, N-Dns-лейцина/изолейцина и N-Dns-фенилаланина. Следует подчеркнуть, что величина m/z для молекулярного иона метиловых эфиров N-Dns-лейцина и изолейцина в масс-спектрах электронного удара одинакова, поэтому данным методом нельзя точно идентифицировать эти аминокислоты. Максимальные уровни включения 13 С в молекулы аминокислот, измеренные по увеличению усреднённого значения m/z для молекулярного иона изотопномеченого образца в сравнении с молекулярной массой природной аминокислоты варьируют от 35% для [13 C]аланина до 95% для [13 С]фенилаланина (табл. 2). Учитывая ауксотрофность штамма по L -изолейцину, разброс значений может быть объяснён вкладом экзогенного L -изолейцина в уровень изотопного включения лейцина, а также других метаболически связанных с ним аминокислот (см. текст ниже).

Для штамма B. methylicum наблюдалось специфическое возрастание уровней изотопного включения дейтерия в молекулы индивидуальных аминокислот культуральных жидкостей (табл. 2) при ступенчатом увеличении концентраций 2 Н2 O в ростовой среде. Уровни включения дейтерия в молекулы разных аминокислот при одинаковых условиях культивирования различаются. Такой результат зафиксирован во всех экспериментах, где источником стабильных изотопов служила 2 Н2 О.
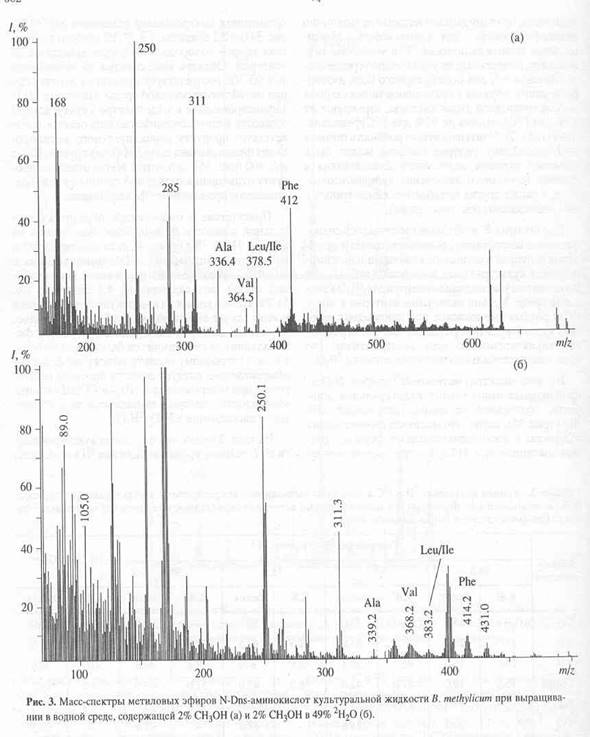
Из масс-спектра метиловых эфиров N-Dns-производных аминокислот культуральной жидкости, полученной со среды, содержащей 49% 2 Н2 О (рис. 3 б ) видно, что молекула фенилаланина содержала 6 изотопнозамещённых форм со средним значением m/z 414.2, которое возрастает по сравнению с контрольными условиями (m/z 412.0, рис. 3 а ) на 2.2 единицы, т. е. 27.5% от общего количества атомов водорода в молекуле замещены на дейтерий. Область масс-спектра со значениями m/z 90-300 соответствует продуктам дериватизации метаболитов ростовой среды. Пик с m/z 431.0, зафиксированный в масс-спектре культуральной жидкости и проявляющийся во всех опытах, соответствует продукту дополнительного метилирования фенилаланина по a-NH-(Dns)- группе. Пик с m/z 400 (рис. 3 б ) вероятнее всего отвечает продукту отщепления метильной группы от дейтерированного производного фенилаланина.
Присутствие в масс-спектре образца культуральной жидкости B. methylicum , полученной на среде с 73.5% 2 Н2 О (рис. 4) пика молекулярного иона метилового эфира N-Dns-фенилаланина с m/z 416.1 указывает на увеличение молекулярной массы фенилаланина на 4.1 единицу, т. е., 51.2% атомов водорода в молекуле фенилаланина в этом случае замещены на дейтерий. Очевидно, что вышеобозначенные атомы дейтерия включились в молекулу фенилаланина за счет процесса биосинтеза de novo , т. е. по углеродному скелету молекулы. К легко обмениваемым следует отнести протоны (дейтероны) при гетероатомах в NH2 -и СООН- группах аминокислот, которые замещаются за счёт лёгкости диссоциации в Н2 О (2 Н2 О).
Таблица 2
Уровни включения 2 Н и 13 С в молекулы аминокислот, секретируемых в культуральную жидкость (КЖ) B. methylicum и M. flagellatum, и в аминокислотные остатки белков (данные получены для метиловых эфиров N-Dns-аминокислот и N-Cbz-аминокислот)
|
| Содержание 2 Н2 О в среде, %* 24.5 49.0 73.5 98.0 КЖ белок КЖ белок КЖ белок КЖ белок |
1%13 СН3 ОН** КЖ белок | ||||
| Глицин | - 15.0 | - 35.0 | - 50.0 | - 90.0 | 60.0 90.0 | |
| Аланин | 24.0 20.0 | 37.5 45.0 | 62.5 62.5 | 77.5 97.5 | 35.0 95.0 | |
| Валин | 20.0 15.0 | 46.3 36.3 | 43.8 50.0 | 58.8 50.0 | 50.0 50.0 | |
| Лейцин/изолейцин | 15.0 10.0 | 47.0 42.0 | 46.0 45.0 | 51.0 49.0 | 38.0 49.0 | |
| Фенилаланин | 15.0 24.5 | 27.5 37.5 | 51.2 50.0 | 75.0 95.0 | 95.0 80.5 | |
| Тирозин | - 20.0 | - 25.6 | - 68.8 | - 92.8 | - 53.5 | |
| Серин | - 15.0 | - 36.7 | - 47.6 | - 86.6 | - 73.3 | |
| Аспарагиновая кислота | - 20.0 | - 36.7 | - 60.0 | - 66.6 | - 33.3 | |
| Глутаминовая кислота | - 20.0 | - 40.0 | - 53.4 | - 70,0 | - 40.0 | |
| - 10.0 | - 35.3 | - 40.0 | - 58.9 | - 54.4 | ||
--> ЧИТАТЬ ПОЛНОСТЬЮ <--