Статья: Синтез и исследование моно- и диамидов тиодигликолевой кислоты как возможных ингибиторов коррозии железа
Существенное влияние на скорость растворения железа в кислых средах оказывают многие органические соединения, в том числе и тиодигликоль [1,2]. Основываясь на определенной структурной аналогии между тиодигликолем S(CH2CH2OH)2 и тиодигликолевой кислотой S(CH2COOH)2, можно было предположить, что тиодигликолевая кислота (ТДГК) и ее азотсодержащие производные тоже будут оказывать влияние на растворение железа в кислой среде.
Исследования показали [3], что ТДГК, ее ангидрид, дигидразид, эфир действительно ускоряют растворение железа в 1 н серной кислоте и могут использоваться в процессах травления. Продолжая начатые исследования, казалось интересным расширить круг производных ТДГК с целью изыскания cреди них возможных ингибиторов и стимуляторов коррозии металлов.
Для этого были взяты моно- и диамиды на основе ТДГК и различных аминов. Сама ТДГК была получена реакцией монохлорацетата с сероводородом [4]. Моноамиды синтезировали исходя из аминов и ангидрида ТДГК, полученного, в свою очередь, кипячением ТДГК в среде хлористого ацетила по схеме:
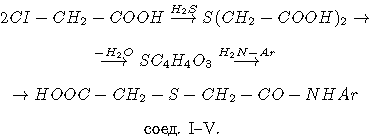
Синтез диамидов ТДГК (соединения V-X) осуществляли из дихлорангидрида ТДГК и тех же аминов:
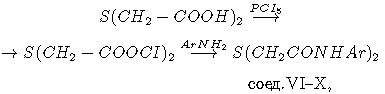
где Аr- фенил, 4-дифенил, alpha- и beta-нафтил, 2-флуоренил. Характеристика соединений приведена в табл. 1 и 2.
Моноамиды и диамиды ТДГК - соединения, плохо растворимые в воде при комнатной температуре, поэтому для испытаний их приходилось растворять в малых объемах органических растворителей (диоксан, диметилформамид), и этот раствор в качестве ингибитора вводить в 0,1 н серную кислоту. К тому же можно было надеяться, что малые дозы органических растворителей усилят защитные свойства ингибиторов, вызывая эффект синергизма [6].
Изучение предполагаемых ингибиторов проводили методом поляризационного сопротивления [7,8] на приборе Р-5035 при температуре ![]() oC течение 2 ч. Величина электродного потенциала железа измерялась с помощью прибора рН-340 с хлорсеребряным электродом сравнения. Измеренное значение поляризационного сопротивления Rin усредняли из пяти параллельных опытов и сравнивали со значением Ron в кислоте без ингибитора.Вычисляли коэффициент торможения
oC течение 2 ч. Величина электродного потенциала железа измерялась с помощью прибора рН-340 с хлорсеребряным электродом сравнения. Измеренное значение поляризационного сопротивления Rin усредняли из пяти параллельных опытов и сравнивали со значением Ron в кислоте без ингибитора.Вычисляли коэффициент торможения ![]() , который показывает,
, который показывает,
Таблица I
Моноамиды тиодигликолевой кислоты HOOC-CH2-S-CH2-CONHAr (соед. I-V)
| Вещество | Ar |
Выход, % |
Tпл oC (р-ль для крист.) | Формула | Найдено, % | Вычислено, % | ||||||
| C | H | N | S | C | H | N | S | |||||
| I | фенил | 85 | 101-103 (a) | C10H11NO3S | 14,02 | 14,22 | ||||||
| II | 4-дифенил | 87 | 167-168 (a) | C16H14NO3S | 64,66 | 5,16 | 4,62 | 10,73 | 64,16 | 4,71 | 4,68 | 10,70 |
| III | 83 | 157-158 (a) | C14H13NO3S | 60,50 | 4,78 | 5,22 | 11,76 | 61,06 | 4,76 | 5,09 | 11,64 | |
| IV | 80 | 113-114 (a) | C14H13NO3S | 60,75 | 4,86 | 5,25 | 11,70 | 61,06 | 4,76 | 5,09 | 11,64 | |
| V | 2-флуоренил | 91 | 159-160 (б) | C17H15NO3S | 65,34 | 4,91 | 4,36 | 10,25 | 65,15 | 4,82 | 4,48 | 10,23 |
Таблица 2
Диамиды тиодигликолевой кислоты S(CH2CONHAr)2 (соед. VI-X)
| Соединение | Ar |
Выход, % |
Tпл oC (р-ль для кристалл.) | Формула | Найдено, % | Вычислено, % | ||
| N | S | N | S | |||||
| VI | фенил | 90 | 167,168 [5] | |||||
| VII | 4-дифенил | 80 | 234-235 (ДМФА) | C28H24N2O2S | 6,24 | 6,94 | 6,19 | 7,08 |
| VIII | 79 | 192-193 (б) | C24H20N2O2S | 6,87 | 8,74 | 6,99 | 8,004 | |
| IX | 75 | 202-203 (б) | C24H20N2O2S | 6,40 | 8,17 | 6,99 | 8,004 | |
| X | 2-флуоренил | 82 | 255-256 (разл.) | C30H24N2O2S | 5,53 | 5,88 | ||
ДМФА-диметилформамид; а-вода; б-спирт+вода.
Таблица 3
Значения коэффициента торможения коррозии ![]()
для моно- и диамидов ТДГК
| Соединение | Ar |
Моноамиды --> ЧИТАТЬ ПОЛНОСТЬЮ <-- К-во Просмотров: 174
Бесплатно скачать Статья: Синтез и исследование моно- и диамидов тиодигликолевой кислоты как возможных ингибиторов коррозии железа
|