Статья: Влияние кислорода на активность нанесенного ванадиевого катализатора в процессе газофазной полимеризации этилена
Каталитические системы циглеровского типа отличаются высокой чувствительностью к примесям кислорода. На примере гомогенных каталитических систем на основе соединений титана [1, 2] и ванадия [3, 4] и гетерогенных титановых катализаторов [5, 6] показано, что под действием кислорода может происходить активация и ингибирование процесса полимеризации, меняется ММ и стереорегулярность полимерных продуктов.
В литературе нет сведений о влиянии кислорода на полимеризацию с катализаторами, закрепленными на носителе. В связи с тем, что в производстве полиолефинов и наполненных полимерных материалов все более широкое распространение получают процессы газофазной полимеризации с использованием нанесенных катализаторов, в настоящей работе была поставлена задача исследовать влияние кислорода на активность нанесенного ванадиевого катализатора при полимеризации этилена в отсутствие растворителя.
Кинетику газофазной полимеризации этилена изучали в стеклянной вакуумной установке [7]. Полимеризацию осуществляли в термостатируемом реакторе объемом 400 мл, снабженном двумя отростками для раздельного введения нанесенного ванадиевого катализатора и алюминийорганического соединений (в парообразном состоянии). В ходе полимеризации давление мономера и скорость перемешивания реакционной массы поддерживали постоянными.
Ванадиевый катализатор был получен нанесением VC14 на неорганический носитель — перлит (фракция с размером частиц 0,2 мм) по методике, разработанной в ИХФ АН СССР [8]. Содержание ванадия на носителе, определенное колориметрическим методом [9], менялось от 0,27 до 0,55 вес.%; валентное состояние ванадия, по данным потенциометрического титрования, было равно 3.
В качестве сокатализатора использовали А1(изо-С4Н3)з (А1(изо-Вu)3) (т. кип. 39-40°/0,65 гПа). По анализу содержание А1 13,65, содержание изо-Вu-группы 85,4 вес.%.
Этилен подвергали низкотемпературной разгонке и пропускали через колонку с пиролюзитом для очистки от примеси кислорода. Количество кислорода в очищенном этилене по данным колориметрического анализа составляло менее 5 млн. долей.
Кислород, использованный для добавок, был получен разложением КМnСr.А1(изо-Вu)2(ОВu-изо) синтезировали из А1(изо-Вu)з и абсолютного изобутилового спирта. Содержание изо-Вu-групп в диизобутилалюминийизобутоксиде, по данным хроматографического анализа, составляло 58 вес.%; мольное отношение (OBu-изо): (изо-Bu), рассчитанное из ПМР-спектров, равнялось 0,46. Полимеризацию с А1 (изо-Вu)2(ОВu-изо) осуществляли в среде сухого спектрально чистого н-гептана.
В присутствии каталитической системы VCL/перлит — А1 (изо-Вu)3 про-цесс газофазной полимеризации этилена носит нестационарный характер. Активность катализатора, максимальная в начальный момент времени, снижается в ходе полимеризации и достигает постоянного значения (рис. 1).
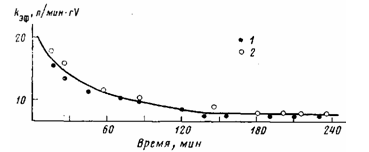
Рис. 1. Изменение эффективной константы скорости полимеризации этилена во времени в присутствии катализатора УС14/перлит — Al (изо-Bu) з. 70°, Al: V=22, [С2Н4] =0,018 моль/л, содержание ванадия на носителе 0,55 вес.%. Содержание кислорода в этилене 5 (1), 280 млн. долей (2)
В исследованных условиях (70°, содержание ванадия на носителе 0,27—0,55 вес.%, мольное отношение Al: V=5—40) эффективная константа скорости полимеризации каф, определяемая как скорость полимеризации, рассчитанная на единицу концентрации мономера и 1 г переходного металла, не зависит от содержания ванадия в нанесенном катализаторе и мало меняется с увеличением мольного отношения Al : V и с изменением порядка подачи компонентов катализатора и мономера в реакционную зону.
Эффекты, наблюдаемые при введении кислорода в процессе полимеризации, обусловлены протеканием химических реакций кислорода либо с исходными компонентами катализатора, либо с продуктами их взаимодействия. Поэтому при изучении влияния кислорода на каталитическую активность количество добавки целесообразно определять не только абсолютной концентрацией кислорода, но и отношением концентраций кислорода и каждого из компонентов катализатора, т. е. мольным отношением 02: V и О2: AI. Добавки кислорода вводили в реакционную зону на стадии формирования каталитических центров и в ходе полимеризации.
В первом случае проводили предварительное взаимодействие одного из компонентов катализатора с кислородом (в течение 5 мин), затем в систему вводили второй компонент и мономер. Условно такой порядок подачи реагентов можно обозначить [А1(изо-Вu)3+О2]+V (I) и [V+О2] + +А1(изо-Вu), (II).
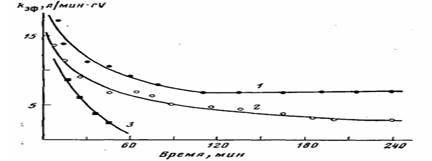
Рис. 2. Кинетические кривые полимеризации этилена на нанесенном ванадиевом катализаторе при различных концентрациях кислорода для системы I. 70°, Al: V= •=18-23, [С2Н4] =0,018 моль/л, содержание ванадия на носителе 0,27 вес.%- 02: А1=0 (1); 0,1 (2); 0,15 (3)
Рис. 2 демонстрирует влияние добавок кислорода на процесс полимеризации для системы I. Из рисунка видно, что с увеличением мольного отношения О2: А1 снижается каталитическая активность, меняется характер кинетики полимеризации, т. е. резко ускоряется дезактивация катализатора. При мольном отношении О2: А1=0,2 (соответственно 0,2 об.% О2) система I полностью теряет каталитическую активность.
Известно, что окисление алюминийтриалкилов кислородом приводит к образованию их алкоксипроизводных [10, 11]. Реакция протекает через стадии образования высокореакционноспособных перекисных соединений алюминия и их превращений. При температурах выше 20° основным продуктом реакции является моноалкоксид алюминия. На примере титановых катализаторов показано, что системы, включающие в качестве сокатализа-тора алкоксипроизводные триэтилалюминия, либо характеризуются низкой каталитической активностью [11], либо не активны в полимеризации [12].
В настоящей работе с целью установления причин дезактивации системы I исследовали продукт окисления Аl(изо-Ви)3 — диизобутилалюми-нийизобутоксид как сокатализатор с VCL/перлит. Методика эксперимента не позволяла осуществлять полимеризацию в газовой фазе из-за низкой упругости паров А1(изо-Вu)2(ОВu-изо) (т. кип. 120°/0,65 гПа), поэтому опыты проводили в к-гептане. Подобное различие в скоростях полимеризации в жидкой и газовой фазе отмечается также Кейи [13] при полимеризации пропилена с <x-TiCl3 — AlEt2Cl.
Полученные экспериментальные результаты по полимеризации этилена с А1(изо-Вu)2(ОВu-изо) приведены на рис. 3 и сводятся к следующему: катализатор УС14/перлит не обладает каталитической активностью в сочетании с А[(изо-Вu)2(ОВu-изо); добавки А1(изо-Вu)2(ОВu-изо) на стадии формирования активных центров в виде смеси с А1(изо-Вu)3 при одной и той же концентрации триизобутилалюминия (рис. 3, кривые 3, 4) и в ходе полимеризации (рис. 3, кривая 5) приводят к снижению начальной скорости полимеризации и ускорению дезактивации катализатора. На основании этих результатов, исходя из представлений о биметаллической природе активных центров, можно высказать следующие предположения: во-первых, Al(uзo-Bu)2(OBu-uзo) не является алкилирующим агентом и его действие ограничивается образованием комплексов с исходными и алки-лированными соединениями ванадия; во-вторых, образующиеся комплексы являются, пo-видимому, более прочными, по сравнению с комплексами, включающими А1(изо-Вu)3 (из-за сильных донорных свойств А1(изо-Вu)2-(ОВu-изо) [14, 15]); диизобутилалюминийбутоксид может замещать А1(изо-Вu)3 в ванадий-алюминиевых комплексах; в-третьих, комплексы A1(изо-Bu)2(OBu-изо) с алкилированным ванадием неактивны в процессе полимеризации этилена.
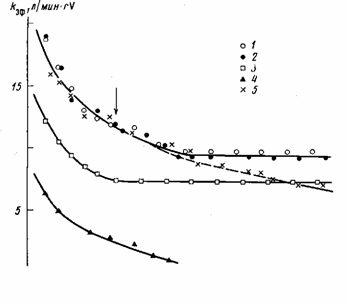
Рис. 3. Влияние добавок А1(изо-Вu)2 (OBu-uao) на каталитическую активность системы УС14/перлит - А1(изо-Вu)з. 70°, Al(uso-Bu)3: V=10-14, [С2А4] =0,018 моль/л, объем и-гептана 70 мл, содержание ванадия на носителе 0,38 вес.% [А1(изо-Вu)г(ОВu-изо)]:[А1(изо-Вu)3]=0 (7); 0,43 (2); 1 (3); 5 (4); 2 (5); стрелкой показано время введения А1(изо-Вu)2(ОВu-изо)
Таким образом, приведенные кинетические данные позволяют объяснить дезактивацию катализатора I с ростом мольного отношения О2: А1 (как и в случае катализатора [(О2+AlEt3)+a-TiCl3] [5]) образованием оксипроизводных алюминия и, как следствие, уменьшением начального числа активных центров в результате понижения эффективной концентрации исходных компонентов (алкилирующего агента А1(изо-Вu)3 и соединений ванадия, не связанных в комплекс с А1(изо-Вu)2(ОВu-изо)), а также накоплением неактивных комплексов алкилированного ванадия с диизо-бутилалюминийизобутоксидом.
Тот факт, что при полимеризации в газовой фазе дезактивация катализатора наблюдается при значительно меньших концентрациях бутоксида алюминия по сравнению с полимеризацией в растворителе, может быть связан с тем, что в растворе алкоксипроизводные алюминия находятся преимущественно в виде димеров и концентрация реакционноспособной мономерной формы низка [15].
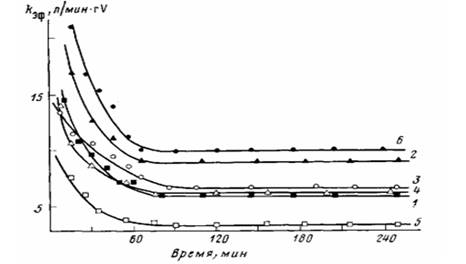
Рис. 4. Кинетические кривые полимеризации этилена на нанесенном ванадиевом катализаторе при различных концентрациях кислорода. Система II. Условия полимеризации те же, что на рис. 2. 02: V=0 (i), 1 (2), 2 (3), 4 (4), 7 (5), 7 (6) (через 5 мин после начала взаимодействия с ванадиевым компонентом кислород удаляли из реактора вакуумированием, после чего вводили А1(изо-Вu)3)
Изменение каталитической активности системы II с концентрацией кислорода показано на рис. 4. Из полученных экспериментальных данных следует, что если первым в контакт с кислородом вступает ванадиевый компонент, то образующаяся система II (в отличие от системы I) по стабильности не отличается от исходной. Характер кинетических кривых не меняется с увеличением мольного отношения О2 : V. Из рис. 4 видно также, что предварительное взаимодействие ванадиевого компонента с кислородом в эквимольных количествах (кривая 2) приводит к активации катализатора. Значения кэф. и кэф. ст, полученные в отсутствие кислорода и при различных мольных отношениях О2 : V, приведены на рис. 5. Как видно из этих данных, зависимость каталитической активности системы II от мольного отношения О2 : V носит экстремальный характер. При увеличении мольного отношения О2 : V от 0 до 1 (0,05 об. % О2) /сэф. 0 возрастает от 19,5 до 26 л/минт V, кэф. ст от 6,5 до 9 л/мин-г V. При более высоких концентрациях кислорода активность системы II снижается, при мольных отношениях 02.' V>10 (>1 об.% О2) система становится неактивна в полимеризации.
Таким образом, наблюдаемая активация системы II может быть связана с образованием соединений ванадия высшей валентности. Известно, что активность катализаторов, включающих в качестве исходного ванадиевого компонента соединения высоковалентного ванадия (VOCl3, VO(OR)3), значительно превышает активность катализаторов на основе галоидов ванадия низшей валентности [17]. Дезактивация катализатора при мольных отношениях О2: V выше эквимольного (рис. 5), как было показано, не является результатом взаимодействия кислорода с исходным ванадиевым соединением. Если после окисления ванадия (при высоких мольных отношениях О2: V) непрореагировавший кислород удаляли вакуумированием и затем добавляли А1(изо-Вu)3, то активность катализатора была значительно выше, чем в опытах без удаления кислорода (рис. 4, кривая 6 и рис. 5). По-видимому, понижение активности системы II с увеличением концентрации кислорода, как и системы I, обусловлено ингибирующим действием образующегося диизобутилалюминийизобутоксида.
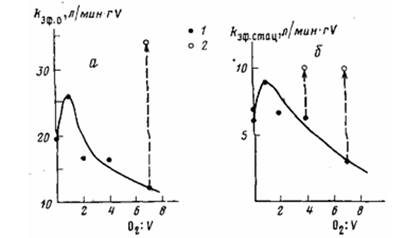
Рис. 5. Зависимость начальной (а) и стационарной (5) эффективных констант скорости полимеризации этилена с системой II от мольного отношения 02: V. Условия полимеризации те же, что на рис. 2. 1 — полимеризацию проводили без удаления кислорода; 2 — через 5 мин после начала взаимодействия с ванадиевым компонентом кислород удаляли из реактора вакуумированием, после чего вводили А1(изо-Вu)з
--> ЧИТАТЬ ПОЛНОСТЬЮ <--