Учебное пособие: Будова атомів металів
10. Де виникають поверхневі дефекти?
«Кристалізація металів»
Кристалізацією називають перехід металів з рідкого стану в твердий (кристалічний). Відбувається вона внаслідок переходу системи з термодинамічно нестійкого стану в термодинамічно стійкий стан, тобто зі стану з більшою енергією у стан з меншою вільною енергією або термодинамічним потенціалом, коли вільна енергія кристала є меншою від вільної енергії рідкої фази.
Енергетичний стан системи прийнято характеризувати вільною енергією. Вільною енергією називається частина повної енергії речовини, яка обернено змінює свою величину при зміні температури, поліморфних перетвореннях, плавленні. З підвищенням температури величина вільної енергії зменшується. Зміну вільної енергії рідкої і твердої речовини показано на рис. 1.10.
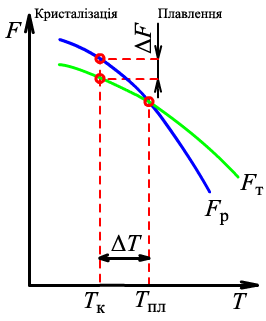
Рис. 1.10 Зміна вільної енергії рідкого і твердого металу залежно від температури
При рівноважній температурі Тпл величини вільної енергії металу в рідкому і твердому стані рівні; метал в обох станах перебуває у рівновазі. При температурі вище Тпл стійкішим є рідкий метал, який має менший запас вільної енергії, а нижче цієї температури стійким є твердий метал. Процес кристалізації розвиватиметься в тому випадку, якщо рідкий метал охолодити нижче температури Тпл.
Температура, за якої практично починається процес кристалізації, називається фактичною температурою кристалізації Тк.
Різниця між рівноважною температурою Тпл і фактичною температурою Тк називається ступенем переохолодження ΔТ: ![]() (1.1)
(1.1)
Процес переходу металу з рідкого стану у твердий можна описати за допомогою кривих у координатах температура — час.
На рис. 1.11 показані криві охолодження, які характеризують процес кристалізації чистих металів при охолодженні з різною швидкістю V. При дуже повільному охолодженні ступінь переохолодження малий і при температурі кристалізації на кривій з'являється горизонтальна ділянка (зупинка у падінні температури), утворення якої пояснюється виділенням прихованої теплоти кристалізації.
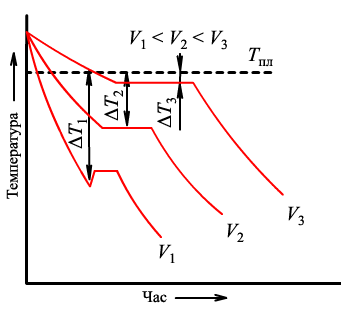
Рис. 1.11. Криві охолодження чистого металу
Під час плавлення відбувається поглинання теплоти, яка витрачається на підвищення енергії атомів, тобто на «руйнування» кристалічної ґратки металу. Ця теплота називається прихованою. У процесі кристалізації відбувається зворотне виділення енергії у вигляді прихованої теплоти кристалізації, яка компенсує тепло, що відводиться в оточуюче середовище, і затримує падіння температури.
Зі збільшенням швидкості охолодження ступінь переохолодження збільшується (криві 2 і 3) і процес кристалізації відбувається при температурах, які є значно нижчими, ніж рівноважна температура кристалізації.
Ступінь переохолодження залежить від природи і чистоти металу. Чим чистіший метал, тим при більшому ступені переохолодження виникають зародки твердих кристалів.
Процес кристалізації складається з двох стадій:
утворення центрів кристалізації (зародків кристалів);
розростання кристалів навколо цих центрів.
Схематично процес кристалізації показаний на рис. 1.12. При переохолодженні металу нижче температури Тпл у багатьох ділянках рідкого металу утворюються стійкі, здатні збільшуватися кристалічні зародки, які називають критичними зародками. Поки їх оточує рідина, кристали ростуть вільно і можуть мати правильну геометричну форму. Однак при зіткненні зростаючих кристалів їх правильна форма порушується, оскільки на ділянках контакту зростання граней припиняється. Кристал росте лише в тому напрямку, де він стикається з рідиною. Наслідком є те, що зростаючі кристали, які мають спочатку геометрично правильну форму, після тверднення набувають неправильної зовнішньої форми. Їх називають зернами, або кристалітами (рис. 1.13).

Рис. 1.12 Схема процесу кристалізації металу

Рис. 1.13. Мікроструктура заліза: а — зерна заліза; б — зерно заліза
Швидкість процесу кристалізації визначається двома величинами: швидкістю зародження центрів кристалізації і швидкістю росту кристалів.
Під швидкістю зародження центрів кристалізації розуміють кількість зародків, які виникають за одиницю часу в одиниці об'єму. Під швидкістю росту кристалів розуміють швидкість збільшення лінійних розмірів кристала за одиницю часу.
Кількість центрів кристалізації і швидкість росту кристалів залежать від ступеня переохолодження. Як видно з рис. 1.14, кількість зародків і швидкість їх зародження при рівноважній температурі кристалізації дорівнює нулю. При збільшенні ступеня переохолодження вони зростають і досягають максимуму. При великих ступенях переохолодження кількість центрів кристалізації і швидкість росту дорівнюють нулю, оскільки при низьких температурах дифузійна рухомість атомів є зменшеною, а тим самим є зменшеною і здатність системи до перетворення.
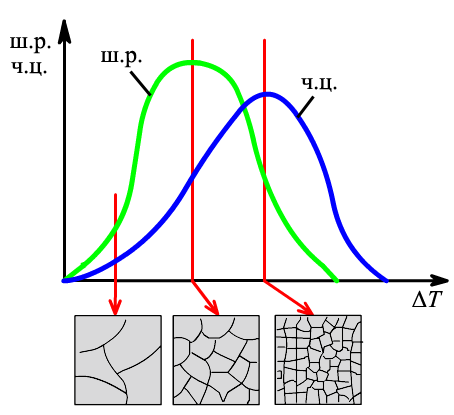
Рис. 1.14 Швидкість росту кристалів (ш.р.) і швидкість зародження центрів кристалізації (ч.ц.) залежно від ступеня переохолодження