Учебное пособие: Химические методы анализа
Денситометрия – основана на измерении плотности (определение концентрации веществ в растворах). Для определения состава измеряют вязкость, поверхностное натяжение, скорость звука, электропроводность и т.д.
Для установления чистоты веществ измеряют температуру кипения или температуру плавления.
Прогнозирование и расчет физико-химических свойств
Теоретические основы прогнозирования физико-химических свойств веществ
Приближенный расчет прогнозирования
Прогнозирование подразумевает оценку физико-химических свойств на основании минимального числа легкодоступных исходных данных, а может и полагать полное отсутствие экспериментальной информации о свойствах исследуемого вещества (» абсолютное» прогнозирование опирается только на сведенья о стехиометрической формуле соединения).
Прогноз неизвестных характеристик основывается на соотношениях между физико-химическими величинами, которые не являются универсальными и абсолютно строгими, такие соотношения наз. Корреляциями.
Закон соответственных состояний
Одно из центральных положений теорий термодинамического подобия – закон соответственных состояний возникла как следствие из приведенного уравнения Ван-дер-Вальса:
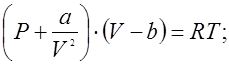 (для 1-го моля вещества)
(для 1-го моля вещества)
a = 3Pk Vk 2; b = 1/3 Vk ;
где Р, Рк – давление и критическое давление;
V, Vk – обьем мольный и критический мольный обьем;
Т, Тк - температура и критическая температура;
a, b – постоянные Ван-дер-Вальса;
R – универсальная газовая постоянная;
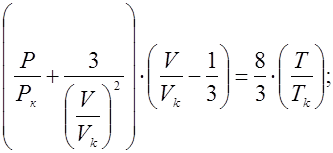
Отношение параметра к критическому параметру – приведенный параметр:
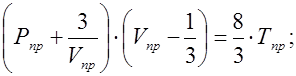 (1) – приведенное уравнение Ван-дер-Вальса;
(1) – приведенное уравнение Ван-дер-Вальса;
Состояние веществ с одинаковыми значениями приведенных параметров наз. Соответствующими состояниями.
Уравнение (1) отсутствует параметр относящийся к конкретному веществу, поэтому можно ожидать, что оно выполняется для определений совокупности веществ, следует, что из (1) при равенстве двух приведенных параметров нескольких веществ, третий приведенный параметр также должен быть одинаковым для всех веществ – закон соответственных состояний.
Теория термодинамического подобия
Основная теория подобия заключается в том, что зависимость между характеристиками объектов, выраженная в безразмерной форме справедливо для большой совокупности подобных объектов.
Зависимость между свойствами д.б. обобщенная и носить универсальный характер, а свойства должны быть представлены в безразмерной форме:
ƒ (Тпр , Рпр , Vпр ) = 0; (2)
Наличие такой зависимости для группы подобных веществ позволяет определить неизвестное свойство по известным значениям двух других свойств.
Уравнение (2) записывается относительно инварианта того свойства, которое подлежит определению с помощью закона соответствующих состояний.
Рпр = φ (Тпр , Vпр ); (3)
Уравнение должно быть пригодным для расчета широкого спектра свойств, поэтому развитием теории термодинамического подобия привело к выводу о том, что в соответствующих состояниях подобных веществ одинаковы не только безразмерные параметры состояния, но и инварианты любых физико-химических свойств. Такой инвариант может быть безразмерной комбинацией любых физико-химических свойств: