Учебное пособие: Общая и неорганическая химия
Состояние электрона характеризующееся различными значениями побочного квантового числа ![]() называется энергетическим подуровнем. В пределах каждого уровня с увеличением
называется энергетическим подуровнем. В пределах каждого уровня с увеличением ![]() , растёт энергия орбитали.
, растёт энергия орбитали.
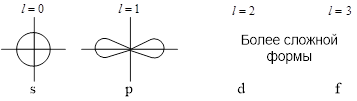
Каждому значению ![]() соответствует определённая форма орбитали (например, при
соответствует определённая форма орбитали (например, при ![]() – это сфера, центр которой совпадает с ядром).
– это сфера, центр которой совпадает с ядром).
Магнитное квантовое число ![]() характеризует ориентацию орбитали в пространстве (принимает все целочисленные значения от -
характеризует ориентацию орбитали в пространстве (принимает все целочисленные значения от - ![]() до +
до +![]() ).
).
Например, для ![]()
![]() . В пределах каждого подуровня орбиталь имеет одинаковую энергию.
. В пределах каждого подуровня орбиталь имеет одинаковую энергию.
Спиновое квантовое число ![]() характеризует вращательный момент, который приобретает электрон в результате собственного вращения вокруг своей оси (принимает два значения:
характеризует вращательный момент, который приобретает электрон в результате собственного вращения вокруг своей оси (принимает два значения: ![]() – вращение по часовой стрелке,
– вращение по часовой стрелке, ![]() – вращение против часовой стрелки).
– вращение против часовой стрелки).
Атомные орбитали заполняются электронами в соответствии с 3-мя принципами:
Принцип устойчивости (принцип min энергии): Каждая новая орбиталь заполняется только после того, как будут заполнены все предыдущие, т.е. более устойчивые (с min энергией) орбитали.
Энергия атомных орбиталей возрастает следующим образом:
![]()
Правило Клечковского: заполнение электронами атомных орбиталей происходит в соответствии с увеличением суммы главного ![]() и побочного
и побочного ![]() квантовых чисел; если
квантовых чисел; если ![]() одинакова, то атомная орбиталь заполняется от больших
одинакова, то атомная орбиталь заполняется от больших ![]() и меньших
и меньших ![]() к меньшим
к меньшим ![]() и большим
и большим ![]() .
.
| Орбиталь | |||
| 1 | 0 | 1 | 1s |
| 2 | 0 | 2 | 2s |
| 1 | 3 | 2p | |
| 3 | 0 | 3 | 3s |
| 1 | 4 | 3p | |
| 2 | 5 | 3d | |
| 4 | 0 | 4 | 4s |
| 1 | 5 | 4p | |
| 2 | 6 | 4d | |
| 3 | 7 | 4f | |
| 5 | 0 | 5 | 5s |
| 1 | 6 | 5p | |
| 2 | 7 | 5d | |
| 3 | 8 | 5f | |
| 4 | 9 | 5g | |
| 6 | 0 | 6 | 6s |
Принцип Паули: в атоме не может быть 2 электрона, у которых 4 одинаковых квантовых числа. Следовательно, на 1-ой орбитали могут находиться не более 2-х электронов, отличающихся друг от друга значением спинового квантового числа. Отсюда следует, что максимальное количество электронов на энергетическом уровне ![]() , на энергетическом подуровне
, на энергетическом подуровне ![]() .
.
Пример:
![]()
![]()
![]()
Правило Хунда: электроны располагаются на орбиталях равной энергии таким образом, чтобы их суммарный спин был максимальный. Это означает, что первоначально электроны заполняют все свободные орбитали данного подуровня по 1-му, имея при этом параллельные спины, и только потом происходит заполнение этих орбиталей 2-ми электронами.
Пример:
![]()
![]() Px Py Pz
Px Py Pz
| ↑ | ↑ |
| ↑ | ↑ | ↑ |
| ↑↓ | ↑ | ↑ |
| K | L | M | |||||||
| 1 | 2 | 3 | |||||||
| 0 | 0 | 1 | 0 | 1 | 2 | ||||
| 0 | 0 | -1 | 0 | +1 | 0 | -1 | 0 | +1 | |
| ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | |
Количество неспаренных электронов на внешнем уровне определяет валентность элемента, т.е. способность образовывать химические связи с другими атомами. В большинстве случаев, но не всегда.
![]() 5
5 ![]()
![]() 4
4 ![]()
4 ![]() 3
3 ![]()
3 ![]() 2
2 ![]()
2 ![]() 1
1 ![]()
1 ![]()
Периодический закон (1869 г): свойства простых тел, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
До появления сведений о сложном строении атома основной характеристикой элемента служил атомный вес (относительная атомная масса). Развитие теории строения атома привело к установлению того факта, что главной характеристикой атома является положительный заряд ядра.
В современной формулировке периодический закон звучит: свойства химических элементов, а также формулы и свойства образуемых ими соединений находятся в периодической зависимости от величины заряда ядер их атомов.
Физической основой структуры периодической системы элементов служит определённая последовательность формирования электронных конфигураций атомов по мере роста порядкового номера элемента.
В зависимости от того, какой энергетический подуровень заполняется электронами последним, различают 4 типа элементов:
![]() – элементы (последним заполняется
– элементы (последним заполняется ![]() -подуровень внешнего энергетического уровня)
-подуровень внешнего энергетического уровня)