Учебное пособие: Пояснення різних станів речовини з погляду атомно-молекулярного вчення
Властивості твердих тіл:
![]() Зберігають надану їм форму, об’єм.
Зберігають надану їм форму, об’єм.
![]() Характер молекулярного руху – коливання атомів та молекул відносно положення рівноваги.
Характер молекулярного руху – коливання атомів та молекул відносно положення рівноваги.
Мал.1
Розглянемо процеси, пов’язані із переходом речовини із одного агрегатного стану в інший:
1. Випаровування – процес перетворення рідини на пару. Воно відбувається за будь-якої температури.
(Запитання до учнів)
Поміркуйте: Відомо, що влітку, рідина надворі випаровується. Чи відбувається процес випаровування рідини взимку?
(Якщо учні не дійшли до правильного висновку, то вчителем наводяться приклади)
Наприклад, взимку білизна, хоч і довго, але поступово висихає; замерзлі калюжі поступово зникають. Отже, відбувається процес випаровування, інтенсивність якого залежить від температури: чим вища температура, тим швидше випаровується рідина.
2. Плавлення – процес перетворення твердого кристалічного тіла на рідину.
3. Кристалізація - процес перетворення рідини на тверде кристалічне тіло.
Численні приклади переходу речовини із одного агрегатного стану в інший, переконують нас у тому, що тверді тіла, рідини і гази – це не особливі речовини, яким властиві цілком певні ознаки, а стани, в яких може перебувати кожна речовина за певних фізичних умов.
Мотивація. Тоді постає запитання: „Чим пояснити можливість перебування речовини у трьох агрегатних станах?”
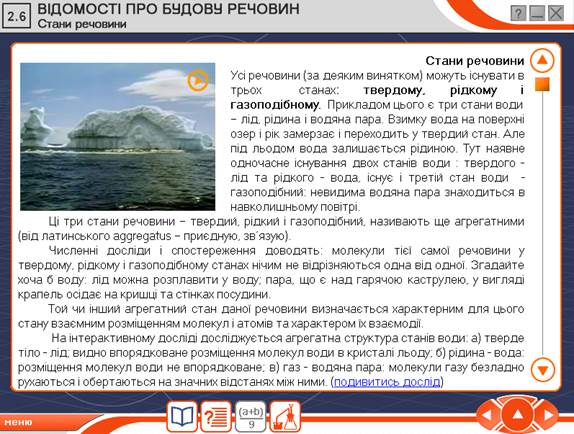
(Учні за допомогою програми проводять інтерактивний дослід агрегатної структури станів води. Див мал.2, мал.3, мал.4)


Мал. 2 Мал.3

Мал.4
(Розповідь учителя з елементами бесіди)
Очевидно, що в твердому стані речовина перебуває тоді, коли атоми і молекули взаємодіють настільки сильно, що знаходяться у чітко фіксованих положеннях. Вони практично не переміщуються, а лише хаотично коливаються відносно своїх стабільних положень. Треба докласти певних зусиль, щоб тіло змінило надану йому форму. Наприклад, можна розплющити залізний цвях ударами молотка; виліпити фігуру з пластиліну. Проте якщо ми спробуємо зігнути скло, воно розкришиться. Разом з тим відомо, що майстри-склодуви виробляють чудові художні вироби, попередньо нагрівши скло до певної температури. Ковалі розжарюють у горнах металеві заготівки, щоб вони були податливіші під час кування. Тобто властивості твердого тіла залежать також від його температури.
Якщо підвищувати температуру, то настане момент, коли тверде тіло почне плавитися і перетвориться на рідину. Підвищення температури твердого тіла веде до послаблення зв'язків між атомами і молекулами. Тобто атоми і молекули твердого тіла внаслідок нагрівання набувають такої рухливості, що вже можуть, як у рідинах, стрибкоподібно пересуватися. У кристалічних тілах (наприклад, металах) це відбувається за певної температури, яку називають температурою плавлення. Так, температура плавлення алюмінію дорівнює 660 °С, заліза — 1535 °С, вольфраму — 3387 °С.
Якщо рідину охолоджувати, молекули поступово втрачають рухливість, оскільки зв'язки між ними посилюються. Вони починають займати певні положення, продовжуючи коливатися відносно них. За певної температури відбувається кристалізація, або тверднення, — процес, зворотний до плавлення.
Що ж відбувається з рідиною зі зміною її температури?
Як відомо, молекули рідини взаємодіють таким чином, що утримуються одна біля одної, але не втрачають при цьому своєї рухливості. Вони коливаються і час від часу стрибкоподібно переміщуються, ніби просочуючись поміж сусідніми молекулами. Тому рідинам властива текучість і вони набувають форми посудини, в якій містяться.
Рідини випаровуються з вільної поверхні, яку вони утворюють на межі з газом. Це відбувається тоді, коли окремі молекули втрачають зв'язок з найближчими сусідами і починають вільно рухатися над поверхнею рідини.
Очевидно, що чим вища температура, тим більше молекул виривається з вільної поверхні рідини. Це підтверджує і наш життєвий досвід. Адже відомо, що в теплу погоду білизна висихає швидше, ніж у холодну.
Отже, перехід рідини у газоподібний стан відбувається внаслідок розриву зв'язків між її молекулами. Вони починають вільно рухатися в усьому наданому їм просторі, взаємодіючи лише під час короткочасних зіткнень. Ї х можна порівняти із співударом кульок, які розлітаються тим дужче, чим з більшою швидкістю наближаються одна до одної.
Якщо температура газу знижується, то швидкість хаотичного руху молекул зменшується. За цих умов може статися, що окремі молекули, наближаючись одна до одної, починають взаємодіяти і «злипаються» в маленькі крапельки. Відбувається конденсація — зворотний до випаровування процес, тобто перехід речовини із газоподібного в рідкий стан. Іноді цей процес називають скрапленням газу.
До опорного конспекту учнів:
Тверді тіла зберігають надану їм форму, оскільки атоми пов'язані між собою надто сильно.
Окремі властивості твердих тіл залежать від температури.