Дипломная работа: Распределение антигенов системы HLA у больных туберкулезом и здоровых представителей русской этнической группы Челябинской области
Рисунок 2. Трехмерное строение молекулы HLAII класса
Предполагают, что одни из этих участков расположены в пределах бороздки в положении, оптимальном для связывания антигена, а другие образуют детерминанты, вовлекаемые во взаимодействие с Т-клеточными рецепторами. В частности, было показано, что некоторые аминокислотные замены в полиморфных участках молекул HLA могут влиять на структурные изменения, значимые для образования "карманов", в которых связываются определенные презентируемые пептиды. Эти изменения могут даже полностью нарушать правильное связывание конкретного пептида, препятствуя его успешной презентации, а также влиять на корректное физиологическое распознавание комплекса "пептид-молекула HLA" Т-клетками. На основании полученных данных предположено, что стабильное взаимодействие молекул MHC II класса с пептидами зависит также и от плотности сети водородных связей между аминокислотными остатками альфа-спиралей молекулы MHC и связываемым пептидом. С другой стороны, установлено, что с CD4-рецепторами могут взаимодействовать и неполиморфные участки вторых доменов молекулы HLA (в данном случае HLA-DR). Таким образом, структура генов и молекул HLA обусловлена их биологическим предназначением [36].
Первичная функция HLA-II класса - представление чужеродного антигена иммунной системе для образования или подавления ответа Th, что, в конечном счете, ведет к производству антител против того же самого антигенного пептида. HLA DR найден на АПК (макрофаги, B-клетки и дендритные клетки). На поверхности клеток во время возбуждения увеличивается число антигенов DR, поэтому он является также маркером для иммунного возбуждения.
Существует чрезвычайно высокий уровень аллельного разнообразия в HLA DRB1, он стоит на втором месте после HLA-B. Эти 2 полиморфные области определяют все разнообразие последовательностей HLA в пределах человеческого генома. Это означает, что HLA-DRB1 развивается намного быстрее, чем все другие геномные локусы. Большая часть разновидностей в HLA DRB1 происходит в положениях контакта пептида в кармане, в результате многие из аллелей изменяют способ, которым DR связывает лиганды пептида и изменяет репертуар, который каждый рецептор может связать. Это свидетельствует о большом количестве изменений функционирующих в природе, и поэтому находится под действием отбора. В HLA области гены находятся в гетерозиготном состоянии или под давлением отбора, хотя некоторые аллели, возможно, находятся под положительным или отрицательным отбором.
HLA-DR и DQ локусы, вероятно, связаны с самым большим числом различных болезней относительно любых других локусов. Это происходит из-за сложной природы резистентности и высокого полиморфизма в этих локусах. Большинство этих болезней имеет низкую частоту, некоторые, подобно диабету 1 типа и целиакии являются редкими, но не исключениями.
Поскольку аллели DR находятся в неравновесном сцеплении с HLA-DQ локусами, отдельные изучения часто не могут определить точную ассоциацию с болезнью. В таких случаях используют трехлокусный гаплотип DR-DQA-DQB.
1.1.3 Многообразие функций системы HLA
Помимо того, что система HLA осуществляет регуляцию иммунного ответа на его начальных и продуктивных этапах, она также обеспечивает и такой "терминальный" этап регуляции, как апоптоз различных типов антиген-презентирующих клеток. При этом следует отметить, что этот эффект касается как профессиональных антиген-презентирующих клеток (макрофаги и CD34+ -клетки, дифференцировавшиеся из моноцитов в культуре клеток, и дендритные клетки), так и В-лимфоцитов.
Так, коллективом исследователей, работающих под руководством проф. D. Сharron, в самые последние годы было установлено, что блокирующее воздействие моноклонального антитела L243 на молекулы HLA-DR, экспрессированные на различных типах антиген-презентирующих клеток, блокирует их апоптоз, определяемый с помощью FITC-меченного аннексина V. Во всех указанных клетках после блокировки молекул DR отмечалось значительное снижение апоптоза. Авторы считают, что регуляция апоптоза дифференцирующихся антиген-представляющих клеток осуществляется через молекулы HLA-DR, и это может явиться решающим механизмом для ограничения их жизни.
Данные в целом свидетельствуют в пользу ключевой физиологической роли молекул HLA-DR в регуляции апоптоза всех типов антиген-презентующих клеток. Последнее, по сути, является регуляцией одного из важнейших этапов развития иммунного ответа и ещё раз свидетельствует в пользу того, что при современном уровне знаний о физиологической роли генов HLA-DR, можно считать, что именно в действительности являются генами иммунного ответа человека.
Генам главного комплекса гистосовместимости принадлежит ещё ряд важнейших физиологических функций. Описанию одной из них (генетическому контролю качества иммунного ответа) была посвящена работа, опубликованная в Российском физиологическом журнале им. И.М. Сеченова. Речь идет об ассоциированном с системой HLA контроле активности различных субпопуляций иммунокомпетентных клеток, что в свою очередь существенным образом сказывается на конечном уровне, т.е. на качестве иммунного ответа человека. При этом, естественно, следует помнить, что эта функция является "вторичной" и реализуется только в случае, если организм человека генетически способен отвечать на данный агент. Предпосылкой развития данного направления можно считать предположение, выдвинутое W. Bodmer и J. Bodmer еще в 1978 г., о том, что на формирование HLA-профиля европеоидной популяции в значительной степени оказали влияние имевшие место в средние века эпидемии таких заболеваний, как чума, оспа, холера и т.д. В результате этого среди выживших оказался значительный процент людей с определенными HLA-генотипами, в первую очередь с генотипом HLA-A1, - В8, - DR3. Этот генотип, как предположил W. Bodmer, обеспечивает более высокую резистентность к инфекционным заболеваниям и является на сегодняшний день генетическим маркером европеоидной популяции. Следует отметить, что это предположение было подтверждено на примере недавних вспышек брюшного тифа в Суринаме, когда среди выживших европеоидов значительный процент составили лица с гаплотипом HLA-A1, - В8, - DR3. Одновременно с этим W. Bodmer высказал справедливое предположение, что реализация этого эффекта могла быть связана только с ассоциациями между конкретными HLA-специфичностями и HLA-гаплотипами и иммунным ответом. Учитывая тот факт, что с одними и теми же гаплотипами HLA оказалась связана устойчивость к самым различным инфекционным агентам, логично было предположить, что подобного рода ассоциация с HLA может быть связана не только с самой генетически обусловленной отвечаемостью к конкретному инфекционному агенту, но и с теми звеньями иммунного ответа, которые принимают участие в его реализации, т.е. в конечном эффекте. Именно это в настоящее время и подразумевается под качеством иммунного ответа. И именно под таким названием в программу последнего рабочего совещания и конференции по HLA вошло новое отдельное направление изучения физиологической функции HLA. Следует отметить, что в данном направлении исследований отечественные иммунологи имеют несомненный приоритет, хотя само это направление ранее именовалось как исследование ассоциации между HLA и иммунным статусом человека [2].
К настоящему времени достаточно хорошо известно, что между отдельными HLA-специфичностями и HLA-гаплотипами существуют положительные и отрицательные ассоциации с теми или иными показателями иммунного статуса, такими как количество и функциональная активность клеток СD4+ , CD8+ , EKK, фагоцитирующей функцией нейтрофилов и т.д.
Отдельно следует отметить, что, как стало известно в самое последнее время, главному комплексу гистосовместимости принадлежит существенная роль в регуляции активности популяции клеток, стоящих "на грани" между факторами, определяющими специфический и неспецифический иммунитет. Это так называемые естественные клетки-киллеры (ЕКК).
Данной популяции клеток, как известно, принадлежит весьма существенная роль в обеспечении противоинфекционной, в первую очередь противовирусной защиты организма. Они также несут ответственность и за обеспечение элиминации из организма мутирующих, в том числе раковых клеток, которые распознаются ЕКК по отсутствию или даже снижению на их поверхности МНС-антигенов. При этом следует отметить, что роль в запуске активности ЕКК играет не только уровень экспрессии, но и их специфичность. Существуют данные о том, что в организме имеет место своего рода "приспособление" популяции ЕКК к HLA-генотипу. Это приспособление происходит в процессе дифференцировки ЕКК, когда из их популяции элиминируются клетки, рецепторы которых не связываются с антигенами HLA, входящими в генотип организма. Таким образом, исключается возможность повреждения собственных "нормальных" клеток, и активность ЕКК реализуется по отношению к клеткам с потерянной или ослабленной способностью экспрессии антигенов HLA.
Одной из важнейших физиологических функций системы HLA, которая, впрочем, довольно тесно связана и с ее основной (или, возможно, более известной) функцией - контролем иммунного ответа, является ее участие в репродукции человека. Одним из наиболее демонстративных проявлений является роль HLA-совместимости супругов в репродукции.
У человека система HLA создает условия, препятствующие появлению HLA-гомозиготного потомства, и, хотя медицинские мероприятия в ряде случае могут "преодолеть противодействие", в ряде случаев HLA-гомозиготные индивидуумы имеют повышенный риск развития целого ряда патологий.
Также гены главного комплекса гистосовместимости человека играют очень важную роль при пересадке тканей. Шансы на совместимость органа, пересаживаемого от родителя к ребёнку, составляет пятьдесят процентов. Когда органы пересаживаются между братьями и сестрами, вероятность, что антигены окажутся в основной массе одинаковыми, составляет двадцать пять процентов. Трансплантации между HLA-совместимыми братьями и сестрами или родителями и детьми даёт результаты столь же хорошие, как и при пересадке между однояйцевыми близнецами, то есть сто процентов [22].
Полученные данные совпадают с концепцией о том, что система HLA человека как наиболее полиморфная из генетических систем человека играет ведущую роль в обеспечении высокого уровня полиморфизма генома человека в целом.
Разумеется, при этом остается открытым вопрос, может ли система HLA в какой-то степени принимать участие в "предварительном", т.е. до супружества, выборе HLA-идентичных партнеров?
Использование молекулярных методов HLA-генотипирования, позволяющих исследовать HLA-полиморфизм на недоступном ранее уровне и выявлять HLA-гомозиготы без осуществления семейного типирования, возможно, даст ответ на этот вопрос, так как ранее выполненные работы, основанные на серологическом типировании HLA-DR, не смогли дать в этом отношении убедительных результатов.
1.1.4 Роль HLA в реализации иммунного ответа
Представления о строении системы HLA развивались и развиваются в течение всего периода ее изучения, однако, за последние годы произошел качественный скачок в развитии этой проблемы. Раньше, когда основным объектом исследования могли служить только белки-антигены HLA, представления о комплексе генов HLA могли формироваться в основном на анализе косвенных данных. Эти данные включали изучение антигенов HLA в популяциях, в семейном анализе, реакциях, субстратом которых были антигены HLA, и т.д. Теперь благодаря развитию молекулярной генетики и иммунохимии появилась возможность не только проводить тонкий анализ антигенов HLA, но и изучить сами гены HLA. Особенный прогресс в этом направлении произошел после открытия и внедрения в исследования в области изучения системы HLA метода полимеразной цепной реакции (ПЦР), позволяющего анализировать необходимые для исследований участки ДНК, что в свою очередь открывало широкие возможности для быстрого и точного анализа молекулярного полиморфизма HLA [31].
Внедрение в исследования системы HLA молекулярно-генетических методов не только позволило конкретизировать представления о системе HLA, но и значительно расширило представления о ее полиморфизме, что дало возможность более тщательного изучения ее функции. При этом были открыты многие новые аллели классов I, II и III, и общее количество только известных специфичностей HLA классов I и II увеличилось более чем в 6 раз.
В последнее время обнаружено, что антигены MIC-A, расположенные в непосредственной близости от HLA-B, участвуют в активации взаимодействия TcR-молекулы МНС в развитии Т-клеточно-опосредованной цитотоксичности и активности НК-клеток, тем самым, в частности, играя роль в обеспечении противоракового иммунитета.
В классе II основными локусами HLA являются DR, DQ и DP, а также открытые в более позднее время DM, LMP и ТАР. Три последних локуса обеспечивают такие важнейшие функции, как процессинг и экспрессия антигенов HLA на поверхности клеток. Класс III включает в себя гены, кодирующие факторы комплемента, фактор некроза опухолей и некоторые другие.
Физиологическая функция аллелей и кодируемых ими антигенов HLA, относящихся к различным классам HLA, в значительной степени различается. Так, антигены HLA классов I и II принимают участие во взаимодействии между иммунокомпетентными клетками в процессе иммунного ответа. Но антигенам класса I принадлежит также и физиологическая функция обеспечения взаимодействия между всеми другими ядросодержащими клетками организма, вплоть до взаимодействия нейрон-синапс. Тем самым с помощью системы HLA обеспечивается целостное функционирование не только иммунной системы человека, но и организма в целом [30].
Что касается обеспечения развития самого иммунного ответа, то роль антигенов системы HLA здесь первостепенна. Дело в том, что именно молекулы антигенов HLA обеспечивают презентацию, то есть представление иммунодоминантных пептидов, являющихся продуктом внутриклеточного протеолиза чужеродных антигенов, против которых и будет индуцирован, а затем и разовьётся иммунный ответ [19]. Этой функции антигенов системы HLA способствует само строение её молекул, которое, несмотря на выраженное различие в структуре строения молекулы антигенов HLA классов I и II, позволяет образовать на внешнем её конце так называемую пептид-связывающую бороздку, в которой и удерживается представляемый для распознавания пептид.
На рисунке 3 показана принципиальная схема представления пептидов антигенами HLA класса I (справа) и класса II (слева).
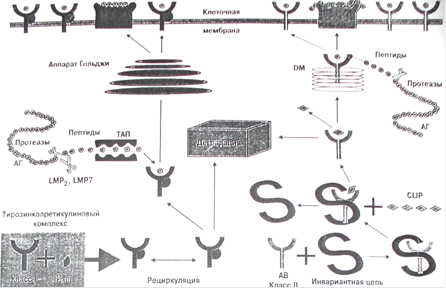
Рисунок 3. Схема представления пептидов молекулами HLA.
Общим для антигенов классов I и II является следующее. Антиген-представляющая клетка осуществляет свое специфическое взаимодействие, представляя пептид в контексте собственной HLA-молекулы, идентичной таковой на клетке, воспринимающей информацию. Именно за открытие этого феномена, названного феноменом двойного распознавания, Цинкернагель и Догерти получили Нобелевскую премию. Действительно, этот феномен явился ключевым моментом в понимании основ физиологической регуляции иммунного ответа. В то же время на рисунке 3 видны и существенные различия между взаимодействием, обеспечиваемым в процессе иммунного ответа антигенами HLA классов I и II. Во-первых, антигены HLA класса II обеспечивают взаимодействие антиген-презентирующей клетки с Т-хелпером, а антигены HLA класса I - с Т-эффектором/киллером. Во-вторых, помогают им в этом различные молекулы ко-рецепторы - CD4 для Т-хелперов и CD8 для Т-киллеров. Естественно, что различным явится и эффект этого взаимодействия. Так, распознавание пептидов в контексте молекулы HLA класса II ведет к формированию популяции Тh1 - и Тh2-клеток, одни из которых индуцируют развитие гуморального иммунного ответа, а другие явятся необходимым компонентом в индукции Т-киллеров. Что же касается антигенов гистосовместимости класса I, то Т-киллер, индуцированный против иммунодоминантного пептида, экспрессированного на поверхности клеток-мишеней в контексте антигенов HLA класса I, идентичного таковым, экспрессированным на Т-киллере, уничтожит их. Следует еще раз подчеркнуть, что оба эти важнейших звена "нормального", т.е. физиологического, иммунного ответа строго ограничены HLA-набором каждого конкретного человека.