Дипломная работа: Синтез и исследование сорбционных свойств гуанидинсодержащих полимерных нанокомпозитов
Двойные слоистые гидроксиды
M6 Al2 (OH)16 CO3 ·nH2 O; M=Mg, Zn
1.2 Структура слоистых алюмосиликатов и их физические и химические свойства
Природные слоистые алюмосиликаты, обычно используемые в нанокомпозитах, принадлежат к структурному семейству, известному, как 2:1-филосиликаты[6, 25, 26].
Атомные структуры обычно встречающихся глинистых минералов были весьма детально определены в результате работ многочисленных исследователей, которые при этом основывались на обобщениях Паулинга [27], сделанных им для структуры слюд и родственных им слоистых минералов.
В основе строения атомных решеток большинства глинистых минералов лежат два структурных элемента. Один структурный элемент состоит из двух слоев плотноупакованных атомов кислорода или гидроксильных групп, между которыми в октаэдрической координации расположены атомы алюминия, железа или магния, так что они равноудалены от 6 кислородов или гидроксилов (рис. 1). Если в этих положениях находятся атомы алюминия, они заполняют лишь две трети всех возможных положений, чтобы уравновесить структуру, которая в этом случае является структурой гидраргиллита и имеет формулу А12 (ОН)6 . При наличии магния заполненными оказываются все положения; уравновешенная структура является в этом случае структурой ору сита и характеризуется формулой Mg3 (OH)6 . Обычно расстояние О - О равно 2,60 Å , а расстояние ОН - ОН обычно 3 Å, однако в данном структурном элементе расстояние ОН - ОН имеет величину 2,94 Å, и пространство, доступное для иона в октаэдрической координации, имеет размер примерно 0,61 Å . Толщина этого структурного элемента в структурах глинистых минералов равна 5,06 Å. Второй элемент структуры построен из кремнекислородных тетраэдров. В каждом тетраэдре атом кремния равноудален от четырех атомов кислорода или гидроксильных групп в зависимости от требований баланса структуры, образованной тетраэдрами с атомами кремния в их центрах. Тетраэдрические группы кремнезема расположены в форме бесконечно повторяющейся гексагональной сетки, образующей слой состава Si4 О6 (OH)4 (рис. 1). Тетраэдры расположены так, что вершины каждого из них направлены в одну и ту же сторону, а основания находятся в одной и той же плоскости. В структуре этого слоя можно выделить три уровня. На первом уровне в виде ажурной сетки находятся атомы кислорода. На втором уровне находятся атомы кремния, каждый из которых лежит в выемке, образованной тремя соприкасающимися атомами кислорода первого уровня, вследствие чего они в своей совокупности образуют гексагональную сетку. На третьем уровне находятся гидроксильные группы, причем каждый гидроксил расположен в вершине тетраэдра прямо над атомом кремния. Гранецентрированная гексагональная сетка может рассматриваться как образованная тремя системами рядов атомов кислорода, пересекающихся под углом в 120°. Расстояние О - О в тетраэдрическом слое равно 2,55 Å , а пространство, доступное для иона, в тетраэдрической координации имеет размер примерно в 0,55 Å . Толщина этого структурного элемента в структурах глинистых минералов — 4,93 Å ; каждый из них имеет расстояние от центра до центра примерно 2,1 Å [28].
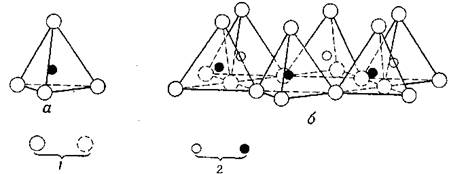
Рис. 1.1. Схематическое изображение отдельного кремнекислородного тетраэдра (а) и сетки кремнекислородных тетраэдров, расположенных по гексагональному мотиву (б): 1 – атомы кислорода; 2 – атомы кремния
Некоторые глинистые минералы являются волокнистыми и построены из структурных элементов, отличных от описанных выше. По своим структурным особенностям эти минералы подобны амфиболам, и их основные структурные элементы состоят из кремниевых тетраэдров, расположенных в форме двойной цепи состава Si4 О11 , как показано на рис. 2. Структура этого элемента подобна структуре слоя из кремнекислородных тетраэдров в слоистых минералах с тем лишь отличием, что она имеет бесконечную протяженность только в одном направлении. В другом направлении она распространена лишь примерно на 11,5 Å. Цепи связаны вместе атомами алюминия или магния, расположенными так, что каждый из них окружен шестью «активными» атомами кислорода. Активными являются те атомы кислорода, которые имеют лишь одну связь с кремнием и, следовательно, находятся на краях цепей и в вершинах тетраэдров [29].
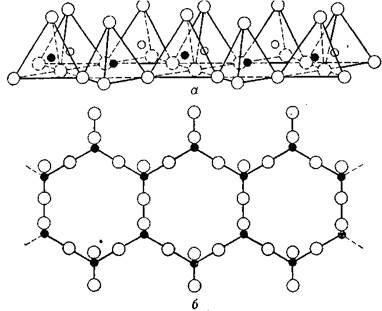
Рис. 1.2. Схематическое сдвоенных цепей кремнекислородных тетраэдров, характерных для амфиболевого структурного типа глинистых минералов. а – в перспективе;
б – в проекции на плоскость основания тетраэдров
1.2.1 Монтмориллонитовые минералы
Монтмориллонитовые минералы встречаются лишь в виде частиц крайне малого размера, так что они не могут быть исследованы рентгеновскими методами, пригодными для изучения монокристаллов. Концепции об их структуре, таким образом, должны основываться на данных порошковых рентгенограмм и учете особенностей более детально изученных структур. В связи с этим имеется неопределенность в отношении структуры монтмориллонита.
Представления о характере структуры монтмориллонитовых минералов впервые высказали в 1933 г. Гофманом, Энделл и Вилмом. В дальнейшем они были несколько изменены, согласно гипотезам Мегдсфрау и Гофмана [27], Маршалла [30] и Хендрикса [28]. Согласно этим представлениям, монтмориллонит состоит из структурных элементов, построенных из двух наружных кремнекислородных тетраэдрических сеток и промежуточной алюмокислородной октаэдрической сетки. Все вершины тетраэдров в сетке направлены в одну и ту же сторону — к средней части структурного элемента. Тетраэдрические и октаэдрические сетки сочленены друг с другом таким образом, что вершины тетраэдров каждой кремнекислородной сетки совместно с вершинами слоев гидроксилов октаэдрической сетки образуют общий слой. В вершинах, общих для тетраэдрических и октаэдрических. сеток, располагаются вместо гидроксильных групп ОН атомы О. Слои являются непрерывными в направлениях а и b и наложены друг на друга в направлении с.
Во взаимном расположении кремне- и алюмокремнекислородных слоев слои атомов кислорода каждого структурного элемента являются смежными со слоями атомов кислорода соседних структурных элементов, вследствие чего между ними существует очень слабая связь и в минерале наблюдается прекрасная спайность. Характерной особенностью структуры монтмориллонита является то, что молекулы воды и другие полярные молекулы, например некоторые органические молекулы, могут проникать между структурными слоями, вызывая расширение решетки в направлении оси с. В связи с этим величина периода с не является постоянной, а изменяется, начиная примерно с 9,6 Å , когда между структурными слоями нет никаких полярных молекул, до полного, в некоторых случаях материального разобщения отдельных слоев. На рис. 3. схематически изображена структура монтмориллонита такого типа. Обменные катионы находятся между силикатными слоями, и межплоскостное расстояние вдоль оси с полностью дегидратированного монтмориллонита в некоторой степени зависит от размера межслоеных катионов: оно тем больше, чем больше по своим размерам катионы. В случае адсорбции полярных органических молекул между силикатными слоями величина периода с также изменяется и зависимости от размера и геометрии органической молекулы. Толщина водных слоев, расположенных между силикатными структурными слоями, при данном давлении паров воды зависит от природы обменных катионов.
В нормальных условиях монтмориллонит с Na+ в качестве обменного нона обычно имеет между силикатными слоями один слой молекул воды; межплоскостное расстояние в направлении оси с примерно равно 12,5 Å. Монтмориллонит с Са++ обычно содержит два молекулярных слоя воды и имеет межплоскостное расстояние в направлении оси с 15,5 А. Свойства разбухания монтмориллонитов являются обратимыми. Однако если структура полностью сжата при удалении всех межслоевых полярных молекул, повторное набухание может происходить с трудом.
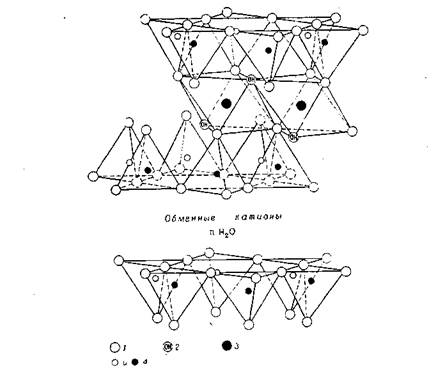
Рис. 1.3. Схематическое изображение структуры монтмориллонита (по Гофману, Энделлу, Вилму, Маршаллу и Хендриксу)
Опыты Меринга [31] и других авторов [32] с монтмориллонитом (в присутствии большого количества воды) указывают, что при одних поглощенных катионах, например Nа+ , структурные слои могут полностью разойтись, а при других катионах, таких, как Са++ и Н+ , разделение слоев не является полным.
Как впервые было отмечено Маршаллом [30] и Хендриксом [28], состав монтмориллонита всегда отличается от состава, выражаемого вышеприведенной теоретической формулой, вследствие замещения в пределах решетки кремния в тетраэдрической координации алюминием и, возможно, фосфором или алюминия в октаэдрической сетке магнием, железом, цинком, никелем, литием и т. д. В тетраэдрической сетке замещение Si4+ на А13 + ограничено, по-видимому, 15%. Согласно приведенной выше формуле, в монтмориллоните заполнены лишь две трети возможных положений в октаэдрической сетке. Замещение А13+ на Mg2+ может быть в соотношении один к одному или 2А13+ на 3Mg+2 , причем в последнем случае заполняются все октаэдрические положения. В октаэдрической сетке степень замещения изменяется от самых малых значений вплоть до полного замещения. Полное замещение 2А13+ на 3Mg2+ дает минерал сапонит; замещение алюминия железом — нонтронит; хромом — волконскоит, цинком — соконит.
Радиус иона Mg++ равен 0,65Å , а иона Fe3+ — 0,67Å . Эти ионы слишком велики, чтобы строго соответствовать решетке монтмориллонита; в результате монтмориллонитовые минералы со значительными замещениями этими ионами подвержены направленным напряжениям, проявляющимся в удлиненной щепкоподобной или игольчатой форме частиц.
Слоистые минералы, у которых все возможные октаэдрические положения заполнены, в общем случае называются октафиллитами, или триоктаэдрическими, тогда как минералы, у которых заполнены лишь две трети возможных октаэдрических положений, называются гептафиллитами, или диоктаэдрическими. Многочисленные анализы монтмориллонита доказали, что благодаря замещениям в пределах октаэдрического слоя этот минерал является либо триоктаэдрическим, либо диоктаэдричсским. Росс и Хендрикс [27] произвели пересчеты большого числа химических - анализов монтмориллонита для приведения их в соответствие с его структурой. К сожалению, эти пересчеты не сопровождаются структурными данными и некоторые из образцов могут оказаться смесью глинистых минералов. Однако выводы, сделанные на основании этих анализов, можно считать правильными, так как количество анализов достаточно велико. Согласно Россу и Хендриксу, число ионов в шестерной координации, т. е. ионов октаэдрических положений, находится в двух пределах: от 4.00 до 4,44 и от 5.76 до 6,00. Далее, если минерал является диоктаэдрическим, то для него, по-видимому, возможна значительная вариация точного расположения алюминия и других атомов ни всем возможным октаэдрическим положениям.
Другое обстоятельство, в силу которого монтмориллонит всегда отличается от идеальной формы, выражаемой его теоретической формулой, заключается в том, что его решетка вследствие указанных выше замещений Аl3+ на Mg++ , Si4+ на Аl3+ и т. д. всегда неуравновешенна. Такая неуравновешенность может обусловливаться замещениями ионов разной валентности как в тетраэдрической, так и в октаэдрической сетках. Неуравновешенность в одной из этих сеток может компенсироваться частично (но лишь частично) замещениями в других сетках структурного слоя. Так, замещения Si4+ на Аl3+ могут быть частично компенсированы за счет заполнения более двух третей октаэдрических положений. Компенсация может также происходить благодаря замещениям атомов кислорода октаэдрического слоя на группы ОН. Существенно, что замещения в решетке монтмориллонита совместно с внутренними компенсирующими замещениями всегда вызывают почти один и тот же результирующий отрицательный заряд решетки. Согласно данным многих анализов, такой заряд равен примерно 0,66 на элементарную ячейку. Результирующий отрицательный заряд уравновешивается обменными катионами, адсорбированными между структурными слоями и вокруг их краев (ионный обмен), и равен примерно двум третям единицы на элементарную ячейку. Для его достижения требуется, например, замещение каждого шестого А13+ на Mg2+ или каждого шестого Si4+ на А13+ .
Отрицательный заряд монтмориллонита, синтезированного из чистых водных смесей окиси магния и кремнезема, не мог быть вызван замещениями в решетке. Он мог быть обусловлен наличием вакантных мест в решетке; такие вакантные места, возможно, имеются у естественных минералов.
Росс и Хендрикс [27] по данным химического анализа вычислили структурные формулы многих монтмориллонитов, что позволило установить пределы замещений в решетке и характер частично компенсирующих замещений в структуре. Номенклатура минералов монтмориллонитовой группы зависит от характера изоморфных замещений в решетке. В табл. 1.1 приведены, согласно Россу и Хендриксу [27], наименования монтмориллонитов и соответствующие им структурные химические формулы.
Таблица 1.2.
Формулы некоторых членов монтмориллонитовой группы, выведенные Россом и Хендриксом
|
Диоктаэдрические (гептафиллитовые) монтмориллониты | |
|
монмориллонит |
(ОН)4 Si3 (Al3,34 Mg0,66 {Na0,66 })O20 |
|
К-во Просмотров: 364
Бесплатно скачать Дипломная работа: Синтез и исследование сорбционных свойств гуанидинсодержащих полимерных нанокомпозитов
| |