Курсовая работа: Биогенез мембран
Некоторые небольшие белки (<8,5 кДа) транспортируются в эндоплазматический ретикулум независимо от СРЧ. В их число входят препропептид GLa лягушки, препромелиттин (оба они являются предшественниками секретируемых белков) и пробелок оболочки фага М13. Во всех этих примерах конформация предшественника такова, что белки должны оставаться способными к переносу даже в отсутствие СРЧ и рибосом.
2. Рецептор СРЧ, или стыковочный белок. Комплекс СРЧ/ рибосома/образующаяся полипептидная цепь транспортируется в шероховатый эндоплазматический ретикулум, преодолевая энергию сильного взаимодействия между СРЧ и мембраносвязанным рецептором СРЧ, называемым также стыковочным белком. Рецептор СРЧ содержит субъединицу с мол. массой 73 кДа, присоединенную N-концом к мембране. Вероятно, рибосома также связывается со специфическими рецепторами, присутствующими в мембране.
3. Рецептор сигнальной последовательности. Сигнальная последовательность на образующейся полипептидной цепи перемещается от СРЧ ко второму рецептору, находящемуся в мембране и называемому рецептором сигнальной последовательности. Об этом свидетельствуют результаты опытов по фотохимическому сшиванию, в которых используется метка, связанная с сигнальной последовательностью препролактина. Предполагаемый мембраносвязанный рецептор представляет собой гликопротеин с мол. массой 35 кДа. Возможно, он образует часть канала, через который осуществляется перенос. С помощью такого же подхода с использованием поперечной сшивки и синтетического сигнального пептида был обнаружен еще один кандидат на роль рецептора сигнальной последовательности (45 кДа). Связь между этими двумя белками неизвестна и функции их до конца не установлены. Как только образовавшаяся полипептидная цепь связывается с мем-браносвязанным рецептором, СРЧ и ее рецептор могут освободиться от рибосомы и принять участие в новом цикле. О предполагаемом канале, участвующем в переносе, ничего не известно; очистка его является довольно сложной задачей.
3 Липиды
После рассмотрения механизмов синтеза транспорта и встраивания мембранных белков необходимо рассмотреть и процессы происходящие с липидами мембран.
В мембранах эукариотических клеток обнаружено огромное количество разных липидов, причем они не распределены равномерно по разным клеточным мембранам. Эта неравномерность относится к распределению как полярных головок, так и ацильных хвостов. Например, степень ненасыщенности фосфолипидов в общем случае уменьшается при переходе от эндоплазматического ретикулума к комплексу Гольджи и затем к плазматической мембране. Для животной клетки среднее молярное отношение холестеролфосфолипиды равно 0,3— 0,4, при этом для плазматической мембраны оно гораздо выше (0,8—0,9), чем для других мембран, таких, как шероховатый эндоплазматический ретикулум (около 0,1). Кроме того, для многих мембран характерно неравномерное распределение липидов и по разным половинам бислоя.
Вопрос о механизме создания и поддержания такой асимметрии очень интересен и сложен. Напомним, что многие мембраны эукариотических клеток участвуют в эндоцитозе и экзоцитозе, при которых от одних мембран везикулы отпочковываются, а с другими сливаются. Этот процесс селективен для белков, которые транспортируются с помощью везикул, но почему-то не приводит к идентичности липидного состава вовлекаемых в него мембран. Причина этого явления неизвестна, выяснены лишь некоторые его аспекты. Рассмотрим, где синтезируются мембранные липиды, а затем обсудим, как они могут транспортироваться к месту назначения.
3.1 Прокариоты
У Е. coli весь синтез фосфолипидов протекает в плазматической мембране. В общих чертах этот процесс представлен на рис.4. Жирные кислоты синтезируются в виде предшественников, ковалеитно связанных с белком — переносчиком ацила, а затем включаются в мембрану путем ацилирования с образованием CDP-диацилглицерола. Два ацилирующих фермента рис.4 проявляют предпочтение к ненасыщенным жирнокислотным группам, находящимся в положении sn -2. На уровне CDP-диацилглицерола происходит разветвление процесса, после чего образуется фосфатидилсерин или фосфатидилглицерол рис.4. Механизм регуляции равновесного соотношения между фосфолипи-дами почти не изучен. В штаммах, в которых фермент, необходимый для биосинтеза кардиолипина, синтезируется в количествах, в 10 раз превышающих норму, наблюдается лишь незначительное увеличение содержания этого фосфолипида в мембране.
Аналогичные результаты были получены для фосфатидилсеринсинтазы и фосфатидилглицеролфосфатсинтазы . Сверхпродукция этих ферментов оказывает лишь небольшое влияние на фосфолипидный состав мембраны. С другой стороны, полное отсутствие фосфатидилглицеролфосфатсинтазы губительно для клетки, вероятно, потому, что кислые фосфолипиды необходимы для обеспечения предшественниками других биосинтетических реакций или участвуют в регуляции.
Получены мутанты, содержащие очень мало фосфатидилглицеролфосфатсинтазы, у которых единственным основным фосфолипидом является фосфатидилэтаноламин. Очищены некоторые ферменты биосинтетического пути, в том числе CDP-диглицеридсинтаза и фосфатидилсеринсинтаза. Первый фермент, как и ожидалось, связан с мембранами, но фосфатидилсеринсинтаза связана с рибосомами в бесклеточных экстрактах.
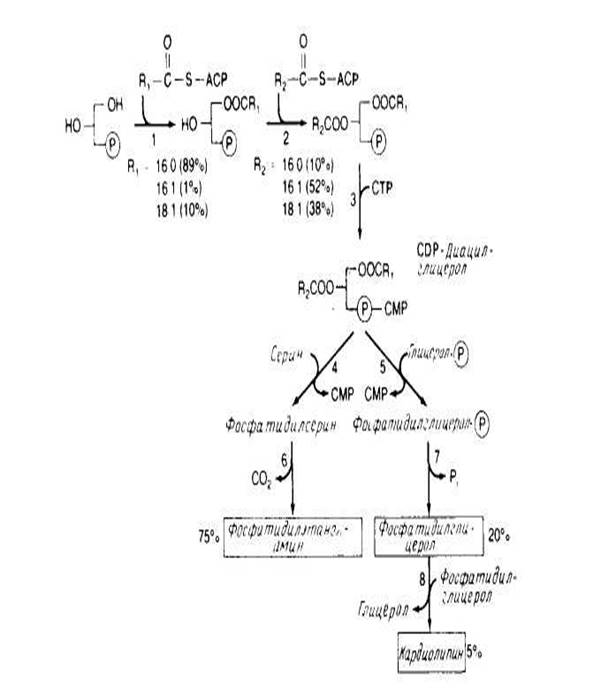
Рис.4 Синтез липидов у прокариот
3.2 У эукариот
На рис.5 представлена более сложная суммарная схема биосинтеза фосфолипидов в эукариотических клетках. Синтез жирных кислот происходит как в эндоплазматическом ретикулуме, так и в митохондриях. В качестве субстрата используется ацил-СоА, поскольку животные клетки не содержат эквивалента белку — переносчику ацила. Большинство ферментов, участвующих в биосинтезе фосфолипидов, локализовано на цитоплазматической стороне мембраны эндоплазматического ретикулума, но есть и исключения. В эукариотических клетках, как и в Е. coli , синтез фосфатидилглицерола и карднолипина может осуществляться через промежуточное образование CDP-диацилглицерола.
Однако ферменты, необходимые для этого, содержатся во внутренней мембране митохондрий, и эти фосфолипиды обнаруживаются только в митохондриях. Низшие эукариоты (например, дрожжи) тоже могут синтезировать фосфатидилсерин с помощью механизма, используемого Е. coli , но соответствующий фермент обнаружен как в эндоплазматическом ретикулуме, так и в митохондриях. В дрожжах на долю фосфатидилсерина приходится только около 5% всех фосфолипидов, но он является предшественником фосфатидилэтаноламина и фосфатидилхолина.Эукариоты, в том числе и дрожжи, могут синтезировать фосфа-тидилэтаноламин и фосфатидилхолин в ходе реакции с участием 1,2-днацилглицерола (рис. 5).
Это основной путь синтеза фосфолипидов в животных клетках. Затем специальные ферменты, находящиеся в эидоплазматическом ретикулуме высших эукариот (но ие дрожжей), катализируют реакцию обмена полярных головок, в результате чего образуется фосфатидилсерин. Эта реакция необходима высшим эукариотам для получения фосфатидилсерииа. После образования в эидоплазматическом ретикулуме фосфатидилсерин декарбоксилируется (по кра