Курсовая работа: Кинетическое и термодинамическое исследование физико-химических процессов
Чувствительность оптических методов анализа может быть значительно повышена, если в качестве рецептора применить фотоумножители вместо обычных фотоэлементов.
Для измерения скорости реакции можно применять также турбидиметрические и нефелометрические методы. В качестве примера приведем реакцию окисления тиосульфат-иона перекисью водорода с образованием сульфат-иона:
4Н2O2 + S2O32- = 3H2O + 2SO42- + 2H+
В исследуемый раствор вводят хлорид бария и желатин. Образующийся при этой реакции сульфат-ион дает суспензию BaSO4, оптическая плотность которой может быть измерена на фотоэлектроколориметре. Но так как оптическая плотность суспензии пропорциональна концентрации сульфат-иона в растворе, то все приведенные выше рассуждения применимы и к этому случаю.
Применение люминесцентного метода определения скорости химической реакции весьма перспективно, так как вследствие большой чувствительности метода по изменению люминесценции раствора можно определять очень малые изменения концентрации реагентов в растворе. В качестве индикаторной была выбрана реакция окисления флуоресцирующего вещества — стильбексона перекисью водорода. Эта реакция катализируется железом.
О скорости реакции можно судить по изменению величины lgI0/I во времени (I0 и I - интенсивность флуоресценции в начальный и в данный момент времени, соответственно).
При каталитических реакциях, сопровождающихся хемилюминесценцией, скорость реакции также может быть измерена методом люминесцентного анализа. Так, например, А. К. Бабко и Н. М. Луковская при изучении реакции между перекисью водорода и люминолом в присутствии солей меди применяли фотографический метод оценки интенсивности свечения. При действии выделяющегося при хемилюминесценции света на фотопластинку происходит ее почернение (после проявления и фиксирования). Интенсивность почернения зависит от концентрации реагирующих веществ.
Применение потенциометрического метода измерения скорости химических реакций изучено на реакции окисления тиосульфат-ионов ионами железа (III), которая катализируется солями меди.
В этом случае можно применять платиновый электрод в качестве индикаторного и для измерения скорости реакции использовать концентрационную цепь.
При полярографическом методе измерения скоростей химических реакций используют зависимость между силой диффузионного тока и концентрацией определяемого вещества. Так, за изменением концентрации хромовой кислоты в процессе ее восстановления можно следить по величине диффузионного полярографического тока.
Даже небольшие изменения в соотношении концентраций иодида и иода в растворе можно регистрировать амперометрически при помощи двух платиновых индикаторных электродов. Сила тока в системе зависит от концентрации иода, выделяющегося при окислении иодида.
Такую систему, следовательно, можно использовать для измерения скорости выделения иода из иодида при окислении его, например, перекисью водорода. Скорость этой реакции, как известно, зависит от концентрации катализаторов (молибдена, вольфрама и др.) в растворе. При протекании реакции в растворе сила тока линейно изменяется во времени. По тангенсу угла наклона прямой время—сила тока можно найти скорость соответствующей реакции и определить концентрацию элемента-катализатора в растворе.
2. Термодинамический вывод диаграммы состояния
При исследовании систем, состоящих из двух или большего числа химических индивидов, главную роль играет зависимость свойств системы от cостава. Измеряется то или иное свойство для смесей или растворов различного состава, по возможности от 0 до 100 % каждого из исходных индивидов, и строится диаграмма состав - свойство или эта зависимость дается аналитически. Несмотря на то, что последний способ представления результатов является более высокой ступенью в обработке результатов измерения, в физико-химическом анализе пока используется преимущественно графический метод. Геометрический образ — диаграмма — отражает, какие процессы прошли в системе: образовались ли механические смеси, твердые или жидкие растворы, возникли ли новые соединения и т. д. По диаграмме также определяются границы существования различных фаз в системе. Анализ диаграммы позволяет выявить не столь резко выраженные процессы и отметить слабые межчастичные взаимодействия, которые не приводят к образованию новых соединений или распаду имеющихся.
Естественно, в одном реферате рассмотреть все диаграммы состояния для всех систем просто невозможно. Поэтому, в качестве примера мы решили рассмотреть диаграммы состояния двойных конденсированных систем без превращений в твердых фазах.
2.1. Термодинамический вывод диаграммы состояния системы с простой эвтектикой
Рассмотрим изотермы удельных изобарных потенциалов расплавов двойной системы В—А для разных температур. Установим, какие фазы находятся в равновесии при той или иной температуре, и построим диаграмму зависимости температур от состава системы, т. е. диаграмму состояния.
На рис.I изображены изотермические диаграммы удельного изобарного потенциала этой системы в жидком состоянии для температур t1 › t2 › t3 › t4 › t5 › t6 (диаграммы I—VI; VII — полученная из них диаграмма состояния). Точками Аs и Вs на всех диаграммах обозначены удельные изобарные потенциалы компонентов в твердом состоянии. Точки Al и Bl (концевые точки кривых) относятся к тем же компонентам в жидком состоянии.
Пусть температура t1 выше температуры плавления более высокоплавкого компонента А. При этой температуре точки Аs и Вs лежат соответственно выше точек Al и Bl (диаграмма I). Следовательно, смеси всех составов при температуре t1 будут в жидком состояни. При понижении температуры изобарный потенциал возрастает, так как dG/dT =-S, где S — энтропия, величина всегда положительная. Энтропия одного и того же вещества в жидком состоянии больше, чем в твердом при той же температуре, поэтому с понижением температуры изобарный потенциал жидкости возрастает быстрее, чем твердого тела. Вследствие этого при более низких температурах устойчиво твердое вещество. Эти различия в температурном ходе изобарного потенциала твердых и жидких веществ обусловливают и вывод диаграммы с начала кристаллизации расплавов, для которого важно относительное движение точек Аs (Вs) и Al (Bl). При понижении температуры точка Аs, сближается с точкой Al, а точка Вs — с Bl, и при температуре плавления компонента А (t2) точки Аs и Al совпадают, точка же Вs лежит пока еще выше Bl, и при температуре t2 компонент В находится в расплавленном состоянии (диаграмма II).
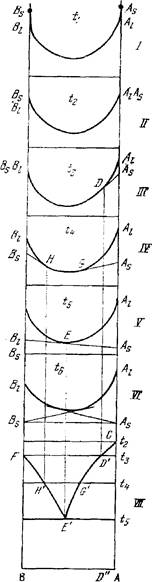
Рис.1. Вывод диаграммы состояния двойной системы с простой эвтектикой из изотермы изобарного потенциала.
Диаграмма III соответствует t3 - температуре плавления компонента В; точки Вs, и Bl; совпадают. Точка Аs находится ниже Al. Проведем из точки Аs касательную к кривой и через точку касания D — вертикальную линию. Отметим на диаграмме состояния (диаграмма VII) температуру t3 и проведем соответствующую ей изотермическую прямую F t3. Точка пересечения прямой F t3 с указанной выше вертикальной прямой (точка D') указывает температуру начала затвердевания системы с составом, изображаемым точкой D. Кроме того, отметим на диаграмме точки плавления компонентов А и В (точки С и F).
При дальнейшем понижении температуры до t4 (диаграмма IV), которая немного ниже температуры плавления более низкоплавкого компонента В, обе точки Аs и Вs, по сравнению с Al и Bl окажутся еще ниже, чем при температуре t3. Из этих точек можно провести касательные к кривой, причем точки касания G и Н дают составы растворов, находящихся при этой температуре в равновесии с твердым А и соответственно с твердым В. Точка G, как легко видеть, будет лежать левее, чем точка D диаграммы VII. Пользуясь диаграммой VII, получим соответствующие точки Н' и С' на диаграмме состояния при помощи описанного выше приема. При продолжающемся падении температуры точки Аs и Вs будут претерпевать дальнейшее понижение относительно Al и Bl, вследствие чего точки касания G и Н будут двигаться навстречу друг другу (первая налево, а вторая направо). Наконец, при температуре t5 (диаграмма V), когда обе точки касания встретятся в точке Е, обе касательные сольются в одну прямую. Это означает, что при этой температуре оба твердых компонента находятся в равновесии с одним и тем же раствором, состав которого дается точкой Е. Перенесем уже описанным способом точку Е на диаграмму состояния и получим точку Е'.
Если соединить точки, полученные указанным выше способом на диаграммеме VII, то получим две линии температур начала затвердевания: FН'Е’, отвечающую выделению компонента В, и CD’G'Е', отвечающую выделению компонента А. Таким образом, кривая температур начала кристаллизации диаграммы состояния окажется построенной. Эта кривая называется ликвидусом и состоит из двух ветвей, соответствующих кристаллизации того и другого компонента. Ветви пересекаются в точке Е', которая будет изображать состояние раствора (расплава), находящегося в равновесии одновременно с твердыми В и А. Раствор, находящийся в равновесии с двумя твердыми фазами, называется двояконасыщенным. При продолжающемся отнятии теплоты от системы температура и состав жидкости, состояние которой определяется течкой Е', постоянны. Расплав Е' называется эвтектическим или жидкой эвтектикой. Затвердевшая жидкая эвтектика называется твердой эвтектикой ( по валовому составу они тождественны), а температура, при которой такая эвтектика затвердевает,— эвтектической температурой. Точка Е' изображающая состояние жидкой эвтектики (фигуративная точка жидкой эвтектики), называется эвтектической точкой. Когда это не может повести к недоразумению, употребляют один термин — эвтектика, объединяя и температуру, и состав эвтектической точки. Так как в эвтектике двойной системы число компонентов равно двум, число фаз — трем, а давление постоянно, то эта точка нонвариантная (точнее, условно-нонвариантная).
Вернемся к рис.1. При дальнейшем понижении температуры (диаграмма VI) точки Аs и Вs и соединяющая их прямая еще более опустятся по отношению к кривой. Из этих точек можно, конечно, провести касательные к кривой и определить, таким образом, растворы, находящиеся в равновесии с твердыми А и В. Однако эти равновесия отвечают неустойчивым состояниям, что соответствует возможности продолжить кривую плавкости за эвтектическую точку. В устойчивых же состояниях будут находиться механические смеси твердых А и В, так как при данном составе удельный изобарный потенциал смеси будет меньше, чем смеси твердых А или В с находящимися с ними в равновесии растворами.
Список литературы
К.Б. Яцимирский ″Кинетические методы анализа″, М.:″ Химия″ 1967г
В.Я. Аносов, М.И. Озерова, Ю.Я. Фиалков ″Основы физико-химического анализа″, М.: ″Наука″,1976