Курсовая работа: Прикладные аспекты темы Скорость химической реакции и катализ на уроках химии в средней школе
если равновесная концентрация углекислого газа равна 0,02 моль/л, водорода – 0,005 моль/л, а угарного газа и воды – по 0,01 моль/л.

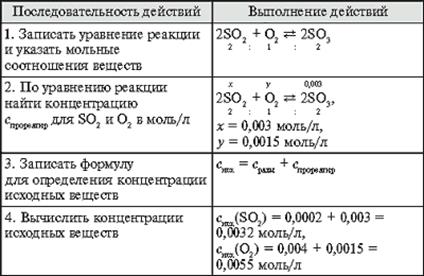
Алгоритм 11. Вычисление исходных концентраций веществ
Задача. Обратимая реакция выражается уравнением
2SO2 + O2 ![]() 2SO3 .
2SO3 .
Известны равновесные концентрации: для оксида серы(IV) – 0,0002 моль/л, для кислорода – 0,004 моль/л, для оксида серы(VI) – 0,003 моль/л. Найдите исходные концентрации кислорода и сернистого газа.
Задания для самоконтроля
1. Уравнение реакции
Н2 + I2 ![]() 2HI.
2HI.
Даны равновесные концентрации: водорода – 0,004 моль/л, йода – 0,25 моль/л, йодоводорода – 0,08 моль/л. Вычислить исходные концентрации водорода и йода и константу равновесия.
Ответ. [H2 ] = 0,044 моль/л, [I2 ] = 0,29 моль/л, К = 6,4.
2. Как изменится давление к моменту наступления равновесия в реакции N2 + 3Н2 ![]() 2NН3 ,протекающей в закрытом сосуде при постоянной температуре, если начальные концентрации азота и водорода равны соответственно 2 и 6 моль/л и если равновесие наступает тогда, когда прореагирует 10% первоначального количества азота?
2NН3 ,протекающей в закрытом сосуде при постоянной температуре, если начальные концентрации азота и водорода равны соответственно 2 и 6 моль/л и если равновесие наступает тогда, когда прореагирует 10% первоначального количества азота?
Ответ. Уменьшится в 1,05 раза.
3. В какую сторону сместится равновесие реакций:
2H2 S ![]() 2Н2 + 2S – Q,
2Н2 + 2S – Q,
N2 O4 ![]() 2NO2 – Q,
2NO2 – Q,
CO + H2 O (г.) ![]() СО2 + Н2 + Q,
СО2 + Н2 + Q,
а) при понижении температуры;
б) при повышении давления?
Ответ. Смещение равновесия в реакциях:
а) при понижении температуры:
2Н2 S ![]() 2Н2 + 2S – Q – влево,
2Н2 + 2S – Q – влево,
N2 O4 ![]() 2NO2 – Q – влево,
2NO2 – Q – влево,
CO + H2 O (г.) ![]() СО2 + Н2 + Q – вправо;
СО2 + Н2 + Q – вправо;
б) при повышении давления:
2Н2 S ![]() 2Н2 + 2S – Q – не сместится,
2Н2 + 2S – Q – не сместится,
N2 O4 ![]() 2NO2 – Q – влево,
2NO2 – Q – влево,
CO + H2 O (г.) ![]() СО2 + Н2 + Q – не сместится [5].
СО2 + Н2 + Q – не сместится [5].
1.2 Практическая работа «Действие катализаторов »