Курсовая работа: Состав атмосферы и его формирование в процессе эволюции биосферы
В тропосфере сероводород неустойчив и в результате реакции с кислородом воздуха преобразуется в S![]() . Хотя эта реакция в изолированных условиях протекает достаточно медленно, однако присутствие в тропосфере аэрозолей и мельчайших капелек воды резко ускоряет ее прохождение[1].
. Хотя эта реакция в изолированных условиях протекает достаточно медленно, однако присутствие в тропосфере аэрозолей и мельчайших капелек воды резко ускоряет ее прохождение[1].
Повышение концентрации 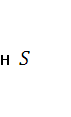 в воздухе представляет опасность для здоровья и даже жизни живых существ, в том числе и человека. В этой связи промышленные источники, выделяющие в составе отходов
в воздухе представляет опасность для здоровья и даже жизни живых существ, в том числе и человека. В этой связи промышленные источники, выделяющие в составе отходов 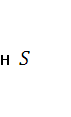 , должны строго контролироваться. К их числу относится ряд химических производств, в том числе процессы переработки каменных углей, осуществляемые без доступ воздуха, и т. д[1].
, должны строго контролироваться. К их числу относится ряд химических производств, в том числе процессы переработки каменных углей, осуществляемые без доступ воздуха, и т. д[1].
7.4 Сернистый газ
Содержание природного ![]() в атмосфере ничтожно, его источниками являются вулканические процессы и окисление в воздухе сероводорода, поступающего в результате жизнедеятельности бактерий-десульфузаторов. Незначительные количества
в атмосфере ничтожно, его источниками являются вулканические процессы и окисление в воздухе сероводорода, поступающего в результате жизнедеятельности бактерий-десульфузаторов. Незначительные количества ![]() выделяются в воздух также в результате окисления с поверхности рудных месторождений, содержащих сульфиды. В почвенном воздухе над месторождениями сульфидных руд содержание сернистого газа составляет 25-50 частей на миллиард при фоновой концентрации от -15 до 10 частей на миллиард. Таким образом, источники природного
выделяются в воздух также в результате окисления с поверхности рудных месторождений, содержащих сульфиды. В почвенном воздухе над месторождениями сульфидных руд содержание сернистого газа составляет 25-50 частей на миллиард при фоновой концентрации от -15 до 10 частей на миллиард. Таким образом, источники природного ![]() ограничены в масштабах. Однако поступление в тропосферу значительных количеств техногенного сернистого газа уже в настоящее время представляет одну из наиболее серьезных проблем загрязнения окружающей среды[2].
ограничены в масштабах. Однако поступление в тропосферу значительных количеств техногенного сернистого газа уже в настоящее время представляет одну из наиболее серьезных проблем загрязнения окружающей среды[2].
Присутствие ![]() в атмосфере оказывает не только прямое отрицательное воздействие на жизнедеятельность животных и растений. Взаимодействуя с кислородом воздуха,
в атмосфере оказывает не только прямое отрицательное воздействие на жизнедеятельность животных и растений. Взаимодействуя с кислородом воздуха, ![]() преобразуется в крайне реакционноспособный
преобразуется в крайне реакционноспособный ![]() , который с водой атмосферы дает серную кислоту. Разрушительные свойства последней общеизвестны. Реакция окисления сернистого газа до
, который с водой атмосферы дает серную кислоту. Разрушительные свойства последней общеизвестны. Реакция окисления сернистого газа до ![]()
![]() О +М →
О +М →![]() +
+ ![]() ;
;
2![]() +
+ ![]() + окислители →
+ окислители → ![]() ;
;
![]() +
+ ![]() →
→ 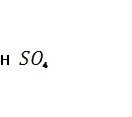 .
.
Где М – любая молекула газа. Первая реакция требует одновременно столкновения молекулы ![]() , атомарного газа и любой другой газообразной молекулы, которая служит для отвода образуемой в процессе столкновения и реакции энергии. Иначе этот процесс же пойдет в обратном направлении и
, атомарного газа и любой другой газообразной молекулы, которая служит для отвода образуемой в процессе столкновения и реакции энергии. Иначе этот процесс же пойдет в обратном направлении и ![]() вновь будет преобразован в
вновь будет преобразован в ![]() с отщеплением атома кислорода. Особенно благоприятные условия для прохождения этой реакции существуют в пределах озонового слоя атмосферы, где атомарный кислород непрерывно генерируется в процессе распада молекул на О и
с отщеплением атома кислорода. Особенно благоприятные условия для прохождения этой реакции существуют в пределах озонового слоя атмосферы, где атомарный кислород непрерывно генерируется в процессе распада молекул на О и ![]() . В результате в стратосфере на высоте порядка 18 км существует слой с повышенной концентрацией
. В результате в стратосфере на высоте порядка 18 км существует слой с повышенной концентрацией 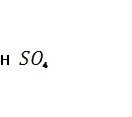 , поскольку
, поскольку ![]() легко соединяется с присутствующей в атмосфере водой. Вторая реакция для быстрого осуществления требует присутствия окислителей. Последние всегда накапливаются в воздухе, загрязненном в результате производственной деятельности человека. Таким образом, окисление
легко соединяется с присутствующей в атмосфере водой. Вторая реакция для быстрого осуществления требует присутствия окислителей. Последние всегда накапливаются в воздухе, загрязненном в результате производственной деятельности человека. Таким образом, окисление ![]() до
до ![]() с последующим образованием серной кислоты особенно интенсивно происходит в атмосфере городов и в районах промышленных предприятий[2].
с последующим образованием серной кислоты особенно интенсивно происходит в атмосфере городов и в районах промышленных предприятий[2].
Высокая растворимость 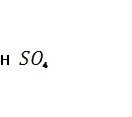 , образующейся в результате окисления сернистого газа, в воде определяет быстрое удаление серной кислоты из атмосферы с дождями. В результате проблема загрязнения атмосферы сернистым газом слилась с проблемой «кислых дождей». Возможные экологические последствия столь резкого окисления дождевых вод пока еще не вполне ясны. Беспокойство экологов, в ча
, образующейся в результате окисления сернистого газа, в воде определяет быстрое удаление серной кислоты из атмосферы с дождями. В результате проблема загрязнения атмосферы сернистым газом слилась с проблемой «кислых дождей». Возможные экологические последствия столь резкого окисления дождевых вод пока еще не вполне ясны. Беспокойство экологов, в ча