Курсовая работа: Теоретичні основи генно-модифікованих продуктів
Сформувалися два альтернативних напрямки у використанні технології рекомбінантної ДНК: введення генів шляхом векторних систем та пряме введення ДНК до рослинних клітин. Ці технології знаходяться на стадії модельних експериментів, однак ряд розробок вже мають практичне використання в селекції. Найбільш тріумфальні успіхи генетичної інженерії пов'язані з мікробіологічним синтезом просто організованих білків тваринного (людського) походження (гормони, ферменти, інтерферон та ін.).
З точки зору операційної технології рекомбінантні ДНК можна поділити на декілька головних компонентів: індивідуальні гени, регуляторні елементи, векторні та селекційні системи.
Таблиця 1 Прогресгенетичноїінженеріїврізнихсферахбіології.
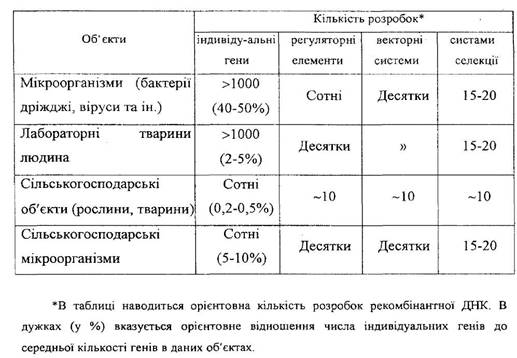
Перенесення та експресія індивідуальних добре охарактеризованих генів, власне, і складає кінцеву мету будь яких генно-інженерних маніпуляцій. Регуляторні елементи у представників різних родів, не кажучи вже про більш значні таксономічні одиниці, можуть значно розрізнятися. Тому перед перенесенням гену (наприклад, бактеріального) в чужорідне генетичне оточення (наприклад, в рослинну клітину) в гені необхідно замінити бактеріальні регуляторні елементи на рослинні, так як в іншому випадку перенесений ген не буде експресуватися. Подібній модифікації необхідно н ряді випадків піддавати також і структурну частину ієну, оскільки у рослин та тварин вона в типовому випадку складається з так званих інтронів та екзонів, при цьому тільки останні ділянки гена кодують поліпептидний ланцюг білку, а перші - вирізаються (видаляються) в процесі дозрівання ДНК. Імовірно, що ген з невидаленими інтронами, що належить до оукаріотичної клітини, не може кодувати синтез відповідного білку в клітині бактерії. Третім істотним елементом генно-інженерних маніпуляцій є спеціальні пекторні системи, які забезпечують високоефективне перенесення чужорідного гену в реципієнтну клітину та мого стабільне закріплення або шляхом інтеграції з клітинною ДНК, або шляхом набуття статусу автономного ядерного або цитоплазматичного елементу. Та, нарешті, четвертим важливим фактором технології рекомбінантної ДНК є система селекції або детекції тих химерних клітин або організмів, в які включився та функціонує чужорідний ген.
Для вирішення головних завдань біотехнології необхідно сконцентрувати увагу на питанні використання індивідуальних генів, молекулярних механізмів формування основних селекційно-вагомих показників та регуляторних елементів, так як вони визначають експресію генів в онтогенезі еукаріот.
Особливу увагу слід приділити розробці складових технології рекомбінантної ДНК, в першу чергу різноманітних векторних систем та систем селекції, при цьому не допустити розриву між фундаментальними та прикладними розробками; для цього необхідно забезпечити пріоритетність науковим працям в галузі мікробіології та вірусології. Тоді можна очікувати, що генетична інженерія стане лідируючою наукою, яка буде використовуватися в технологічних процесах отримання нових біологічно активних речовин, сироваток, різноманітних ліків та іншого
При обговоренні переваг методів клітинної та генетичної інженерії для створення на їх базі сучасних напрямків біотехнології неодноразово висловлювалась думка, що з двох біоінженерій клітинна по ряду причин забезпечує більш швидке отримання практично вагомих результатів. Це висловлювання, яке є правильним у загальній формі, потребує істотних доробок. Дійсно, строки реалізації ряду вагомих біотехнологічних розробок на базі методів клітинної інженерії знаходяться в межах початку та кінця 90-х років, а деякі з них впроваджуються в практику вже зараз. Так, наприклад,безвірусненасінництворяду сільськогосподарських культур або трансплантація ембріонів с/г тварин. Технологія рекомбінантної ДНК, в протилежність напівемпіричним підходам клітинної інженерії, спроможна реалізовувати свій вагомий науковий потенціал тільки при детальній молекулярно-біологічній та генетичний вивченості об'єктів та господарсько вагомих ознак, які є предметом генно-інженерного експерименту. Це як раз і зумовлює строки реалізації більшої частини розробок генетичної інженерії на початок 2000-х років.
Однак, існує можливість (і вона частково використується) для значного прискорення результатів генетичної інженерії. Джерелом цього прискорення можуть стати інтенсивні дослідження мікроорганізмів та вірусів, які мають практичне значення, а також стабільний пошук простих моногенних ознак рослин та тварин, за якими просто вести селекцію. У цьому випадку мова не йде про мікробіологічний синтез фізіологічно активних речовин на основі технології рекомбінатної ДНК типу гормонів, антибіотиків та ферментів, які використовуються у виробництві. У загальній формі віруси та мікроби відіграють дуже важливу роль у життєдіяльності тварин та рослин, виступаючи в ролі симбіонтів або паразитів. Тому, маніпулюючи з просто організованим генетичним матеріалом вірусів та мікробів, можливо в значних масштабах впливати на життєдіяльність та продуктивність цих об'єктів, обходячи обмеження, які віддаляють строки реалізації розробок генетичної інженерії при безпосередніх маніпуляціях з генетичним матеріалом рослин та тварин.
На порозі польових випробувань знаходиться проект, націлений на створення "біологічних пестицидів" - рекомбінантних клітин Pseodomonas fluorescens, які входять до асоційованої сапрофітної мікрофлори ряду культурних рослин, куди вбудований ген ентомопатогенного токсину Васіllus thiringiensis. Можна вказати також на успішні спроби боротьби з ранніми заморозками шляхом генетичної модифікації клітин Pseodomonas syringae , які являють собою сапрофітну мікрофлору багатьох рослин, яка відповідає за уражуючий ефект ранніх заморозків. Особливий білок, що секретується цими бактеріями, служить центрами кристалізації льоду, в результаті чого вода на поверхні рослини замерзає, як звичайно, не при -4°, а при температурі 0°С. Рекомбінантні клітини Рs. syringae, які загубили здатність секретувати білок-кристалізатор льоду, будуть першими химерними організмами, які вийдуть з лабораторії у довкілля.
Значну практичну вагу для інтенсивних біотехнологій має стійкість культурних рослин до гербіцидів, яка може досягатися двома шляхами: або за рахунок значного руйнування гербіциду в клітині, або за рахунок непроникненності клітин для конкретного гербіциду. Зараз гербіцидостійкість може бути досягнена шляхом перенесення в культурні рослини або бактеріального гену, або мутантного рослинного гtну, що руйнують такі розповсюджені гербіциди, як гліфосат та сульфоніл-сечовина, У процесі розробок знаходяться і рекомбінантні плазміди, які спроможні попереджувати утворення корончатих галів у рослин. Строки реалізації інших генно-інженерних проектів, так чи інакше пов'язаних з мікроорганізмами, відносяться до початку третього тисячоліття.
Що стосується генів виших еукаріот, то відносно швидко можуть бути реалізовані інтерфероновий та гормональний проекти, як у формі продуктів мікробного синтезу, так і у формі генів, що переносяться до організму. У випадку інтерферону продукт мікробного синтезу в ряді експериментів підвищував стійкість рослинних клітин до фітовірусних інфекцій, і можна розраховувати, що подібний ефект забезпечить безпосереднє введення інтерферонового гену до рослин. Препарати типу гормону росту при введенні тваринам стимулюють їх ріст. Отримання гігантських форм може бути досягнено, як це продемонстровано в експериментах на лабораторних тваринах, також при введенні гена гормону росту, який забезпечує посилений синтез цього регулятора в організмі. Інші генно-інженерні проекти наведені в таблиці 3 та розраховані на більш довгострокові терміни реалізації.
ГЕН ЯК ЕЛЕМЕНТАРНА ОДИНИЦЯ СПАДКОВОСТІ
Раніше вважалося, що гени являють собою частину хромосом і є неподільною одиницею з такими ознаками: здатністю визначати ознаки організму, здатністю до рекомбінації, тобто до переміщення з однієї гомологічної хромосоми в іншу при кросинговері, та здатністю до мутації з утворенням нових алельних генів. Надалі виявилося, що ген - це складна система, в якій зазначені особливості неподільні.
Ген складається з окремих ніби сходинок, що блискуче підтвердилося новими дослідженнями. Ген являє собою частину молекули ДНК і складається з сотень пар нуклеотидів. Ген як функціональну одиницюамериканськийгенетикС.Бензер запропонував назвати цистроном. Саме цистрон визначає послідовність амінокислот у коленому специфічному білку.
Цистрон у свою чергу підрозділяється на гранично малі в лінійному вимірі одиниці - рекони, які здатні до рекомбінації при кросинговері. Виділяють, крім того, поняття мутон - це найменша частина гена, здатна до мінливості (мутації). Розміри рекону та мутону можуть становити одну або кілька пар нуклеотидів, цистрону -сотні і тисячі пар нуклеотидів.
Виявляється, що різні функції -гена пов'язані з відрізками ланцюга ДНК різного розміру. Ген має складну структуру, в середині якої можуть відбуватися процеси мутації та рекомбінації. Виявлені також гени, які не контролюють синтез визначених білкіп, але регулюють цей процес. Таким чином, виникла необхідність роз'єднати гени на дві категорії: структурні та функціональні.
Стурктурні гени визначають послідовність амінокислот у поліпептидному ланцюзі (тобто, колінеарність). У тих бактерій, де вони вивчені, структурні гени, як правило, розміщені в хромосомі в послідовності відповідно до кодованих реакцій.
Функціональні гени, мабуть, не утворюють специфічних продуктів, які можна виявити в цитоплазмі. Ці гени контролюють функцію інших генів. Один з функціональних генів одержав назву гена-оператора.
За уявленнями, введеними в науку Ф.Жакобом та Ж.Моно, ген-оператор і ряд структурних генів, розміщених поряд у лінійній послідовності, складають оперон. Оперон - це одиниця зчитування генетичної інформації, тобто з кожного оперона знімається своя молекула ІРНК. Функція гена-оператора, в свою чергу, регулюється геном-регулятором. Він кодує синтез білка-репресора. Наявність чи вісутність цього білка, який приєднується до гена-оператора, визначає початок або припинення зчитування інформації.
Колінеарність-властивість,зумовлена відповідністюміжпослідовностямикодонів нуклеїнових кислот та амінокислот поліпептидних ланцюгів. Тобто колінеарність - це властивість, яка створює таку саму послідовність амінокислот у білку, в якій відповідні кодони розміщуються в гені. Це значить, що положення кожної амінокислоти у поліпептидному ланцюзі залежить від особливої ділянки гена. Генетичний код вважається колінеарним, якщо кодони нуклеїнових кислот та відповідні їм амінокислоти в білку розміщені в однаковому лінійному порядку.
Явище колінеарності доведено експериментально. Так, встановлено, що серповидноклітинна анемія, при якій пошкоджується будова молекули гемоглобіну, зумовлюється зміною розміщення нуклеотидів у гені, який відповідає за синтез гемоглобіну.
Завдяки концепції колінеарності можна визначити приблизний порядок нуклеотидів всередині гена та в ІРНК, якщо відомий склад поліпептидів. Навпаки, визначивши склад нуклеотидів ДНК, можна прогнозувати амінокислотний склад білка. Виходячи з цього, зміна порядку нуклеотидів у гені (його мутація) веде до зміни амінокислотного складу білків.
Під впливом різних фізичних та хімічних агентів, а також при нормальному біосинтезі білка в клітині можуть виникати пошкодження. Виявилося, що клітини мають механізми виправлення пошкоджень у нитках ДНК. Така їх здатність одержала назву репарації.
Вперше здатність до репарації була виявлена у бактерій, на які впливали ультрафіолетовими променями. Внаслідок опромінювання цілісність молекул ДНК порушується, оскільки в ній виникають димери, тобто з'єднані між собою сусідні піримідинові основи. Ці димери виникають між: двома тимінами, тиміном та цитозином, двома цитозинами, тиміном та урацилом, цитозином та урацилом, двома урацилами. Проте опромінені клітини на світлі виживають набагато краще, ніж у темряві. Після ретельного аналізу причин цього встановили, що в опромінених клітинах на світлі відбувається репарація (явище світлової репарації). Вона здійснюється спеціальним ферментом, який активується квантами видимого світла. Фермент з'єднується з пошкодженою ДНК, роз'єднує зв'язки, що виникли у димерах, та відновлює цілісність ДНК.
Пізніше була виявлена темнова репарація, тобто властивість клітин ліквідувати пошкодження ДНК без участі видимого світла. Темнова репарація здійснюється комплексом із п'яти ферментів: який "впізнає" хімічні зміни на ділянці в ланцюзі ДНК; здійснює "вирізування" пошкодженої ділянки; видаляє цю ділянку; синтезує нову за принципом комплементарності та з'єднує кінці старого ланцюга і відновленої ділянки.
Під час світлової репарації виправляються тільки ті пошкодження, які виникають під впливом ультрафіолетових променів, при темповій - такі, що виникають під дією іонізуючої радіації, хімічних речовин та інших факторів. Темнова репарація виявлена як у прокаріотів, так і в клітинах еукаріотів (тварин та людей), у яких вона вивчається в культурах тканин. Питання про те, чому одні пошкодження репаруються, а інші ні, залишається відкритим. Якщо репарація не відбувається, то клітина гине або виникає мутація.
1.2 ГЕНЕТИЧНИЙ КОД
З моделі структури ДНК, запропонованої Уотсоном і Кріком, відомо, що генетична інформація передається за допомогою якоїсь специфічної послідовності нуклеотидів її молекули. Вперше питання про код було поставлене Гамовим у 1953 р.
Початок прямого генетико-біохімічного аналізу кодонів було покладено в 1961 р. Ніренбергом та Маттеї, які створили найпростіші синтетичні полімери й замінили ними нативні молекули іРНК в системі компонентів клітин бактерій та суміші амінокислот. У суміші кожного типу одна з амінокислот була помічена радіоактивним вуглецем С14, інші дев'ятнадцять не мали позначення. Було встановлено, що синтетичний полірибонуклеотид, складений тільки з урацилу (поліуридилова кислота - УУУУУ), визначає синтез білка, в якому кожна амінокислоти була фенілаланіном. Виходячи з цього, встановили, що триплет УУУ є кодоном для фенілаланіну.
У наступних подібних експериментах було визначено, що поліаденінова кислота містить код для лізину, а поліцитидинова - для проліну. Наступні досліди, де як штучні ІРНК виступали полінуклеотиди змішаного складу (наприклад, полі-АУ), виявили зв'язок між рядом інших поєднань нуклеотидів та конкретними амінокислотами.