Курсовая работа: Тепломассообмен при испарении и горении капель жидких топлив
2.1 Метод Зельдовича
Для вывода критического воспламенения воспользуемся методом Зельдовича Я.Б. Разделим область rк < r < rпл на две зоны: первая прилегает к поверхности приведенной пленки rв < r < rпл ; вторая - rк < r < rв . Здесь rв - координата условной границы, на которой происходит воспламенение. Пренебрегая теплом, выделяющимся при химической реакции во второй зоне rк < r < rв , уравнение (1.2) запишем в виде
 (2.1)
(2.1)
решая которое получим

а с учётом

имеем выражение для теплового потока
 (2.2)
(2.2)
Для первой зоны rв < r < rпл, пренебрегая изменением температуры с координатой![]() , так какдействие химических источников способствует выравниванию температуры по зоне, получим
, так какдействие химических источников способствует выравниванию температуры по зоне, получим
 (2.3)
(2.3)
Сравнивая (2.1) и (2.3) видим, что на границе двух зон r = rв должна существовать область ![]() ,в которой
,в которой
![]() (2.4)
(2.4)
т.е. количество тепла, выделяемое за счёт химической реакции ![]() , равно теплу, отводимому
, равно теплу, отводимому ![]() . Равенство (2.4) представим в виде первого условия Семёнова
. Равенство (2.4) представим в виде первого условия Семёнова
![]()
Второе условие Семёнова, определяет неустойчивость теплового равновесия
 (2.5)
(2.5)
Подставив в (2.4) ![]() из (2.2)
из (2.2)
 (2.6)
(2.6)
Скорость химической реакции зависит от концентрации паров и температуры. Для определения связи концентрации с температурой запишем уравнение диффузии

Учитывая подобие граничных условий для температуры и концентрации, можно доказать, что
 .
.
Скорость химической реакции в случае избытка окислителя определяется кинетическим уравнением первого порядка
 (2.7)
(2.7)
и зависит только от температуры.
Используя уравнения Семёнова, (2.4) и (2.5), имеем систему уравнений
 (2.8)
(2.8)
 (2.9)
(2.9)
из которой надо исключить температуру парогазовой смеси Тв .
Разделив (2.8) на (2.9), получим уравнение

позволяющее выразить Тв через температуру среды. Оценка величины ![]() даёт малую величину по сравнению с
даёт малую величину по сравнению с ![]() . Поэтому без особой погрешности примем
. Поэтому без особой погрешности примем
 (2.10)
(2.10)
Из (1.13) имеем ранее полученную формулу для массовой скорости испарения
 (2.11)
(2.11)
которая при Nu = 2
 . (2.12)
. (2.12)
Выполним преобразование Франк-Каменецкого
![]()
Подставим в (2.8) и используем (2.10)
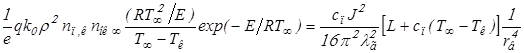
Найдём радиус воспламенения, интегрируя уравнение (2.2) в пределах от rк до rв и от rк до rпл . В результате получим
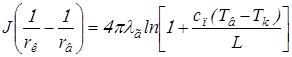
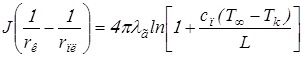
Используя формулу (2.11), имеем
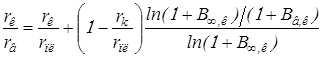 ,
,
где
![]()
Учитывая (2.10) и представляя
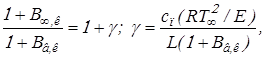
где ![]() , получим формулу для rв в виде
, получим формулу для rв в виде
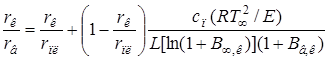 (2.13)
(2.13)
Для случая неподвижной среды ![]() и координата “поверхности” воспламенения определяется как
и координата “поверхности” воспламенения определяется как
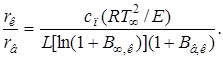
Для капли этилового спирта расчёт по этой формуле даёт rв /rк ≈25. Большое расстояние, на котором происходит воспламенение, требует большого времени, чтобы установилось квазистационарное распределение температур и концентраций в газовой фазе. Очевидно, что это время не должно превышать времени полного испарения капли. Поэтому критическое условие воспламенения (2.9) совместно с (2.13) для случая неподвижной среды может использоваться только для грубой оценки.